Western Blot: analisi delle proteine e fasi principali della tecnica
Slide sul Western Blot, una tecnica di laboratorio per l'analisi delle proteine. Il Pdf è utile per studenti universitari di Biologia, spiegando il principio del blotting e le fasi di purificazione delle proteine.
Mostra di più49 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
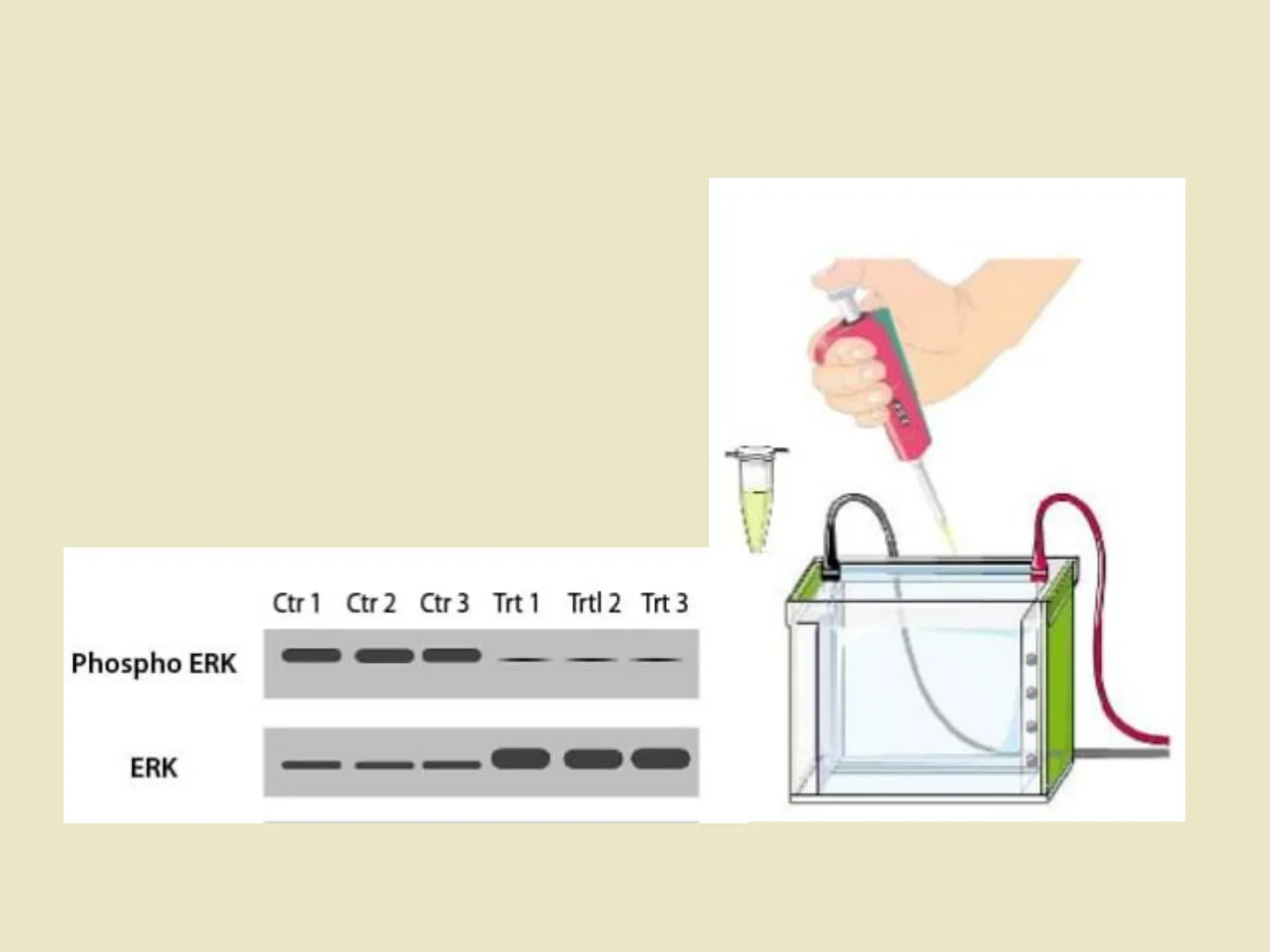
Western Blot
Ctr 1 Ctr 2 Ctr 3 Trt 1 Trtl 2 Trt 3 Phospho ERK ERK
IBlotting
Trasferimento di macromolecole su una membrana
- DNA: Southern blot (Edwin Southern, 1975)
- RNA: Northern blot (James Alwine, David Kemp e George Stark, 1977)
- Proteine: Western blot (Neal Burnette, 1979)
Cosa è un Western Blot?
È una tecnica in cui le proteine sono, inizialmente, separate mediante elettroforesi su gel e successivamente trasferite su un supporto (membrana o filtro). Questa tecnica si usa per rilevare e quantificare proteine che reagiscono con un anticorpo specifico.
-
? + +
Fasi del western blot
Gel cassette Tissue Electrode chamber Add sample + Tank Anode Cathode  Lysate/Extracts Pour Gel and Assambling device Pipet samples and buffer 3 Electrophoresis 4 Separated protein bands 5 1 2) Cathode Buffer Anode Buffer Cell Bacterial I I
FASE 1: Purificazione delle proteine
Estrazione e frazionamento
Una proteina per poter essere purificata deve prima essere estratta dalla sua matrice biologica e poi allontanata selettivamente dalle altre proteine mediante procedure di frazionamento opportune. Purificare una proteina significa ottenerla in forma omogenea (pura), far sì che la proteina di interesse sia l'unica presente nel campione a disposizione.
Fattori che influenzano la purificazione
- CALORE
- DETERGENTI
- METALLI PESANTI
- PH La solubilità di una proteina dipende dal pH, dall'aggiunta di sali (ammonio solfato) e di solventi organici Per prevenire la denaturazione e la rottura dei ponti disolfuro si usano composti contenenti tioli (mercaptoetanolo, glutatione ridotto e ditiotreitolo) Esistono inibitori di proteasi, ciascuno specifico per una proteasi (a serina, a cisteina, aspartiche e metalloproteasi) e inibitori di fosfatasi.
FASE 1: Purificazione delle proteine
Metodi di rottura delle cellule
Metodi meccanici: · Omogenizzatori · Frantumazione con abrasivi · Presse · Sonicazione DA ASITAM TH
Metodi non meccanici: · shock osmotico : l'acqua fuoriesce dalle cellule quando poste in mezzo ipertonico. Le cellule vengono trasferite in una soluzione ipotonica dove entra acqua e la cellula si lisa. · congelamento/scongelamento : provoca fuoriuscita di materiale intracellulare e disgregazione interna dovuta a formazione di cristalli di ghiaccio. · enzimi litici : causano danneggiamento della membrana/parete cellulare. Le cellule possono subire un blando trattamento meccanico o shock osmotico
FASE 1: Purificazione delle proteine
Dosaggio delle proteine
Misurazione della concentrazione totale delle proteine Saggio colorimetrico di Bradford
0.4 0.3 595 A 595 0.2 0.1- 0.04 0 2 4 6 8 10 Concentrazione proteina (ug ml-1)
FASE 2: Elettroforesi
Tecnica che permette di separare particelle dotate di cariche elettriche positive o negative, in base alla loro migrazione differenziale attraverso un mezzo fluido, sotto l'influenza di un campo elettrico. La ionizzazione del gruppo carbossilico dà luogo alla formazione di cariche negative, mentre l'assunzione di protoni sul gruppo amminico determina la presenza di cariche positive.
- Ogni molecola proteica posta in soluzione ad un certo pH potrà avere una prevalenza di cariche elettriche positive (catione) o negative (anione) oppure carica totale = 0 (ugual numero di cariche elettriche positive o negative).
- Il valore di pH al quale la proteina ha carica totale =0 costituisce il punto isoelettrico (pI) della proteina.
- A valori di pH<pI la proteina ha una prevalenza di cariche positive e sotto l'influenza di un campo elettrico migra verso il polo negativo (catodo).
- A valori di pH>pI la proteina ha una prevalenza di cariche negative e sotto l'influenza di un campo elettrico migra verso il polo positivo (anodo).
- A valori di pH=pI la proteina ha una carica netta = 0 e sotto l'influenza di un campo elettrico non migra.
Elettroforesi
- Il passaggio di corrente elettrica attraverso il gel permette la migrazione delle proteine (caricate negativamente a pH >8) verso l'anodo.
- La porosità del gel determina la resistenza al passaggio delle molecole, quelle di maggior dimensioni saranno più rallentate.
Proteine Gel poroso Elettroforesi
FASE 2: Elettroforesi
SDS-PAGE
Sodium-Dodecyl-Sulphate PolyAcrilammide Gel Electrophoresis
- L'SDS è un detergente che carica negativamente le proteine
- E' un gel denaturante: non evidenzia strutture quaternarie
- Separazione di proteine in base alla massa molecolare
- Determinazione della massa molecolare
- Western blot
0 II Na+ 0-S-0-(CH2)11CH3 II 0 Sodium dodecyl sulfate (SDS)
FASE 2: Elettroforesi
SDS-PAGE e ruolo dell'SDS
Nell'SDS-PAGE le proteine vengono esposte al Sodio Dodecil Solfato (SDS) prima e durante l'elettroforesi
+ + - - - H H + + +- - - H - - + -
Ruolo dell'SDS: le proteine multimeriche si dissociano nelle loro subunità: sono forzate in conformazioni estese tutte le catene polipeptidiche assumono la stessa DENSITA' DI CARICA. Il trattamento con SDS elimina le differenze di forma e carica, quindi l'unico determinante della velocità di migrazione sarà il PESO MOLECOLARE.
FASE 2: Elettroforesi
Migrazione e separazione delle biomolecole
Le molecole di grandi dimensioni migrano in genere più lentamente di quelle piccole: ciò permette la separazione delle diverse biomolecole all'interno del gel. I gel di poliacrilammide si fanno a concentrazioni diverse di acrilammide: le dimensioni dei pori diminuiscono all'aumentare della sua concentrazione (%).
5 % 10 % 15 % -200 kD - 75 kD - 35 kD - 120 kD - 50 ŁD - 25 kD - 35 k:D - 75 kD - 25 KD - 15 kD 50 kD - 15 :D - 10 kD .
- 200 kDa - 70 kDa gel al 6-8%
- 80 kDa - 50 kDa gel al 8-10%
- 45 kDa - 20 kDa gel al 15-20%
FASE 2: Elettroforesi
Polimerizzazione del gel
Polimerizzazione S2Og -- SO .-. 0 TEMED 0 TEMED CONH2 CONH2 SO4 -· + A . HỌC= NH, HỌC NH, CONH2 H,NOC S2Og -- SO4 -· 0= 0 0 H2 NH NH SO4 -* + + H2C= N N =CH2 HỌC= NH2 1 NH NH O O= H,NOC
I gel di poliacrilamide si formano dalla co-polimerizzazione di acrilamide e di un agente che forma legami trasversali (N,N'- bisacrilamide) a formare un reticolo tridimensionale
Poly Acrilamide Gel Electrophoresis (PAGE)
- Acrilamide monomero (neurotossico)
- N,N'-bisacrilamide (BIS) ramificante
- Ammonio persolfato (APS) forma radicali
- N,N,N,N-Tetrametil- Etilenediamina (TEMED) stabilizza i radicali
CH3 N H3C. CH3 N CH3 H,C= NH 0 O H, C. H2C= Z- N =CH2 H H (NH4)2S2Og H H . 0 TEMED
FASE 2: Elettroforesi
SDS-PAGE: Gel di impacchettamento e separazione
- Gel di impacchettamento (stacking gel) 4% di acrilammide pH 6.8
- Serve per concentrare le proteine in una sottile banda prima della separazione
- Si sfrutta una forza ionica ed un pH differenti rispetto al tampone elettroforetico ed allo stacking gel
- Pori larghi per una libera migrazione e concentrazione
- Migliora la risoluzione
- Gel di separazione (running gel) pH 8.8 Le percentuali di acrilammide variano:
- 15% per proteine di peso molecolari tra 10.000-100.000 Da
- 10-7.5 % per proteine di peso molecolare maggiore di 100.000 Da
FASE 2: Elettroforesi
SDS-PAGE: Allineamento e separazione
Stacking gel allineamento Separating/running gel separazione
Negative Electrode Load samples here Buffer well well well Stacking Gel Running Gel big proteins J Glass Plates Positive Electrode 1 Spacer small proteins Buffer An illustration of an apparatus used for SDS PAGE. Sample JUUUU Direction of migration + (a)
FASE 2: Elettroforesi
SDS-PAGE: Preparazione
Preparazione
FASE 2: Elettroforesi
SDS-PAGE: BIO-RAD
BIO-RAD ead st gels FB (WP) A
FASE 2: Elettroforesi
SDS-PAGE: Esempio di migrazione
Sample € Direction of migration 0 (a) 1 2 e Myosin 200,000 B-Galactosidase 116,250 Glycogen phosphorylaseb 97,400 Bovine scrum albumin 66,200 Ovalbumin 45,000 - Carbonic anhydrase 31,000 Soybean trypsin inhibitor 21,500 Lysozyme 14,400 + Unknown M. standarde protein (a)
FASE 3: Rivelazione e stima delle proteine da gel
- Colorante
- Affinità uguale per tutte le frazioni proteiche
- Proporzionalità diretta tra assunzione di colore e concentrazione di proteina
- Sensibilità . Comassie Brilliant Blue · Rivela fino a 0.1 mg di proteine · Silver staining · Ag+ -- > Ag sulla proteina · Rivela fino a 0.1 ng
A ¥536 SPD added (M) WT 10- 10-7 10-# 10-9 M +- 52 kDa - 31 kDa - 19 kDa £17 kDa + 11 kDa Coomassie stain gel B SPD added (M) Y536 WT 10-6 10-7 10- 10-9 M +-52 kDa +31kDa +-19 kDa +17 kDa +11 kDa Ponceau-S stain
FASE 4: Trasferimento
Tipologie di Blotting
- Wet Transblot system
- Semidry system MEDIUM
FASE 4: Trasferimento
Come preparare il sandwich
Come preparare il sandwich
FASE 4: Trasferimento
Preparazione del sandwich per il trasferimento
Come preparare il sandwich spugna filtro catodo 0 gel corrente membrana filtro + spugna anodo
FASE 4: Trasferimento
Apparato WET TransBlot
Trasferimento su carta Casting nero
Partendo dal casting nero: · 1 spugna · 2 fogli di carta · Gel
Casting bianco
- Membrana
- 2 fogli di carta
- 1 spugna
Nell'assemblaggio si colloca nero nella direzione del nero, bianco nella direzione del rosso. Le proteine, cariche negativamente, corrono verso il polo positivo
FASE 4: Trasferimento
BIOTEAD
BIOTEAD Dott.ssa Angelucci C.B.
FASE 4: Trasferimento
Componenti dell'apparato di trasferimento
Lid Fiber pad Filter paper Membrane Gel Filter paper Fiber pad Gel holder cassette Blue cooling (keep frozen at -20℃) Electrode module Buffer tank
FASE 4: Trasferimento
00000000000000/ 00000000000000/
FASE 4: Trasferimento
Schema del trasferimento
Filter paper Filter paper Proteins- O + Foam pad Polyacrylamide gel Nitrocellulose membrane Foam pad
FASE 4: Trasferimento
Disposizione degli elementi per il trasferimento
Gel Membrana Carta assorbente Spugna - Catodo O- + Anodo Tampone di trasferimento
FASE 4: Trasferimento
FASE 4 : TRASFERIMENTO
FASE 4: Trasferimento
Configurazioni per 4 e 2 gel
4 Gels 2 Gels
FASE 4: Trasferimento
Trasferimento nell'apparato Semidry system
Electrical Contact Electrical Contact Metal Spacer 2 Lid with vents Power Cord IBlot" Gel Barriers Gel Barriers De-bubbling Surface Blotting Surface è invitrogen Start/Stop Button Metal Spacer 1 Alignment Guide
FASE 4: Trasferimento
Trasferimento Semidry system
Trasferimento nell'apparato Semidry system Carta assorbente - Catodo Corrente O O C Gel Proteine > V Membrana + Anodo
FASE 4: Trasferimento
FASE 4 : TRASFERIMENTO
FASE 4: Trasferimento
FASE 4 : TRASFERIMENTO
FASE 4: Trasferimento
Trasferimento nell'apparato Semidry system
3. Trasferimento nell'apparato Semidry system Transfer Move proteins from gel to membrane
FASE 4: Trasferimento
Confronto tra i due sistemi di trasferimento
Confronto tra i due sistemi Spugna-cassetta - Carta da filtro Gel Membrana ++ Tampone Apparato Semidry WET Trans Blot
Vantaggi: veloce, economico (meno buffer) Svantaggi: efficienza di trasferimento limitata (dimensione gel, % acrilammide, peso molecolare)