Terapia Genica: Patologie, Modalità di Somministrazione e Vettori
Documento sulla Terapia Genica. Il Pdf, un insieme di appunti ben strutturati, esplora le patologie curabili, le modalità di somministrazione e i vettori utilizzati in Biologia a livello universitario, con riferimenti a studi clinici e farmaci approvati.
Mostra di più17 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Terapia Genica: Panoramica
Le patologie che possono essere curate attraverso la terapia genica sono malattie ereditarie monogeniche (mutazione difettiva a carico di un singolo gene). Per poter potenzialmente produrre il farmaco atto alla terapia genica è fondamentale identificare e caratterizzare il gene e la mutazione su di esso, responsabile della malattia. Tra alcune di queste malattie sono stati effettuati dei trials clinici con produzione finale, solo in alcuni casi, di un farmaco.
Patologie Curabili con Terapia Genica
Le patologie curabili con la terapia genica sono:
- Malattie ereditarie: emoglobinopatie (talassemia); una serie di immunodeficienze acquisite; disordini metabolici, i quali possono sfociare o meno in malattie neurodegenerative; distrofia muscolare; fibrosi cistica, per la quale sono stati effettuati molti trials ma nessuno di questi ha portato ad una minima risoluzione della patologia; retinopatie; diabete; malattie cardiovascolari.
- Malattie tumorali: tumori solidi e neoplasie ematologiche. Si sono riscontrati numerosi successi nei trials mirati alla cura dei tumori, soprattutto per quanto riguarda le neoplasie ematologiche.
- Malattie infettive: AIDS, Epatite B ed Epatite C.
Cellule Target della Terapia Genica
In generale, la terapia genica può avere diverse cellule target:
- Somatiche: una volta manipolata la cellula e inserito la copia corretta del gene, tutte le cellule figlie, derivanti dalla proliferazione della cellula manipolata, esprimeranno la copia del gene terapeutico. Usate per malattie ereditarie del sangue e immunodeficienze
- Staminali: usate con più frequenza. Le staminali, infatti, intraprendono processi di autorinnovamento (self-renawal) grazie a divisioni asimmetriche. In questo modo viene mantenuto abbastanza costante nel tempo un pool cellulare di progenitori; essi a loro volta prolifereranno permettendo l'origine in finale di tutte le cellule differenziate di un determinato organo. La trasmissione del gene terapeutico avverrà in tutta la progenie della cellula staminale. Usate per malattie ereditarie del sangue e immunodeficienze
- Germinali: la manipolazione delle cellule dell'embrione attualmente non è praticata sia per ragioni pratiche che per ragioni etiche (altra probabilità di manipolare anche altre caratteristiche genetiche). Una eventuale manipolazione delle cellule germinali permette l'acquisizione del gene terapeutico da parte di tutte le cellule componenti il futuro organismo; potenzialmente è l'approccio migliore per la cura delle malattie ereditarie. In Italia la manipolazione di cellule germinali può avvenire solo e unicamente per scopi riproduttivi; in altri paesi la manipolazione può avvenire anche per scopi nozionistici (acquisire nozioni su caratteristiche, strutture e funzionamento cellule embrionali) in quanto, di fatto, non si hanno delle ripercussioni genetiche sul nascituro.In Cina furono manipolati degli embrioni con lo scopo di ottenere resistenza genica al virus dell'HIV (scienziato successivamente arrestato).
Modalità di Somministrazione della Terapia
Si riconoscono 3 modalità di somministrazione della terapia:
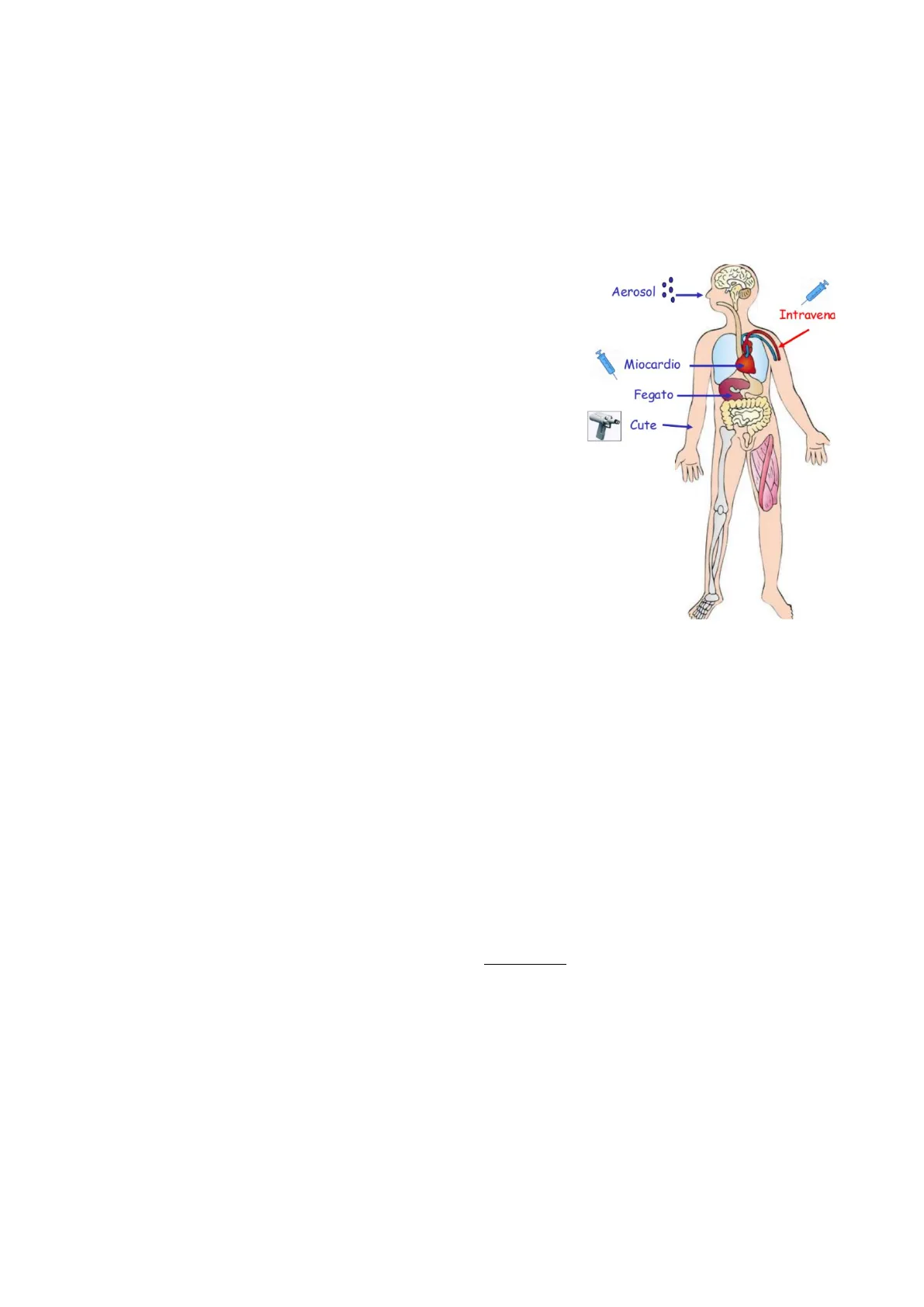
- EX VIVO: consiste nel prelevare le cellule (somatiche o staminali) dal paziente, manipolarle e successivamente reintrodurle all'interno del paziente stesso. Questo approccio permette di avere una vera e propria limitazione al livello della reazione immunitaria dell'ospite. È al momento la modalità più utilizzata, pur rimanendo comunque limitata alle cellule facilmente accessibili e prelevabili; quindi, non si può usare sulle cellule di organi interni, per le quali si opterà per terapie in situ o in vivo. Modalità usata per il trattamento di malattie immunologiche, ematologiche, metaboliche e della cute (tramite biopsia si possono recuperare cellule staminali e manipolarle). Aerosol Intravena Miocardio Fegato Cute
- IN SITU: la terapia genica è somministrata direttamente nell'organo affetto tramite iniezione/inalazione. Si possono trattare patologie/tumori dell'apparato cardiaco, respiratorio, epatico e a livello della cute.
- IN VIVO: è un approccio a livello sistemico; la terapia è data al paziente per via intravena. Questa modalità è la meno efficacie in quanto la terapia deve circolare tramite sangue, raggiungere organo target e in aggiunta superare tutte le barriere biologiche rappresentate dalle membrane delle cellule tissutali.
Vettori della Terapia Genica
Il gene correttivo è trasportato da un vettore, il quale idealmente deve avere le seguenti caratteristiche:
- il trasferimento deve essere efficiente, ossia in grado di trasdurre un alto numero di cellule;
- deve essere in grado di incorporare DNA di varie dimensioni, per accomodare il potenziale gene correttivo di lunghezze variabili;
- l'espressione del gene terapeutico deve essere regolata e prolungata nel tempo, ossia la sua espressione deve essere il più possibile simile a quella del gene endogeno per non andare incontro a fenomeni di sovraespressione/sottoespressione;
- non deve essere patogeno e tossico per l'organismo;
- deve evitare l'innesco di reazioni immunitarie.Nessun vettore ad oggi utilizzato risulta avere simultaneamente tutti questi prerequisiti; si cerca quindi di utilizzare sistemi che rispecchino il più possibile queste caratteristiche.
Vettori Virali e Non Virali
Vettori virali Vettori non virali Gene clonato m Membrana nucleare Integrazione casuale o sito-specifica Gene integrato Gene episamico DIVISIONE CELLULARE Integrazione del transgene nel genoma ospite +espressione stabile Il transgene non si integra nel genoma ospite >>espressione transiente Si utilizzano in maniera predominante vettori virali, si parla di trasduzione); si possono anche usare vettori non virali (si parla di trasfezione). I vettori virali, in via preferenziale, si integrano nel genoma; il gene correttivo, integrandosi, avrà dunque un'espressione stabile. I vettori non virali invece rimangono liberi nel citoplasma in forma episomiale, non integrandosi al genoma. Ciò implica un'espressione transiente del gene correttivo; laddove vi sia la necessità di una stabilità nel tempo è più opportuno ripetere le somministrazioni.
Vettori Virali
La maggior parte dei vettori usati, dunque, hanno origine dal genoma virale. Nella struttura generale del virus è possibile distinguere:
- Core, in cui è localizzato il genoma (di solito DNA a doppio filamento o RNA a singolo filamento) complessato a componenti proteiche;
- Capside, rivestimento del core presente in tutti i virus;
- Envelope, presente solo in alcuni virus. È di fatto un ulteriore rivestimento, esterno al CORE: Acido nucleico + proteine capside, formato per lo più da lipidi e CAPSIDE glicoproteine con funzione di entrare in contatto coi recettori medianti l'endocitosi, facilitando l'ancoraggio e del virus stesso alla cellula ospite. Se non presente tale rivestimento il processo di ancoraggio/entrata nella cellula è mediato da alcuni componenti del capside. RIVESTIMENTO (envelope)
Classi di Virus per Vettori
Per l'ingegnerizzazione di vettori sonno state utilizzate 3 classi di virus:
| Vettore | Ospite e localizzazione | Dimensioni dell'inserto |
| Adenovirus (virus raffreddore) | Vari mammiferi, episomico | Inserto fino a 36 kb, elevato livello espressione |
| Virus adeno-associati | Vari mammiferi, si integra in siti specifici sul cromosoma 19 | Inserto fino a ~5 kb, necessita di adenovirus per packaging |
| Retrovirus | Ampia gamma, si integra in maniera casuale | Dimensioni fino a 8,5 kb (CARGO=dimensione massima dell'inserto che può contenere il vettore; dipende dalla dimensione del genoma del virus dal quale deriva il vettore stesso.) |
Retrovirus, tra cui si trovano anche i lentivirus, hanno un envelope.
Meccanismi di Trasferimento del Genoma Virale
Il trasferimento del genoma virale nella cellula ospite avviene grazie ai seguenti meccanismi:
- interazione con le cellule da infettare mediante legame ai recettori di membrana. Ad esempio, il retrovirus HIV prende contatto tramite le proprie glicoproteine di rivestimento col recettore CD4 e corecettore CCR5;
- segue un'internalizzazione per endocitosi recettore-mediata;
- dopo la fuoriuscita dall'endosoma, avverrà un'integrazione nel genoma ospite grazie a specifiche sequenze (processo che avviene solo in alcuni virus);
- avviene la replicazione del genoma; questo passaggio avviene con diverse modalità a seconda del virus se a DNA o RNA. Si procede anche alla trascrizione e traduzione di tutto l'apparato proteico formante il capside e, laddove previsto, l'envelope;
- si ha il processo di impacchettamento con formazione terminale dei virioni, i quali rilasciano la cellula ospite e, attaccando altre cellule, permettono la propagazione dell'infezione stessa. Alcuni virus sono in grado di attraversare la membrana nucleare, altri no e pertanto possono infettare solo le cellule proliferanti, ossia le cellule che si trovano in fase S in cui si ha la scomparsa della membrana stessa.
Progettazione di Vettori Virali
Nella progettazione di vettori virali è importantissimo andare a disattivare tutti quei processi che comportano l'infettività e la propagazione di essa. Infatti, il genoma virale subisce delle modifiche in maniera tale da rendere il virus difettivo per la replicazione e incapace di produrre le componenti proteiche di packaging del virione. In questo modo è impedita la propagazione e diffusione di virus ricombinanti, eliminando la patogenicità. Alla sostituzione del transgene terapeutico ai geni virali deve seguire anche l'apposizione di un promotore forte che dirige l'espressione del transgene stesso. In questo modo il transgene subisce una trascrizione veloce, la quale non sottostà alla regolazione trascrittiva del virus stesso. La scelta del vettore virale è dettata da tre aspetti: lunghezza del transgene (considero il cargo); tipo di malattia da curare e sito d'insorgenza.
Adenovirus
Gli adenovirus hanno un genoma di 36 kb rappresentato da una molecola di DNA; essi infettato principalmente cellule di mammifero (virus raffreddore) sia proliferanti che post-mitotiche (sono quindi in grado di oltrepassare la barriera della membrana nucleare). Capside Penton Fibe -VI IX 3 Fibre VIII Illa Il genoma inizia e finisce con le sequenze ITR (Ripetizioni Terminali Invertite) le quali servono come origine di replicazione e promotori trascrizionali. Al 5' la ITR è seguita dalla sequenza ų (psi) la quale è una sequenza di regolazione per il packaging; non codifica per le proteine ma dirige l'assemblaggio di esse. All'interno del genoma si possono distinguere due classi di geni:
- geni precoci, i quali sono indicati con la E (E1, E2B, E2A, E3, E4). Essi sono i primi geni che vengono attivati in quanto si occupano della replicazione/trascrizione virale e inibizione della risposta immunitaria dell'organismo ospite;
- geni tardivi, i quali sono indicati con L (L1, L2, L3, L4, L5). La loro trascrizione è attivata successivamente e codificano per le proteine strutturali costituenti il capside (assente envelope) Tramite le proprie protrusioni, l'Adenovirus si lega alla membrana plasmatica della cellula bersaglio; entra per endocitosi; l'endosoma si fonde poi con un lisosoma. L'ambiente acido di quest'ultimo favorisce l'escape del virus e il rilascio del genoma virale, il quale si integrerà nel genoma ospite.
Vettori Adenovirali
Sono state sviluppate diverse generazioni di vettori, tutte aventi lo scopo ultimo di ridurre al minimo il potenziale patogenico. ΔΕ ΔΕ3 1 generazione Transgene ΔΕ JE2 ΔΕ3 ΔΕ 14 kb Transgene 3 generazione 36 kb Transgene I. 1º generazione prevede l'eliminazione dei geni E1 e E3, rendendo rispettivamente difettivo il virus per la replicazione e immune per l'escape. Il cargo disponibile in questa generazione è di 8kb. II. 2º generazione prevede l'eliminazione di tutti i geni precoci; il cargo in questa generazione sale a 14 kb. III. 3º generazione è caratterizzata dalla rimozione, oltre che dei geni precoci, anche dei geni tardivi. Il cargo sale a 36kb e del genoma di partenza vengono mantenute solo le sequenze ITR e y. In termini di cargo i vettori adenovirali sono i più efficienti. 0 10000 20000 30000 36000 pill PVTI PV 52K pilla PX PVI Hexon Protease 100K 33K 22K 12.5K gp 19k 14.7K EIB-19K EIB-55K 12 PVII Fiber E1 PIX L1 13 L4 E3 15 ITR ITR E2B pIVa2 Polymerase DTP E2A DBP E4 Orf3 Orf6 Orf6/7 Hexon 8 kb 2 generazione