Le proteine e gli amminoacidi: struttura, proprietà e valore nutrizionale
Documento di Università sulle Proteine. Il Pdf, per il corso di Chimica, esplora la struttura, le proprietà chimico-fisiche e il valore nutrizionale delle proteine e degli amminoacidi, con schemi e grafici per illustrare i concetti.
Mostra di più17 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Le Proteine
- le proteine sono polimeri di aminoacidi ( + di 20 AA) a diversi livelli di organizzazione (struttura primaria, secondaria, terziaria, quaternaria)
- possono essere coniugati con gruppi prostetici (glucidi, lipidi, gruppo eme ... )
- principale fonte di azoto: glucidi e lipidi non contengono azoto
- importanza nutrizionale, specialmente le proteine contrattili del muscolo (actina e miosina) e quelle di riserva (proteine dell'uovo, semi ... )
- in certi casi possono essere fattori anti-nutrizionali: inibitori enzimatici (es: proteine che bloccano l'attività di amilasi -> l'amido che mangio non genererà quei glucosi che serviranno per la mia nutrizione), lectine, allergeni (nella maggior parte dei casi sono proteine), tossine come la ricina nei semi di lino (sostanze che nuocciono a qualunque soggetto che le ingerisca; gli allergeni nuocciono solo a determinati soggetti)
- le proteine influenzano la consistenza (texture) di un alimento: sono gelificanti (es. colla di pesce), emulsionanti e possono fare schiume (prerogativa unica delle proteine)
- alcune proteine possono influenzare il gusto e l'aroma di un prodotto -> es: la taumatina è un dolcificante (a dare gusto dolce sono veramente poche)
- la degradazione degli aminoacidi porta alla formazione di composti (amine biogene), tipici dei cibi in decomposizione -> sono in grado di influenzare (o loro stesse o il loro metabolismo) la sfera sensoriale, sono percepibili con bocca e naso es. pesce non conservato produce istamina, che deriva da istidina= ammina biogena
Amminoacidi
- unità di base delle proteine; composti polifunzionali costituiti da idrogeno + almeno un gruppo carbossilico ed uno amminico + gruppo R che li caratterizza
- il gruppo funzionale caratterizza le loro proprietà chimico-fisiche (polarità, idrofobicità, carica ... )
- il carbonio centrale è un centro chirale
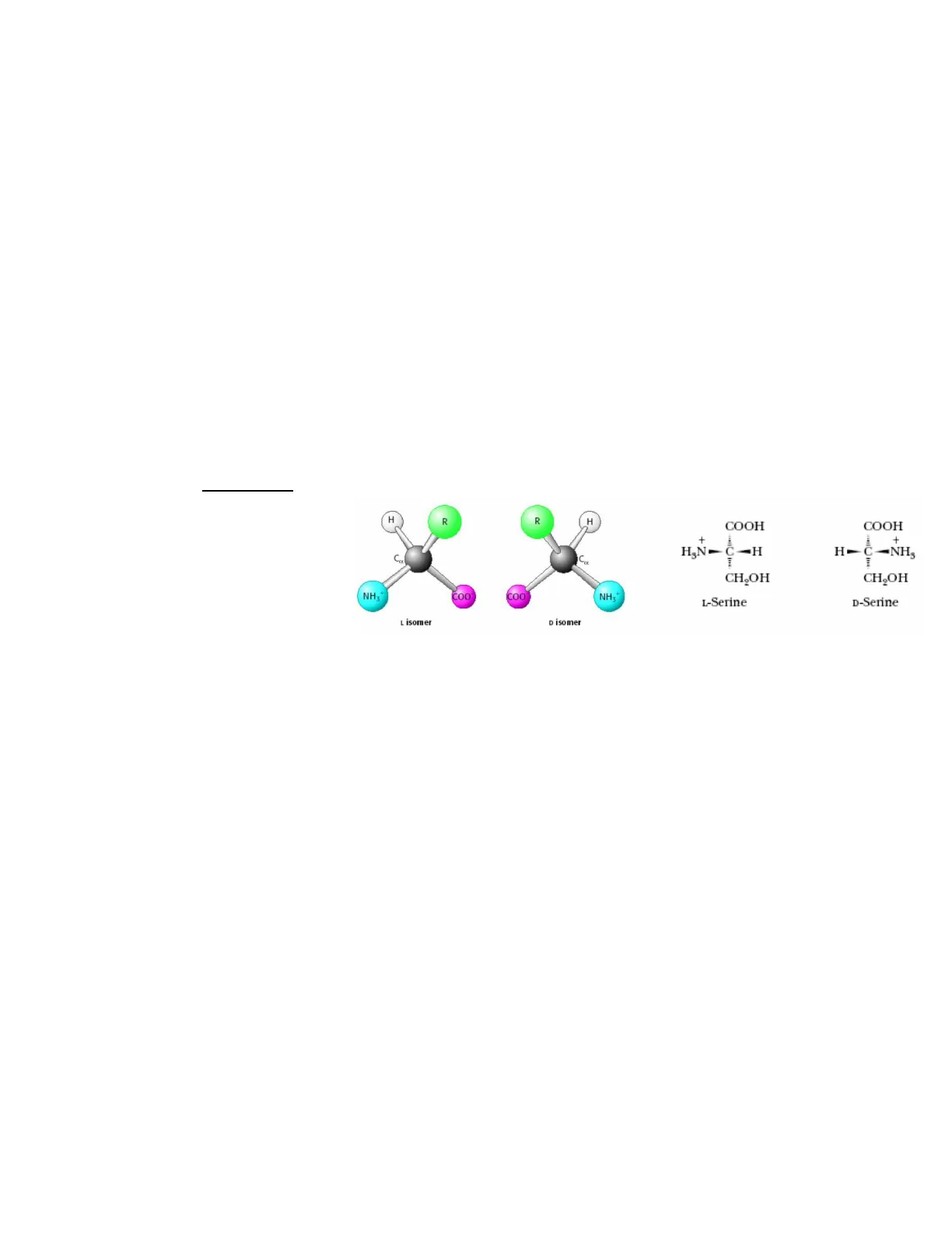
- esistono due serie di AA, la serie L e la serie D
- nelle proteine sono presenti solo L- amminoacidi; i D-amminoacidi sono molto più rari e spesso derivano da processi microbici (fermentazioni) -> la loro presenza è molto rara in un alimento e difficilmente identificabile con i classici sistemi di separazione (essendo stereoisomeri sono molto difficili da separare)
H R R H COOH + C CHŞOH CHỊOH NH3+ COO COO NH L-Serine D-Serine L isomer D isomer
- la differenza nella solubilità degli amminoacidi sta nell'aumento della catena idrocarburica -> più aumenta meno è solubile
Gruppi R Alifatici, Non Polari
il gruppo R alifatico non carico produce una lipofilicità maggiore con il complicarsi della sequenza amminoacidica
- Glicina: unico AA di cui non esistono stereoisomeri > presenta come R un H
- Alanina
- Prolina
- Leucina
- Isoleucina
- Valina questi ultimi 3 hanno la caratteristica comune di avere una catena laterale ramificata; sono rinomati integratori
Gruppi R Polari, Non Carichi
la polarità è conferita dai residui polari come lo zolfo, tiolo, gruppi amidici, ossidrili la presenza di molecole polari, determina particolari interazioni con l'acqua e particolare solubilità
- Metionina Cisteina
- Treonina
- Serina
- Asparagina
- Glutammina
Gruppi R Aromatici
se esiste un gruppo aromatico significa che assorbono nell'ultravioletto -> possiamo usarli per determinare in maniera semi- quantitativa la quantità di queste proteine sfruttando l'assorbimento dei gruppi aromatici, è possibile quantificare la quantità di proteine
- Fenilalanina
- Tirosina
- Triptofano
COOH + H-C -- NH3 H3N-C-Hlegge di Lambert Beer
- A = epsilon * c * 1 A: assorbanza c: concentrazione della proteina espressa come molarità e: coefficiente di estinzione molare (specifico per ogni molecola) l: lunghezza del cammino ottico (cm)
- si illumina la soluzione con lunghezza d'onda di 280 nm > lunghezza d'onda proporzionale alla concentrazione degli AA aromatici presenti
- legge utilizzata per quantificare le proteine in soluzione
- i numeri del grafico sono numeri bassi (assorbanza): anche quando avrò una concentrazione elevata di proteine
- il coefficiente per la fenil alanina ha un massimo intorno a 260 nm ed è molto basso; aumenta per tirosina e per triptofano > assorbono luce a I= 280 nm circa
- è fondamentale per una proteina avere un gruppo aromatico; sappiamo che le molecole aromatiche assorbono nell'ultravioletto, per cui se all'interno di una proteina è presenta un AA aromatico, questa proteina può essere studiata e può essere quantificata in soluzione
- i restanti AA sono trasparenti agli ultravioletti per cui non verranno determinati
Gruppi R Carichi
- POSITIVAMENTE: Lisina, Arginina e Istidina
- NEGATIVAMENTE: Acido aspartico e Acido Glutammico
- questi 5 AA sono i principali responsabili della carica di una proteina: permettono di determinare il PUNTO ISOELETTRICO di una proteina
- punto isoelettrico: valore di pH al quale una molecola presenta carica elettrica netta nulla (pari a zero)
- per un aa avente un solo gruppo amminico ed un solo gruppo carbossilico, il valore di pH può essere determinato dai valori della costante di dissociazione acida di ciascuno dei due gruppi calcolandone la media
- gli amminoacidi sono sostanze anfotere, ovvero si comportano sia da acidi che da basi: la pka del gruppo carbossilico e quella del gruppo amminico sono molto diverse -> a pH acido l'amminogruppo è sempre protonato; alzando il pH si ha la deprotonazione dell'ammino gruppo; alzando ulteriormente il pH si ha la carica negativa
- di conseguenza gli amminoacidi possono fungere da sistemi tampone -> tampone è una soluzione che per sua natura non viene influenzata dal pH; un tampone fosfato mantiene il suo pH a 7, quindi se cerchiamo di alteralo il tampone esso risponderà mentendosi il più possibile all'interno del suo range di pH
Reazioni dei Gruppi Carbossilici
Esterificazione
R-CH-COOH + R'-OH NHỌCIS HO + R-CH-COOR' + H2O NHỌCIO
- il gruppo carbossile può essere fatto reagire con un alcolo e si ottiene la versione esterificata di un amminoacido
- possiamo trovare AA esterificati ad esempio nel vino (MetOH e EtOH)-> la lunga permanenza fra le due classi di molecole (alcol + amminoacidi) fa sì che queste reazioni chimiche abbiano una certa importanza
- il legame estere è un legame abbastanza labile, quindi può essere idrolizzato facilmente a pH estremi
Reazioni dei Gruppi Amminici
- è molto più stabile il legame che forma l'amminogruppo
- il gruppo amminico a pH neutro è protonato (NH3+) > a pH fisiologico
Acilazione Mediante Alogenuri Acidi o Anidridi (Acetica, Succinica ... )
R'-COX + H2N CH-COOP + OHª R R'-CO-NH-CH-COOP + Xe + H2O R
- modificazione della catena laterale applicazioni delle reazioni dei gruppi aminici: N-acetil AA usati come ingredienti in quanto il loro valore biologico rimane intatto; queste molecole non possono fare reazione di Maillard in quanto protette dal gruppo acile, per cui non vengono denaturate questi N-acetil-AA possono essere usati come:
- fortificazione proteine vegetali
- protezione da degradazione anche la tirosina può reagire anche se in maniera minima
Reagenti per la Rilevazione di Amminogruppi
- per analizzare N-terminali di proteine e AA si compiono acilazione o arilazione tramite DANS-Cl (fluoroforo), DABS e TNBS, ossia molecole con base aromatica fortemente cromofori
- questi composti reagiscono con gli amminogruppi, producendo degli AA-marcati che possono essere analizzati: ho questa esigenza perché la maggior parte degli aa è trasparente agli UV
- se ogni aa è legato a un gruppo di questi, posso seguirli, individuarli e misurarli tramite spettrofotometro
- acilazione con DANS-Cl (fluoroforo): analisi di N-terminali di peptidi o proteine; la prolina è l'AA più complesso, farla reagire è un problema, spesso i metodi vanno modificati
- acilazione con DABS utile per detection di AA (anche Pro e OH-Pro) mediante HPLC
- acilazione con TNBS (acido tri nitro benzen sulfonico): derivato giallo analizzabile per spettrofotometria
- DANS DABS e TNBS assorbono bene nel visibile e alcuni nell'ultravioletto
- in tutti i casi queste molecole reagiscono con l'amminogruppo quando si trova nella sua forma dissociata: a pH alto l'amminogruppo è NH2 (forma dissociata= deprotonata) e non NH3+ (forma non dissociata= protonata)
- per reagire l'ammino gruppo deve essere nella sua forma dissociata NH2, infatti il pH è alto (basico TUTTI I COMPOSTI CARBOSSILICI IN BIOCHIMICA SI TROVANO IN FORMA DISSOCIATA POICHÈ SI HA UN VALORE DI PH MOLTOMAGGIORE RISPETTO AL PKA
- ph = pKA + 10g [A~] [HA]
GRUPPO CARBOSSILICO > [CH3CO0] [ CH3 COOH ] < [RNH3+] < [RNH2 ] 1 1 0 1 2 +m 4 4,74 5 6 7 7,4 8 9 ph [RCOOH ]=[COO-] Pka 11 fisiologico [RNH3+] = [ RNH2 ] a ph fisiologico = 7,4 il gruppo carbossifico si trova in forma deprotonata [ CH3000-], il gruppo amminico in forma protonata [NH3+]: questo spiega la struttura dell'amino acido
- reagente di folin-> deriva da questa chimica fa reagire tirosine > anche questo serve per marcare gli AA
- reazioni con isocianati o tiocianati: reazione sfruttata nella degradazione di Edman (sequenziamento); per sapere che proteina è presente, è possibile utilizzare questo metodo, che consiste nel rompere l'amminoacido nell'n-terminale e andare ad identificare tramite HPLC
- reazioni con i gruppi carbonili: la reazione di Maillard (e la reazione di Strecker) è una reazione che incide sull'ammino gruppo; la reazione con nidrina (reazione di Strecker) è impiegata per la quantificazione degli AA
- OPA (oftal aldeide o aldeide oftalica) e mercaptoetanolo: si forma un fluoroforo per l'analisi di aa in HPLC
- OPA: molecola bifunzionale che reagisce con molecola tiolica (tiolo libero come cisteina) e AA a formare un addotto particolare che è un fluoroforo che viene analizzato tramite detector o fluorimetro (misuro aa legati all'OPA)
- applicazioni: dosaggio proteico + analisi profili di digestione
- la molecola di partenza non è fluorescente ma il fluorescente è il prodotto
- fluorescamina: composto fluorescente per l'analisi di amminoacidi, l'eccesso che non reagisce idrolizza e non emette fluorescenza; il prodotto finale che si ottiene (sia con fluorescamina che con OPA) fluoresce, ma non fluoresce la sostanza di partenza: questo è un bene perché è possibile evitare di purificare tramite via cromatografica i prodotti di reazione > ad esempio con i DANS non si può usare lo spettrofotometro perchè entrambi reagenti e prodotti sono fluorescent
OPA: Applicazioni
quantificazione di una proteina-> dosaggio proteico
1,200 y = 0,014x + 0,0151 R2 = 0,9992 1,000 0,800 8 0,600 0,400 0,200 0,000 0 20 40 60 80 100 ug
- si può costruire una retta di taratura -> modo per quantificcare una molecola di interessa es. ci interessa il glutatione, lo faccio reagire con una molecola di OPA (tutte le proteine con OPA diventano fluorescenti) , come faccio a sapere quanto glutatione è nel mio estratto? si fa la retta, poi la colorazione colorimetrica lo metto nello spettrofotometro e leggo l'assorbanza > non viene rilevato, la legge di Lambert Beer non funziona allora si prende glutatione puro e si fa una soluzione 1 micromolare (mM) + OPA= 0,7 oppure 0,2 > si fanno diverse diluizioni avremmo tanti punti che vanno a tracciare una retta y=mx + q
- a volte tutto questo non si può misurare in spettrofotometro perchè ci sono più molecole che assorbono alla stessa lunghezza d'onda
- i kit utilizzati e venduti in commercio per quantificare una proteina falliscono per via degli interferenti; tramite l'uso di questo sistema invece non ci sono interferenti
GRUPPO AMMINICO pka = 9