Proprietà generali degli elementi della Tavola Periodica
Slide sulle Proprietà generali degli elementi della Tavola Periodica. Il Pdf esplora il carattere metallico e non metallico, le reazioni dei metalli alcalini e alcalino-terrosi, con tabelle comparative per lo studio universitario di Chimica.
Mostra di più54 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Proprietà generali degli elementi della Tavola Periodica
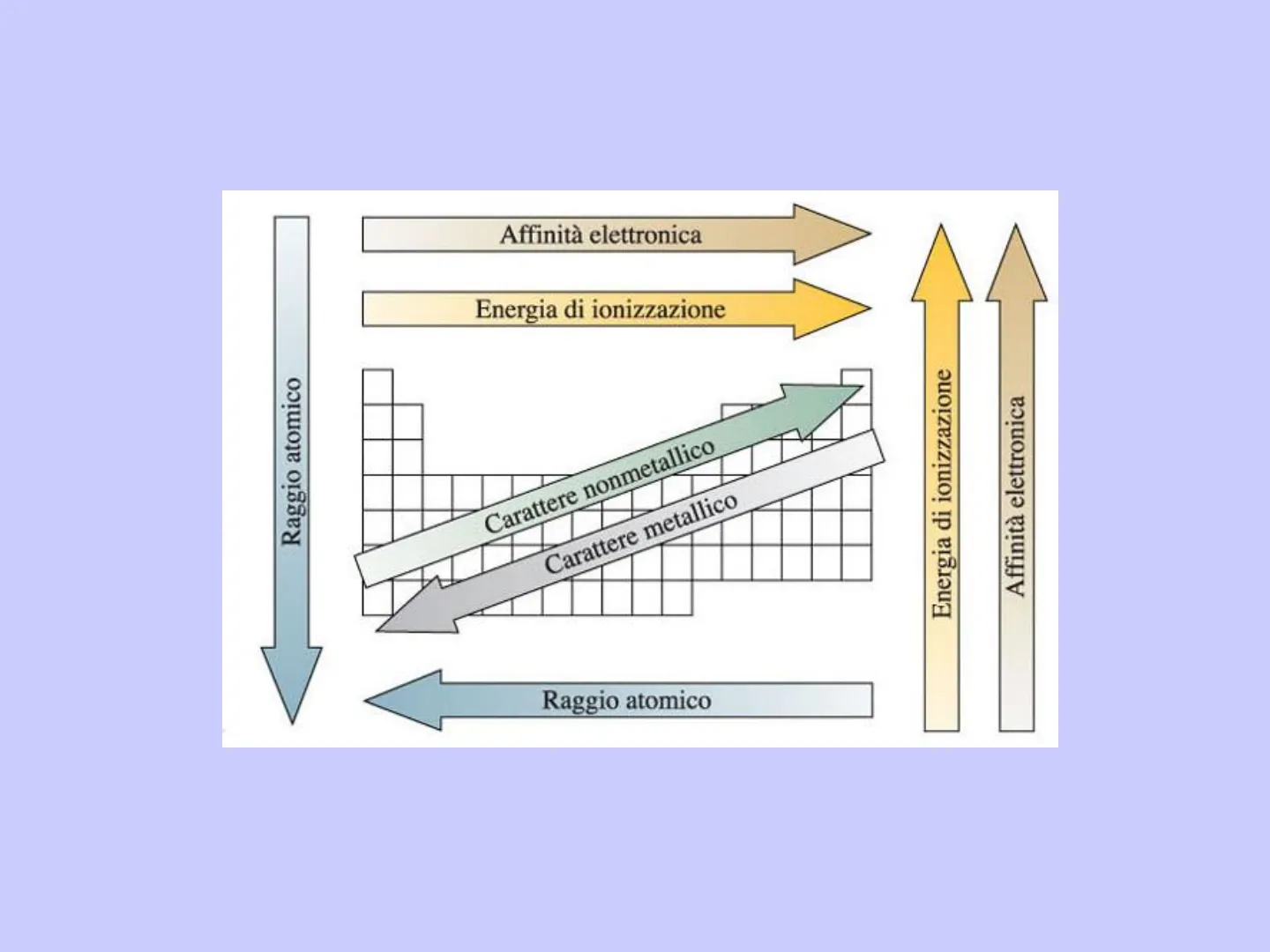
Abbiamo visto che una prima grossa divisione degli elementi della tavola periodica consiste nel loro carattere metallico o non metallico
Affinità elettronica
Energia di ionizzazione
Raggio atomico
Carattere nonmetallico
Carattere metallico
Il carattere metallico aumenta: - da destra a sinistra lungo un periodo - dall'alto al basso lungo un gruppoI metalli sono caratterizzati da: - basse energie di ionizzazione - affinità elettroniche piccole o positive - bassa elettronegatività Come risultato tendono a perdere gli elettroni di valenza formando cationi: Na+ Ca2+ Al3+ I non-metalli sono caratterizzati da: - elevate energie di ionizzazione - affinità elettroniche negative e grandi - elevata elettronegatività Come risultato tendono ad acquistare elettroni formando anioni monoatomici ed ossanioni: Cl- Br- S2- NO3" SO42- CIO4Sono esclusivamente metallici/non-metallici solo i gruppi all'estrema sinistra/destra della tavola periodica.
Metalli alcalini
I metalli alcalini II metalli alcalino-terrosi (XVI O, S, Se; Te, Po) XVII alogeni I gruppi XIII-XV presentano elementi non-metallici all'inizio e metallici alla fine.
1 2 13 14 15 16 17 18 H He Li Be BCNOFNe Na Mg Al Si P S CI Ar K Ca Ga Ge As Se Br Kr Rb Sr In Sn Sb Te I_XeQuasi tutti gli elementi formano ossidi. Gli ossidi sono classificati in: - ossidi basici: reagiscono con acidi (o ossidi acidi) per dare sali CaO + 2HCI -> CaCl2 + H2O - ossidi acidi: reagiscono con basi (o ossidi basici) per dare sali CO2 + 2NaOH -> Na2CO3 + H2O
1 2 13 14 15 16 17 Li Be BCNO F Na Mg Al Si P S CI K Ca Ga Ge As Se Br Rb Sr In Sn Sb Te I Cs Ba TI Pb Sn Po At FIGURA 10-17 Ossidi acidi, basici ed anfoteri degli elementi dei blocchi s e p.Gli ossidi, se solubili, danno reazioni caratteristiche con acqua. - I metalli danno ossidi basici. Gli ossidi dei metalli più reattivi (I e II gruppo) reagiscono con acqua per dare soluzioni basiche (formalmente idrossidi) CaO(s) + H2O(I) -> Ca(OH)2 -> Ca2+(aq) + 20H-(aq) - I non metalli danno ossidi acidi. Gli ossidi dei non metalli più elettronegativi reagiscono con acqua per dare soluzioni acide (formalmente acidi) SO2(g) + H2O(I) -> H2SO3 H+(aq)+ HSO3-(aq) Tali ossidi sono anche noti come anidridi. Vi sono però anche ossidi acidi non solubili reagiscono solo con basi o con ossidi basici. SiO2 + Cao -> CasiO3 (silicato di calcio)Ossidi di elementi non spiccatamente metallici o non metallici reagiscono sia con acidi che con basi (ossidi anfoteri). Al2O3(s) + 6H+ -> 2 Al3+(aq) + 3H2O(I) Al2O3 + 20H- + 3H20 -> 2 AI(OH)4-
1 2 13 14 15 16 17 Li Be BCN O F Na Mg Al Si P S C1 K Ca Ga Ge As Se Br Rb Sr In Sn Sb Te I Cs Ba TI Pb Sn Po At FIGURA 10-17 Ossidi acidi, basici ed anfoteri degli elementi dei blocchi s e p.Elementi del gruppo I Metalli alcalini Sono metalli dall'aspetto argenteo, teneri e bassofondenti (Tf<180℃) A Taglio di sodio metallico Il sodio, un metallo reattivo, è coperto da uno strato di ossido che lo protegge.
Li Na K Rb Cs Atomic number 3 11 19 37 55 Valence-shell electron configuration 2s1 3s1 451 5$1 651 Atomic (metallic) radius, pm 152 186 227 248 265 Ionic (M+) radius, pm 59 99 138 149 170 Electronegativity 1.0 0.9 0.8 0.8 0.8 First ionization energy, kJ mol-1 520.2 495.8 418.8 403.0 375.7 Electrode potential Eº, Vª -3.040 -2.713 -2.924 -2.924 -2.923 Melting point, ℃ 180.54 97.81 63.65 39.05 28.4 Boiling point, ℃ 1347 883.0 773.9 687.9 678.5 Density, g/cm3 at 20 ℃ 0.534 0.971 0.862 1.532 1.873 Hardnessb 0.6 0.4 0.5 0.3 0.2 Electrical conductivityc 17.1 33.2 22.0 12.4 7.76 Flame color Carmine Yellow Violet Bluish red Blue Principal visible emission lines, nm 610,671 589 405,767 780,795 456,459 "For the reduction M+(aq) + e" -> M(s). b Hardness measures the ability of substances to scratch, abrade, or indent one another. On the Mohs scale, ten minerals are ranked by hardness, ranging from that of talc (0) to diamond (10). Other values: wax (0 ℃), 0.2; asphalt, 1-2; fingernail, 2.5; copper, 2.5-3; iron, 4-5; chromium, 9. Each substance can scratch only other sub- stances with hardness values lower than its own. "On a scale relative to silver as 100.Elementi del gruppo I Metalli alcalini La loro configurazione elettronica di valenza è ns1. Essi pertanto reagiscono perdendo questo elettrone e formando monocationi quali Li+, Na+, K+, Rb+ e Cs+ che sono in genere solubili in acqua.
Li Na K Rb Cs Atomic number 3 11 19 37 55 Valence-shell electron configuration 2s1 3s1 451 5s1 6s1 Atomic (metallic) radius, pm 152 186 227 248 265 Ionic (M+) radius, pm 59 99 138 149 170 Electronegativity 1.0 0.9 0.8 0.8 0.8 First ionization energy, kJ mol-1 520.2 495.8 418.8 403.0 375.7 Electrode potential Eº, Vª -3.040 -2.713 -2.924 -2.924 -2.923 Melting point, ℃ 180.54 97.81 63.65 39.05 28.4 Boiling point, ℃ 1347 883.0 773.9 687.9 678.5 Density, g/cm3 at 20 ℃ 0.534 0.971 0.862 1.532 1.873 Hardnessb 0.6 0.4 0.5 0.3 0.2 Electrical conductivity 17.1 33.2 22.0 12.4 7.76 Flame color Carmine Yellow Violet Bluish red Blue Principal visible emission lines, nm 610,671 589 405,767 780,795 456,459Elementi del gruppo I Metalli alcalini Tutti questi metalli reagiscono con acqua dando gli idrossidi e liberando idrogeno con una reazione caratteristica. Ad esempio: 2 Li(s) + 2H2O(1) -> 2 LiOH(aq) + H2(g) La reattività aumenta scendendo lungo il gruppo perché diminuisce l'energia di ionizzazione e l'elettrone esterno viene perso più facilmente. La reazione avviene in maniera più violenta, ad esempio, per il potassio che per il sodio, tanto che la forte esotermicità può far incendiare l'idrogeno gassoso che è uno dei prodotti della reazione.Elementi del gruppo I Metalli alcalini Tutti i metalli alcalini possono formare ossidi basici di formula M2O che con acqua danno idrossidi che si comportano come basi forti 2 Li(s) + 202(g) LizO(s) Li2O(s) + H2O(1) > LiOH(s) > 2 Li+ + 2 OH- Essendo molto reattivi non si trovano mai come metalli liberi in natura ma come cationi in sali quali NaCl. A Cumuli di sale marino (cloruro sodico) ottenuto per evaporazione di acqua di mare.Elementi del gruppo I Metalli alcalini I metalli allo stato elementare sono in genere preparati per elettrolisi di sali fusi. NaCI(I) -> Na(s) + }Cl2(g) elettrolisi Amperometro Elettroni + NaCl fuso Cl2(g) Batteria Na(€) Elettrodo di grafite (inerte) Elettrodo di grafite (inerte) + Setto di ferro Catodo di ferro a forma di anello Anodo di grafite NaCl fuso è costituito da ioni Na+ e ioni CI- (b) Na+ viene ridotto (Na+ + le -> Na); quindi, catodo CI viene ossidato (2CI -> Cl, + 2e); quindi, anodo Questo perché i potenziali di riduzione dei cationi sono molto bassi (grandi e negativi) Na+ + le- - > Na E O Na+/Na = - 2,71 V Voltmetro +Elementi del gruppo II Metalli alcalino-terrosi Sono metalli relativamente più duri ed alto-fondenti, ma meno reattivi dei metalli alcalini.
Be Mg Ca Sr Ba Atomic number 4 12 20 38 56 Atomic (metallic) radius, pm 111 160 197 215 222 Ionic (M2+) radius, pm 27 72 100 113 136 Electronegativity 1.5 1.2 1.0 1.0 0.9 First ionization energy, kJ mol" 899.4 737.7 589.7 549.5 502.8 Electrode potential Eº, Vª -1.85 -2.356 -2.84 -2.89 -2.92 Melting point, ℃ 1278 648.8 839 769 729 Boiling point, ℃ 2970b 1090 1483.6 1383.9 1637 Density, g/cm3 at 20 ℃ 1.85 1.74 1.55 2.54 3.60 Hardness“ ~5 2.0 1.5 1.8 ~2 Electrical conductivity" 39.7 35.6 40.6 6.90 3.20 Flame color None None Orange-red Scarlet Green -1 ªFor the reduction M2+(aq) + 2 e -> M(s). b Boiling point at 5 mmHg pressure. "See footnotes of Table 22.2.Elementi del gruppo II Metalli alcalino-terrosi La loro configurazione elettronica di valenza è ns2. Pertanto essi reagiscono perdendo i due elettroni e formando di-cationi quali Mg2+, Ca2+, Sr2+, Ba2+ Il berillio perde più difficilmente gli elettroni e tende a formare legami covalenti (Ejon più grande), gli altri hanno comportamento simile ai metalli alcalini e la loro reattività aumenta scendendo lungo il gruppo. Reagiscono con acqua dando gli idrossidi e liberando idrogeno ma in maniera meno violenta dei metalli alcalini: Ca(s) + 2H2O(1) -> 2 CaOH2(aq) + H2(g)Elementi del gruppo II Metalli alcalino-terrosi Formano tutti ossidi basici di formula MO che in acqua danno idrossidi che si comportano come basi forti Ca(s) + 202(g) -> CaO(s) CaO(s) + H2O(I) -> CaOH2(s) H2O Ca2+ + 2 OH- Fa eccezione il berillio il cui ossido (e idrossido) è anfotero. I metalli alcalino terrosi non esistono liberi in natura e possono essere preparati per elettrolisi dei cloruri o per riduzione dell'ossido con un metallo che formi ossidi più stabili. + Anodo di grafite Catodo d'acciaio Cloro gassoso Mg spillato Atmosfera inerte Mg fuso MgCl2 fuso Figura 22-6 Cella di elettrolisi di MgCl2 fuso. Il magnesio metallico si forma sul catodo d'acciaio e risale verso l'alto, da dove è spillato periodicamente. Il cloro gassoso si forma attorno all'anodo di grafite ed è aspirato via.Elementi del gruppo XIII Con gli elementi del gruppo XIII si osserva una chiara tendenza all'aumento del carattere metallico scendendo lungo il gruppo dal boro al tallio.
Al Ga In TI Atomic number 13 31 49 81 Atomic (metallic) radius, pm 143 122 163 170 Ionic (M3+) radius, pm 53 62 79 88 Electronegativity 1.5 1.6 1.7 1.8 First ionization energy, kJ mol-1 577.6 578.8 558.3 589.3 Electrode potential Eº, Vª -1.676 -0.56 -0.34 +0.72 Melting point, ℃ 660.37 29.78 156.17 303.55 Boiling point, ℃ 2467 2403 2080 1457 Density, g/cm3 at 20 ℃ 2.698 5.907 7.310 11.85 Hardnessb 2.75 1.5 1.2 1.25 Electrical conductivityb 59.7 9.1 19.0 8.82 ª For the reduction M3+(aq) + 3 e -> M(s). b See footnotes of Table 22.2.Elementi del gruppo XIII Il primo elemento del gruppo, il boro, è un metalloide e la sua chimica è quella di un non-metallo. Quello che formalmente è il suo idrossido, B(OH)3, è un acido, l'acido borico, la cui formula spesso si indica come H3BO3 e che ha proprietà antisettiche. L'ossido del boro, B2O3, è un ossido acido e aggiunto al vetro gli conferisce resistenza alle alte temperature (Pyrex). I composti del boro con idrogeno, i borani, esistono come multipli dell'unità BH3. La molecola di borano BH3 non esiste come composto stabile. Il più semplice idruro di boro isolato è il diborano B2H6.
B B (a) 1s 3 sp3 sp H H H B B H H H 3 sp3 sp 1s (b)