Dosaggio delle Proteine: spettrofotometria e metodo del Biureto
Slide dall'Università degli Studi eCampus su Dosaggio delle Proteine. Il Pdf esplora la quantificazione delle proteine tramite spettrofotometria e metodi colorimetrici, con un focus sul Biureto. Questo materiale di Biologia, adatto per l'Università, è utile per lo studio autonomo.
Mostra di più15 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
UNIVERSITÀ DEGLI STUDI eCAMPUS
Corso di Laurea e Insegnamento
Corso di Laurea: Scienze Biologiche Biochimica Insegnamento: Lezione nº: Titolo: Attività nº: 52 Teoria laboratorio - dosaggio delle proteine 2 Facoltà di Psicologia
Quantificazione delle Proteine
DOSAGGIO DELLE PROTEINE Quantificazione delle proteine
@ 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it TA1
Spettrofotometro e Principi di Funzionamento
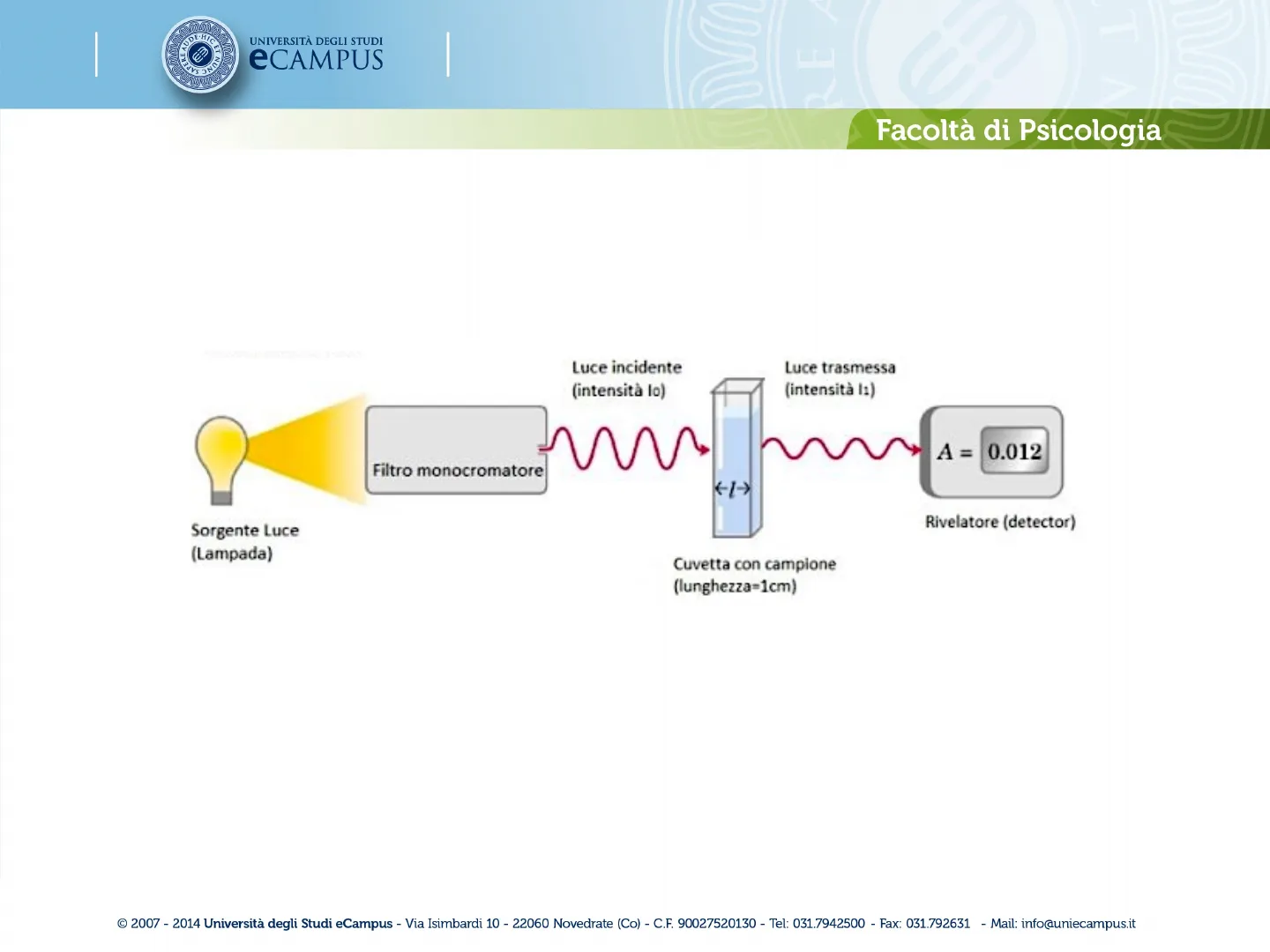
Componenti dello Spettrofotometro
Luce incidente (intensità lo) Luce trasmessa (intensità l:) A = 0.012 Filtro monocromatore Rivelatore (detector) Sorgente Luce (Lampada) Cuvetta con campione (lunghezza=1cm)
Lo spettrofotometro è un importante strumento che permette di quantificare, se presente, un determinato analita di interesse qualora esso abbia capacità (per proprietà chimico-fisiche proprie) di assorbire una o più lunghezze d'onda della radiazione elettromagnetica nello spettro UV-visibile. Lo spettrofotometro è lo strumento utilizzato per la quantificazione delle proteine all'interno di un campione indipendentemente dalla metodica scelta.
@ 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it TA1
Spettro della Radiazione Elettromagnetica
Dettagli dello Spettro EM
Increasing energy M V Increasing wavelength 0.0001 nm 0.01 nm 10 nm 1000 nm 0.01 cm 1 cm 1 m 100 m Gamma rays X-rays Ultra- violet Infrared Radio waves Radar TV FM AM Visible light 400 nm 500 nm 600 nm 700 nm
@ 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it1
Legge di Lambert e Beer
Principi di Assorbimento e Trasmittanza
Conoscendo la capacità di una determinata molecola di assorbire una determinata gamma di radiazioni elettromagnetiche (una determinata lunghezza d'onda), è possibile capire quante molecole sono presenti nel nostro campione. Infatti se ogni molecola assorbe una quantità x di radiazione, possiamo aspettarci che n molecole assorbiranno una quantità x x n di radiazione elettromagnetica alla lunghezza d'onda a cui quella molecola assorbe. La quantità finale di radiazione che riuscirà ad emergere dal lato opposto del campione colpito dal fascio di luce monocromata sarà uguale alla quantità iniziale meno la quantità x x n che viene assorbita dalle molecole nel campione. La luce trasmessa (quella che riesce ad emergere dal campione) viene rappresentata dalla trasmittanza, quella che viene assorbita dall'assorbanza e sono ovviamente inversamente proporzionali poichè maggiore è la quantità di molecole che assorbono, maggiore è la quantità di radiazione assorbita e minore sarà quella trasmessa. Questo è un modo molto semplicistico di vedere le cose poichè affinchè la valutazione spettrofotometrica sia correttamente effettuata altri fattori devono essere presi in considerazione. La legge di Lambert Beer permette di calcolare correttamente la concentrazione molare di un campione, conoscendone l'assorbanza.
Formula della Legge di Lambert e Beer
I. 0 I La legge di Lambert e Beer A = &2 cl A = assorbanza alla lunghezza d'onda 2 &2 = coeff. di estinzione molare c = concentrazione molare I = lunghezza del cammino ottico (1 cm)
@ 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it TA1
Dosaggio Spettrofotometrico Diretto
Caratteristiche del Metodo Diretto
Metodo rapido e diretto di lettura del campione senza utilizzo di reagenti ed il campione può essere quindi riutilizzato.
Assorbimento di Amminoacidi
O HO OH HN- NH, Tryptophan Absorption OH NH2 HO Tryosine O OH HN- NH Histidine 260 280 300 320 wavelength (nm) Sfrutta la lettura dell'assorbimento mediante spettrofotometro. Gli amminoacidi triptofano, tirosina ed istidina hanno assorbimento con picco a 280nm. La composizione in amminoacidi delle proteine è variabile e la lettura può essere imprecisa. Infatti la quantità di proteine può essere facilmente sovrastimata o sottostimata in base alla percentuale relativa degli amminoacidi con alto contributo di assorbanza a 280nm
c 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it1
Interferenze e Formula di Calcolo
II DNA e l'RNA assorbono con un picco a 260nm quindi vi è una leggera sovrapposizione e il contributo degli acidi nucleici deve essere considerato e sottratto. Il metodo quindi seppur rapido e semplice ha lo svantaggio di avere scarsa precisione e specificità.
T Protein Absorption Nucleic Acid 240 260 280 300 320 wavelength (nm)
La formula applicata per determinare la concentrazione delle proteine nella soluzione in analisi è la seguente: mg proteine/ml = 1,55 * A280 -0,76 * A. 260
@ 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it1
Metodi Colorimetrici per Proteine
Principio dei Metodi Colorimetrici
I metodi colorimetrici prevedono l'utilizzo di reattivi in grado di formare complessi colorati dopo aver reagito con le proteine. Tali complessi conferiscono alle proteine un determinato specifico picco di assorbimento della luce ad una determinata lunghezza d'onda.
Principali Metodi Colorimetrici
- Metodo del Biureto
- Metodo di Lowry
- Metodo dell'acido bicinconinico
- Metodo di Bradford
@ 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it TA1
Il Metodo del Biureto
Reazione e Colorazione
Si effettua aggiungendo alla soluzione proteica una soluzione rameica in ambiente basico. La formazione di un complesso tetra-coordinato del rame con i legami peptidici conferisce una colorazione che va dall'azzurro al viola-porpora, con un picco di assorbimento a 540nm.
Schema della Reazione del Biureto
I 0 =C C= 0 H20 NH HN 1 1 R -CH HC -R I CH2+ 1 C=0 HN 1 1 NH H20 R -CH HC -R - 0 = C -
2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it TA1
Vantaggi del Metodo del Biureto
- Rapido e semplice.
- Deviazioni del colore meno frequenti rispetto al metodo di Lowry, assorbimento UV e metodi turbidimetrici.
- Poche sostanze di natura non proteica interferiscono con il dosaggio.
- Non dosa l'azoto da sorgenti non proteiche o non peptidiche.
Svantaggi del Metodo del Biureto
- Poco sensibile (almeno 2-4 mg di proteine per saggio).
- Alte concentrazioni di sali d'ammonio interferiscono con il dosaggio.
- Il colore può variare a seconda delle proteine (la gelatina dà una reazione rosa-porpora).
- La soluzione può essere opalescente a causa di alto contenuto di lipidi e carboidrati.
- Non è un metodo assoluto: necessaria una curva di taratura (ad esempio con BSA).
@ 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it TA1
Il Metodo di Lowry
Principio del Metodo di Lowry
Il metodo di Lowry si realizza combinando una prima reazione con il metodo del Biureto ad una seconda reazione di riduzione del reattivo fosfomolibdicofosfotungstico per i fenoli, il reattivo di Folin-Ciocalteau. Il reattivo di Folin reagisce con la tirosina e il triptofano delle proteine con un colore blu (750 nm) per la formazione di blu di tungsteno e blu di molibdeno grazie alla riduzione operata dal complesso rame- proteina.
Vantaggi del Metodo di Lowry
- Molto sensibile: 50 -100 volte più sensibile del Biureto; 10-20 volte più sensibile dell'assorbimento UV.
- Meno sensibile alla torbidità del campione.
- Più specifico di altri metodi.
- Semplice (1-1,5 ore per il dosaggio).
Svantaggi del Metodo di Lowry
- Il colore può variare a seconda della proteina maggiormente rispetto al Biureto.
- Il colore non è strettamente proporzionale alla concentrazione proteica.
- Diverse sostanze interferiscono (saccarosio, lipidi, fosfati, monosaccaridi).
- Alte concentrazioni di zuccheri riducenti, solfato d'ammonio, e composti sulfidrilici interferiscono con la reazione.
@ 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it1
Il Metodo dell'Acido Bicincroninico (BCA)
Meccanismo del Metodo BCA
Il metodo dell'acido bicinconinico sfrutta anche esso la reazione di riduzione di ioni rameici a rameosi in ambiente basico, mediata da proteine e peptidi. Viene poi aggiunto l'acido bicinconinico (BCA) e gli ioni rameosi reagiscono il BCA per formare complessi di colore viola-porpora costituiti da uno ione rameoso chelato da 2 molecole di BCA. Il colore viene misurato alla lunghezza d'onda di 562 nm, ed è lineare con la concentrazione proteica che va da microgrammi fino a circa 2 mg/ml. Contribuiscono al colore legami peptidici, cisteina, cistina, triptofano, tirosina.
Reazione del Complesso BCA
Protein + Cu2+ (biuret reaction) OH Cu+ + bicinchonic acid O N N Cu N N O o- O Purple Complex of Cu+ with BCA
@ 2007 - 2014 Università degli Studi eCampus - Via Isimbardi 10 - 22060 Novedrate (Co) - C.F. 90027520130 - Tel: 031.7942500 - Fax: 031.792631 - Mail: info@uniecampus.it