Interazioni molecolari, atomi, molecole e microbiota umano
Documento di Università sulle interazioni molecolari. Il Pdf esplora l'esperimento di Stanley Miller, la formazione di atomi e molecole, e il microbiota umano, fornendo definizioni e spiegazioni dettagliate per lo studio della Biologia.
Mostra di più63 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
INTERAZIONI MOLECOLARI
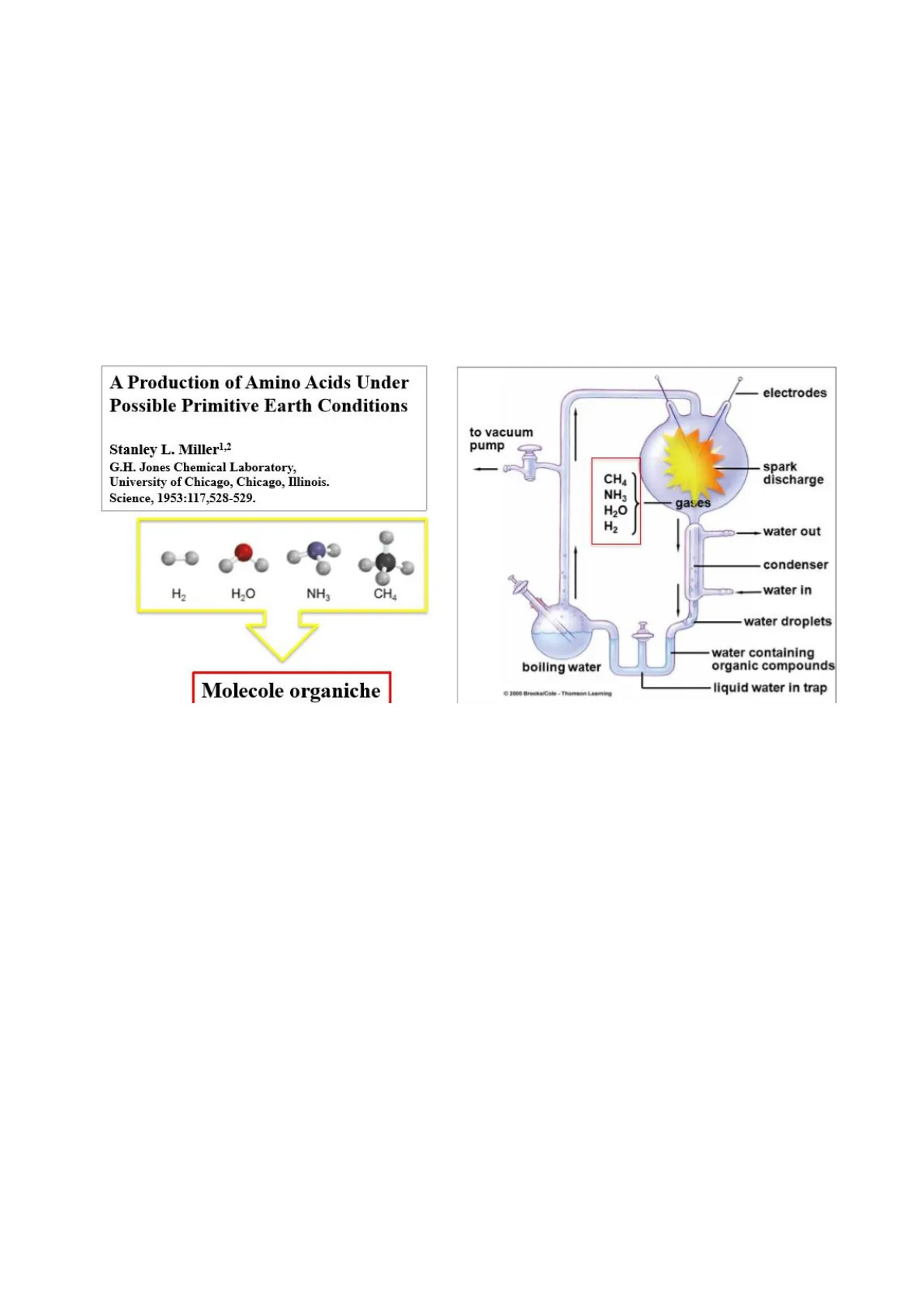
Stanley Miller, fu il primo scienziato, a capire in che modo, le prime molecole organiche vennero formate a partire da elementi inorganici. Egli ricreò, tramite un modello, l'ambiente terreno. All'interno dell'ampolla di questo modello, vi erano immessi gas (idrogeno, vapore acqueo, ammoniaca e metano) soggetti a continue scariche elettriche emesse da elettrodi. Ciò determinava la precipitazione dei gas in un condensatore, all'interno del quale veniva immessa acqua in un circuito che la immetteva e la espelleva. In questo modo all'acqua si legavano i costituenti organici dei gas. Il composto, seguendo la struttura del modello, entrava cosi successivamente in un bollitore, che permetteva ai gas di ritornare nell'ampolla originaria. Questo esperimento permise di capire come, dopo la condensazione dei gas, gli elementi interagivano tra di loro permettendo la formazione di amminoacidi.
A Production of Amino Acids Under Possible Primitive Earth Conditions Stanley L. Miller1,2 G.H. Jones Chemical Laboratory, University of Chicago, Chicago, Illinois. Science, 1953:117,528-529.
electrodes to vacuum pump spark discharge CH4 NH3 H2O H2 gases -water out condenser H2 H2O NH3 CH4 Molecole organiche liquid water in trap 2000 Brooks/Cole - Thomson Leaming water in water droplets boiling water water containing organic compounds
Molecole e Atomi
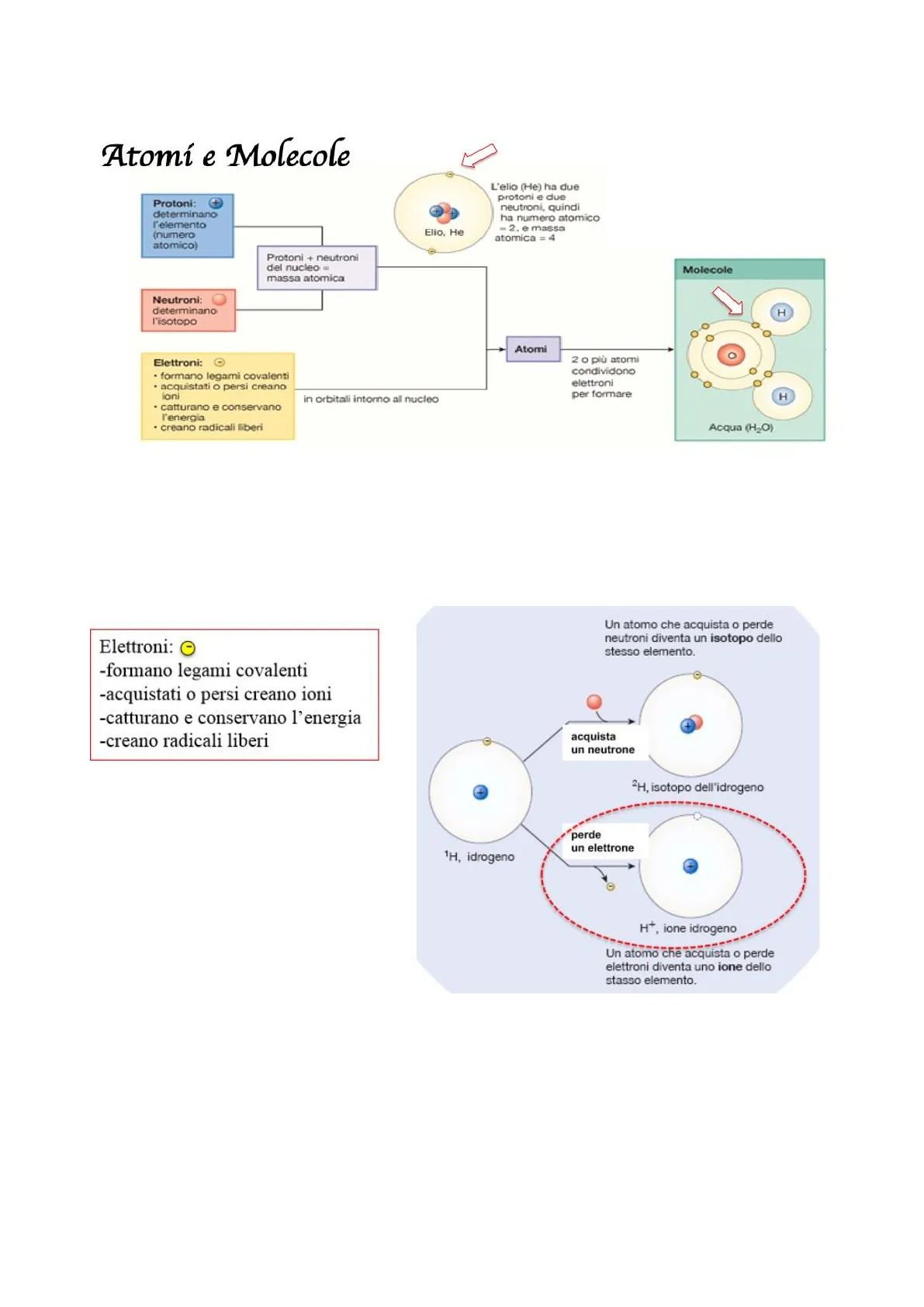
Per capire in che modo vengono a formarsi le molecole. Dobbiamo partire dai loro componenti più piccoli ed essenziali, vale a dire gli atomi. Essi rappresentano la parte più piccola di un elemento che mantiene le proprietà di quell'elemento. Gli atomi sono formati da protoni (+), neutroni ed elettroni (-). L'insieme dei primi due, nel nucleo, determina la massa atomica dell'atomo, mentre gli elettroni formano gli orbitali esterni, determinanti per capire in che modo funzionano i radicali liberi. Più atomi possono condividereelettroni per la formazione di molecole.
Atomi e Molecole
Protoni: determinano l'elemento (numero atomico) Elio, He L'elio (He) ha due protoni e due neutroni, quindi ha numero atomico = 2, e massa atomica = 4 Protoni + neutroni del nucleo = massa atomica Molecole Neutroni: determinano l'isotopo H Atomi Elettroni: · formano legami covalenti · acquistati o persi creano ioni in orbitali intorno al nucleo · catturano e conservano l'energia · creano radicali liberi Acqua (H2O)
Gli elettroni possono formare legami covalenti e non, e durante la creazione di questi legami, possono essere condivisi, persi o acquisiti elettroni generando energia. Scambiando elettroni, si possono formare atomi con elettroni spaiati (singoli). Essi rappresentano atomi iper-reattivi, in quanto, cercando di stabilizzare la propria formazione elettronica, tendono ad interagire con altri atomi. Ciò è alla base dello stress ossidativo.
Elettroni
- formano legami covalenti
- acquistati o persi creano ioni
- catturano e conservano l'energia
- creano radicali liberi
O acquista un neutrone 2H, isotopo dell'idrogeno perde un elettrone 1H, idrogeno H+, ione idrogeno Un atomo che acquista o perde elettroni diventa uno ione dello stasso elemento.
Legami Covalenti
Tra i legami possibili ritroviamo i legami covalenti. Essi sono legami molto forti che prevedono la condivisione degli elettroni. Essi richiedono una forte liberazione di energia per la loro rottura. Le molecole contenenti i legami covalenti sono di due tipi: polari e non polari. Quest'ultime rappresentano molecole la cui distribuzione degli elettroni è equa. Esse quindi non presentano né un polo carico positivamente né uno carico negativamente. Un esempio ne sono gli acidi grassi.
Un atomo che acquista o perde neutroni diventa un isotopo dello stesso elemento.
O 2 o più atomi condividono elettroni per formare HLe molecole polari, invece, rappresentano molecole la cui distribuzione degli elettroni permette la formazione di poli positivi e negativi. Esse sono molecole tendenzialmente solubili in acquia, quindi idrofili che, e la molecola d'acqua ne rappresenta proprio la tipologia più comune.
I legami covalenti si hanno quando gli atomi condividono elettroni. Questi legami richiedono molta energia per la loro rottura.
Molecole Non Polari
(a) Molecole non polari Le molecole non polari hanno una distribuzione eguale degli elettroni. Per esempio, molecole costituite prevalentemente da carbonio e idrogeno tendono a essere non polari. Acido grasso Idrogeno Carbonio
Molecole Polari
(b) Molecole polari Le molecole polari hanno regioni di carica parziale (8+ o 8-). L'esempio più importante di molecola polare è l'acqua. Polo negativo Molecola d'acqua 8- 8- 5+ 8+ Polo positivo
Legami Non Covalenti
I legami non covalenti sono di tre tipi. I principali sono i legami ionici, essi rappresentano legami deboli che si basano sulla cessione di un elettrone da parte di un atomo più piccolo attirato da un atomo con attrazione grande. più
Legami Ionici
(c) Legami ionici I legami ionici sono attrazioni elettrostatiche fra ioni. Un comune esempio è il cloruro di sodio. anione Catione + Na CI Na CI Atomo di sodio Atomo di cloro lone sodio (Na+) lone cloro (CI-)
I legami a idrogeno rappresentano legami deboli caratterizzati dalla semplice vicinanza degli atomi di idrogeno con atomi di ossigeno, azoto o fluoro, le forze di van der waals in vece rappresentano legami ancora più deboli che si formano sulla base della vicinanza tra atomi non specifici i cui elettroni si avvicinano fin quando non si respingono.
Gli elementi essenziali in natura sono rappresentati da ossigeno, idrogeno e carbonio che, nell'essere umano rappresentano il 90% della massa corporea. Esistono anche elementi secondari come magnesio, fosforo, zolfo, sodio, potassio, cloro.
H: D:H - HP H . H2OL'unione di atomi di diversa natura può portare alla formazione dei cosiddetti gruppi funzionali. Molto importanti in quanto essi rappresentano alcune caratteristiche di una molecola.
Gruppi Funzionali
Gruppo funzionale Nome Descrizione -OH ossidrilico - OH polare e solubile in acqua: tende a formare legami a H 0 U OH carbossilico -COOH acido debole: tende alla forma -COO perdendo uno ione H* H -N H amminico - NH2 base debole: tende alla forma NH3* acquistando uno ione H* H 1 -C=0 aldeidico - COH polare e solubile in acqua >c=0 chetonico =CO polare e solubile in acqua 0 -P-OH 1 OH fosfato - PO3H2 acido: tende alla forma PO32- perdendo due H*
I composti formati da carbonio, prendono il nome di composti o molecole organiche o biomolecole. Le biomolecole più importanti del nostro organismo sono rappresentate dai carboidrati, proteine, lipidi ed acidi nucleici. (ripetizione delle macromolecole di biochimica)
CELLULE E TESSUTI
Robert Hooke, nel 1665, riuscì per primo ad identificare le cellule tramite lo studio di un pezzo di sughero analizzato con l'ausilio di un microscopio rudimentale. Il nome cellula venne da lui coniato in quanto esse gli parvero morfologicamente simili alle cellette in cui le api inseriscono il miele. Teoria cellulare che poi fu approfondita e supportata da altri studiosi come Schleiden, Schwann e Virchow. Quest'ultimo definì il corpo umano come una città all'interno delle quali vi erano i cittadini, ovvero le cellule.
La Cellula Animale
La cellula animale è formata da un compartimento ben separato dal resto, la membrana cellulare. Essa racchiude il citoplasma, che a sua volta, è formato dal citosol (parte liquida), organelli membranosi di vario tipo, inclusioni lipidiche, di glicogeno e ribosomi e fibre proteiche. All'interno del citoplasma, inoltre, vi è il nucleo che contiene tutte le informazioni geniche delle cellula. La cosa importante da ricordare è che tutte le cellule di un organismo pluricellulare, contengono lo stesso apparato genetico. La differenziazione cellulareavviene, in quanto, solo una parte del patrimonio genico in possesso delle cellule viene espresso.
Cellula animale Membrana cellulare Nucleo Citoplasma Cellula adiposa: 50-150 u.m Citosol Organelli membranosi Inclusioni Fibre proteiche Oocita: 100 um · Mitocondrio . Gocce · Citoscheletro · Reticolo endoplasma- tico lipidiche · Centrioli · Granuli · Ciglia Eritrocita: 7.5 um di glicogeno · Flagelli · Apparato del Golgi · Ribosomi · Lisosomi · Perossisomi Leucocita 15 am Cellula del muscolo liscio: 15-200 jam di lunghezza Liquido extracellulare
La Membrana Cellulare
1)La membrana cellulare Essa è formata essenzialmente da fosfolipidi e sfingolipidi, insieme al colesterolo che ha l'importantissima funzione di regolare, in base alla temperatura, la vicinanza o la lontananza delle maglie fosfolipidiche in modo da preservare la selettività della membrana relativamente al passaggio di molecole nello spazio intra ed extra cellulare. Nella membrana sono presenti anche carboidrati e proteine. I Primi possono legarsi con i fosfolipidi di membrana, creano glicolipidi, e con le stesse proteine, formando glicoproteine. Queste molecole hanno tre funzioni essenziali: danno stabilità alla membrana, possono rappresentare dei segnali cellulari (sporgendo dalla membrana) per il riconoscimento cellulare degli antigeni, e di conseguenza regolano anche la risposta immunitaria. Oltre alla membrana cellulare, i fosfolipidi possono essere usati per creare membrane appartenenti anche ad altri organelli. Essi possono disporsi in una sorta di sfera membranosa nel formare le micelle (piccole molecole che servono all'assorbimenti dei lipidi), oppure possono formare un doppio strato fosfolipidico nella formazione della membrana dei Liposomi. Organelli al cui centro vi è del liquido utile al trasporto di ioni ed elementi nutrizionali. I liposomi, possono essere usati nella Farmaceutica dei fitoterapici. Quest'ultimi, infatti, rappresentano dei nutraceutici molto efficaci, ma a causa della loro bassa biodisponibilità, dovremmo assumerne dosi molto elevate. Per aumentarne l'assorbimento, i fitoterapici,spesso, vengono inseriti in formule farmaceutiche, all'interno delle maglie fosfolipidiche dei liposomi.
Struttura e Composizione della Membrana Cellulare
Membrana cellulare Struttura Composizione Funzione Le proteine periferiche possono essere rimosse senza compromettere l'integrità della membrana. Glicoproteina Le proteine transmembrana attraversano il doppio strato lipidico. Le teste fosfolipidiche sono rivolte verso i compartimenti acquosi intra- ed extracellulari Proteine ancorate ai lipidi Proteine periferiche Lo strato interno della membrana è formato da code lipidiche. Citoplasma Proteine del citoscheletro Molecole di colesterolo si inseriscono nello strato lipidico. Modello a mosaico fluido *. Singer and Nicolson, 1972
Il Citoscheletro
2)Il citoscheletro Esso è un'impalcatura tridimensionale situata al di sotto della membrana cellulare formata da filamenti intermedi, microfilamenti e microtubuli che danno tridimensionalità alla cellula. I filamenti intermedi sono formati da miosina, i microtubuli sono formati da spirali di tubulina, mente i microfilamenti sono formati da actina.
Filamento intermedio miosina tubulina 4 Microtubulo Le actina Microfilamenti
Un importantissimo concetto è relativo ad il trinomio "struttura-composizione-funzione". Ogni cellula, infatti in base alla propria struttura e composizione, possiede una funzione diversa. In questo esempio sono rappresentate le cellule a ciglio. Esse sono formate da 8 coppie di microtubuli posti circolarmente, con un