Tolleranza immunologica periferica e regolazione immunitaria, Università degli Studi di Palermo
Documento dall'Università degli Studi di Palermo su Tolleranza Immunologica Periferica e Regolazione Immunitaria. Il Pdf di Biologia, adatto per l'Università, esplora i meccanismi di tolleranza linfocitaria e la regolazione della risposta immunitaria, inclusi i ruoli di linfociti T e B, cellule dendritiche e segnali co-inibitori.
Mostra di più12 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Lezione e Argomento
Lezione nº2 del 13/10/2022 Sbobinatore: Molinari Anna Revisore: Modesto Lucia Docente: Ugel Stefano Argomento: tolleranza immunologica periferica e regolazione immunitaria
Tolleranza Immunologica Periferica e Regolazione Immunitaria
La lezione odierna verte su un argomento parzialmente trattato durante il corso di Immunologia (dove si era trattata la tolleranza centrale a livello timico), mentre dalla prossima lezione si inizierà la parte clinica. L'argomento della lezione, ovvero la tolleranza immunologica periferica, risulta essere un concetto fondamentale per poter comprendere l'ipersensibilità di primo tipo (allergie), l'autoimmunità e tutte le altre patologie a sfondo immunitario. Quando il sistema immunitario si genera, seppur sia presente a livello timico un sistema di selezione abbastanza preciso che determina l'eliminazione di TCR capaci di legare complessi MHC-peptide self (tramite selezione soprattutto negativa), un piccolo numero di questi viene rilasciato in circolo. Vi è dunque una porzione di linfociti T potenzialmente auto-reattivi (ovvero con un TCR potenzialmente specifico per un complesso MHC-peptide self) che sfuggono al controllo timico e che quindi vengono riversati a livello della periferia come linfociti naïve. Una frequenza di questi linfociti T auto-reattivi è presente in tutti i soggetti; il fatto che poi questi linfociti generino una patologia è legato alla frequenza con cui gli stessi verranno attivati in periferia. A livello periferico, ovvero nei linfonodi, nella milza e negli organi linfoidi secondari, esistono diverse cellule con attività immunoregolativa, cioè con capacità di bloccare la proliferazione o la funzionalità dei linfociti auto-reattivi, che altrimenti andrebbero a suscitare un attacco, e quindi un danno, a livello di determinati tessuti. Esistono quindi dei meccanismi di controllo: la tolleranza immunologica periferica e la regolazione immunitaria.
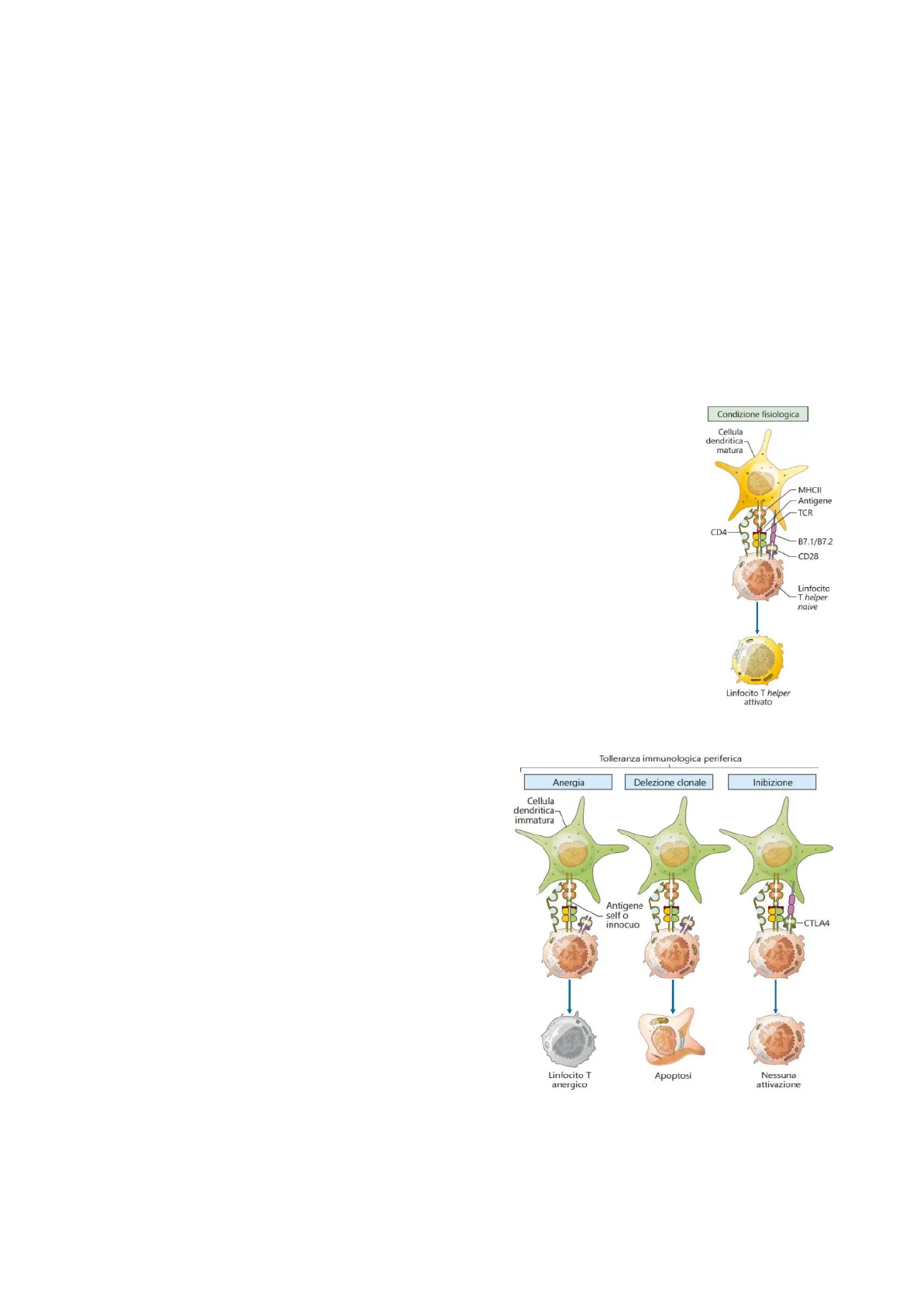
Condizione Fisiologica
Cellula dendritica- matura MHCII Antigene TCR CD4 B7.1/B7.2 CD28 Linfocito T helper naive Linfocito T helper attivato
Tolleranza Linfocitaria nella Periferia
Durante il corso di Immunologia si è visto come una APC (Antigen presenting cell) venisse riconosciuta da un linfocita non solo perché il TCR era complementare al complesso MHC-peptide non-self (primo segnale), ma anche perché la APC presentava in superficie molecole co-stimolatorie (come CD80 e CD86) volte ad attivare in maniera specifica il linfocita (secondo segnale per l'attivazione linfocitaria). Può accadere che al posto di un peptide non-self, venga riconosciuto un peptide self da parte di un linfocita auto-reattivo che non è stato eliminato a livello timico. Tuttavia, una volta avvenuto il riconoscimento, non avviene l'espansione clonale del linfocita; questo è dovuto ad una serie di meccanismi che coinvolgono molecole co-stimolatorie inibitorie, come PDL-1 (che ingaggiando un recettore inibitorio sul linfocita T ne blocca la funzione).
Tolleranza Immunologica Periferica: Anergia e Delezione Clonale
Anergia Delezione clonale Inibizione Cellula dendritica- immatura Antigene self o innocuo -CTLA4 Linfocito T anergico Apoptosi Nessuna attivazione
In generale, la presentazione di peptidi self in periferia può portare a due eventi distinti:
- La delezione clonale: quando una cellula dendritica ripresenta al linfocita auto-reattivo in periferia il complesso MHC-antigene self viene indotta l'apoptosi nei linfociti potenzialmente auto-reattivi che sono sfuggiti al controllo timico.
- La mancata interazione di CD28 con CD80/86 (dovuta all'intervento di PDL-1 che inibisce la funzione del linfocita) determina l'assenza del secondo segnale; il linfocita potenzialmente auto-reattivo potrà quindi persistere all'interno dell'organismo, ma sarà anergico (vivo, ma non funzionale).
Riassumendo quanto visto fino ad ora: errori di selezione linfocitaria a livello centrale possono essere riparati a livello della periferia tramite induzione di morte cellulare (delezione clonale) o di blocco funzionale (anergia) dei linfociti potenzialmente auto-reattivi. Se i meccanismi di questo braccio dell'immunologia con attività negativa non funzionassero in maniera adeguata, i linfociti auto-reattivi potrebbero potenzialmente espandersi ed attaccare in maniera precisa cellule presenti in determinati tessuti, generando quello che viene definito come attacco autoimmune, processo alla base delle patologie autoimmuni. (NB: si parla di antigeni self, ovvero derivanti da proteine endogene).
Regolazione della Risposta Linfocitaria in Periferia
Oltre all'induzione di una tolleranza immunologica periferica, è possibile anche l'induzione di una regolazione immunitaria. Si distinguono due tipi di regolazione immunitaria:
- RICD: morte indotta da attivazioni successive del linfocita auto-reattivo. Più volte il linfocita viene attivato, più questo diventa senescente (poco efficace nella sua proliferazione) fino a che le ripetute presentazioni dell'antigene indurranno la morte nel clone linfocitario. A determinare la morte del linfocita è la presenza del recettore di morte (FAS). Il FAS ligando viene riconosciuto dal recettore FAS localizzato sulla membrana del linfocita; questo riconoscimento induce l'uccisione per apoptosi del linfocita T potenzialmente auto-reattivo.
- La presentazione dell'antigene self può determinare l'espansione di popolazioni di cellule immunoregolatrici come i linfociti regolatori (Treg). A livello timico i Treg sono linfociti CD4+, ma hanno la capacità di esprimere un TCR specifico per complessi MHCII-antigene self. Una volta rilasciati in circolo i Treg possono venire espansi con lo scopo di limitare l'espansione di linfociti CD4+ o CD8+ che potrebbero danneggiare tessuti dell'organismo.
Regolazione Immunitaria: RICD e Soppressione
Regolazione immunitaria RICD Soppressione FASL - FAS TGFB IL10 CTLA4 Apoptosi Linfocito Treg
In questo caso quindi la presentazione di un antigene self può indurre una polarizzazione cellulare verso cellule con attività immunosoppressiva e l'espansione di popolazioni linfocitarie con attività immunoregolatrici, come i linfociti Treg. Un eventuale difetto in questo ramo di regolazione può causare uno sbilanciamento: se vengono a mancare i freni regolativi periferici i pochi cloni auto-reattivi presenti non vengono più bloccati in periferia determinando un aumento della condizione autoimmune.
Tolleranza Linfocitaria nella Periferia: Linfociti B e T
Per quanto riguarda i linfociti T che esprimono TCR potenzialmente auto-reattivi, essi vengono eliminati mediante delezione (selezione negativa) durante l'instaurarsi della tolleranza dei linfociti T a livello timico. Invece, durante la genesi di un linfocita B, se nel corso della ricombinazione avviene la formazione di un paratopo potenzialmente auto-reattivo c'è la possibilità di eseguire una modifica del BCR (editing recettoriale) tramite la ricombinazione del gene codificante la catena leggera 2, in modo da determinare una modifica nel paratopo tale per cui la nuova struttura non sarà più in grado di legare un epitopo self. Nel caso in cui, anche in seguito alla ricombinazione del gene per 2, venisse a generarsi un paratopo potenzialmente auto-reattivo, nella maggior parte dei casi il linfocita verrà eliminato. Tuttavia, errori di selezione di BCR durante il processo di tolleranza centrale nel midollo osseo possono portare al rilascio in circolo di linfociti B potenzialmente auto-reattivi. Molto spesso difetti dei linfociti B auto-reattivi svolgono un ruolo cruciale nell'insorgenza di patologie autoimmuni. Per esempio, il Lupus eritematoso sistemico è una patologia legata alla presenza di un linfocita B con un BCR specifico per proteine nucleari self. Analogamente difetti di TCR possono causare potenzialmente patologie autoimmuni. Il ricorrere del termine "potenzialmente" fa riferimento al fatto che gli individui che presentano un determinato aplotipo saranno più soggetti a sviluppare malattie autoimmuni. Per le patologie autoimmuni si parla di rischio relativo. Infatti, la componente di rischio di sviluppare la patologia che è determinata dalla condizione di polimorfismo dell'MHC, sarà sempre accompagnata da un'altra causa scatenante, determinata dal fattore ambientale (anche con un elevato rischio, se manca il fattore ambientale, la patologia non verrà sviluppata). Dunque, per quanto riguarda le patologie autoimmuni, ad oggi, non c'è un marcatore di malattia preciso (come invece possono essere considerate le mutazioni di p53 o KRAS nel contesto delle neoplasie), ma si ha a che fare con una percentuale di possibilità che il soggetto sviluppi la patologia. Ciò è dovuto al fatto che le cause scatenanti sono molteplici ed i fattori genetici sono attualmente riconosciuti solo per quanto riguarda il polimorfismo dell'MHC (alcuni polimorfismi dell'MHC sono fortemente predisponenti per lo sviluppo di una malattia autoimmune, in quanto quel determinato aplotipo potenzialmente avrà un'ansa che legherà maggiormente peptidi self, determinando la presentazione massiva di peptidi self).
Tolleranza Linfocitaria Periferica: Cellule Dendritiche
Le cellule che attivano la risposta T sono le cellule APC. Una tipologia di APC è rappresentata dalle cellule dendritiche immature, che possono indurre una tolleranza periferica dei linfociti T. La cellula dendritica matura dalla periferia migra (dopo aver captato l'antigene) verso il linfonodo. Questa migrazione è determinata dal fatto che la cellula monta in membrana i recettori chemochinici (per permettere l'attrazione verso il linfonodo), inoltre, durante il percorso dalla periferia al linfonodo, la cellula dendritica comincia ad esprimere le molecole co-stimolatorie CD80 e CD86. In assenza di queste due molecole, una volta arrivata al linfonodo, la cellula dendritica non sarebbe in grado di attivare in maniera efficace il linfocita T, poiché verrebbe a mancare il legame con CD28 presente sulla membrana del linfocita T. Tuttavia, una porzione importante di cellule dendritiche immature persiste nei tessuti periferici, sia linfoidi sia non linfoidi, e la loro funzione è quella di spegnere la risposta immunitaria. Questo aspetto va preso in considerazione, poiché nelle patologie autoimmuni il problema non è mai rappresentato esclusivamente dalla presenza del linfocita auto-reattivo, ma soprattutto dalla mancanza di cellule con attività inibitoria, che spengono questi linfociti. Infatti, in molte patologie difetti della funzionalità di Treg e delle cellule immunosoppressive sono molto importanti nel mantenere un'attivazione spropositata della risposta immunitaria. La APC presenta TOLL-like receptors e PRR (pattern recognition receptor), che le permettono di legare i PAMPs presenti in circolo, i quali, una volta legati vengono trasferiti all'interno del fagolisosoma, trasformati in peptidi e montati su MHC di II classe. Il complesso MHCII-peptide viene riconosciuto dal TCR del linfocita T determinando il primo segnale. A seguire avviene il secondo segnale quando CD28 lega CD80/CD86 ed infine si ha il rilascio di citochine, tra cui IL2, che permetterà la proliferazione dei linfociti B. Dopo l'attivazione completa del linfocita T, quest'ultimo monterà progressivamente in membrana i recettori CD69, CD25, CD40L ed infine il recettore CTLA-4. Nel caso in cui il linfocita incontri una cellula che non presenta le molecole costimolatorie (CD80 e CD86, che determinano l'induzione del secondo segnale) e che non favorisce il rilascio di citochine, la presentazione antigenica viene definita come tollerigenica, ovvero che non favorisce l'attivazione e la proliferazione del linfocita T, ma piuttosto la sua delezione (apoptosi) oppure anergia. In un linfocita attivato da un antigene self (tramite presentazione tollerigenica) possono quindi verificarsi due fenomeni:
- verrà indotta l'attivazione di proteine pro-apoptotiche. Infatti, la classica attivazione di fattori trascrizionali quali: NFKB, AP-1 e NFAT, che non viene potenziata dal legame CD40-CD40L, può favorire l'over