Immunologia: presentazione antigene tramite TCR e selezione clonale timica
Documento di Immunologia sulla presentazione dell'antigene tramite TCR e la selezione clonale timica. Il Pdf, utile per lo studio universitario di Biologia, approfondisce la struttura del TCR, le interazioni con MHC e la sinapsi immunologica, includendo dettagli su molecole accessorie come CD3, CD4 e CD8.
Mostra di più12 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Presentazione dell'antigene tramite TCR e selezione clonale timica
Prof. Adinolfi Una volta capiti gli anticorpi e gli ICR è più facile comprendere come funzioni il TCR, in quanto molti concetti sono simili.
IL TCR - T cell receptor è il recettore dei linfociti T che riconosce l'antigene, e ad ogni linfocita T corrisponde un TCR, che corrisponde ad una singola specificità antigienica. Il TCR resta espresso sulla superficie del linfocita T, e non è in grado di riconoscere da solo l'antigene (l'anticorpo si) e per fare ciò l'antigene deve essere inserito nel contesto del complesso MHC - complesso maggiore di istocompatibilità: il TCR si trova sulla membrana di un linfocita T, l'MHC e l'antigene si troveranno su una cellula, detta reagente al linfocita T, che entrerà in contratto con questo. Questa struttura formata dal contatto di queste cellule prende il nome di sinapsi immunologica.
Struttura del TCR
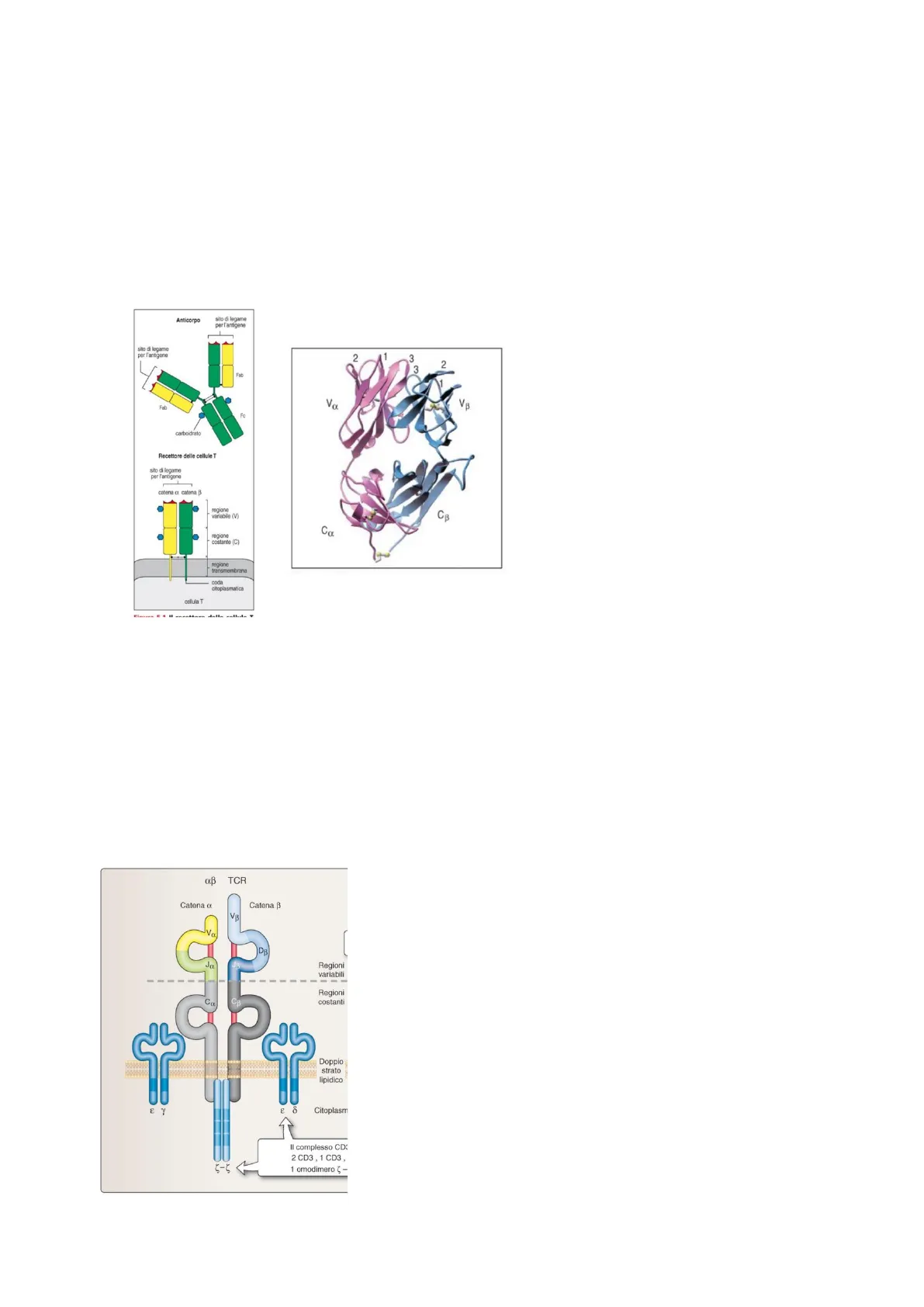
La docente spiega come molte strutture si possono ritrovare negli anticorpi, e durante la spiegazione delle componenti della TCR fa molti paragoni. Consiglia quindi di conoscere bene le immunoglobine. Il TCR è una proteina più piccola rispetto ad un immunoglobina, e ha una struttura proteica simile a quello del frammento FAB delle ImG. Il TCR presenta due domini dati da un ripiegamento simile a quello delle immunoglobine. Presentano una regione variabile, che ha la responsabilità di legare l'antigene e differisce da linfocita a linfocita, e una regione costante che si trova all'interno della membrana. È formato da due catene, alpha e beta, e ancora una volta presentano domini simili a quelle delle immunoglobine in quanto presentano lo stesso ripiegamento: dei beta foglietti che mantengono la struttura e una zona di loop. Il TCR non è in grado da solo di tradurre il segnale all'interno della cellula, nella prossima lezione vedremo quali molecole lo aiutano a fare ciò. Analizziamo ora meglio le due regioni; all'interno della regione variabile possiamo distinguere tre siti ipervariabili che corrispondono alle anse e ai loop dei beta foglietti delle immunoglobine Sito di legame per Assomiglia al frammento Fab di una IgG l'antigene (viste nelle lezioni precedenti). Fab In questa immagine si può vedere la struttura del TCR comparata a quella dell'immunoglobina. Per ogni TCR abbiamo una catena alpha e una catena beta con variable alpha, variable beta, di nuovo la specificità antigienica è data Va VB Ca CB cerniera + + Coda citoplasmatica Regione transmembrana Fc Struttura del dominio : Ig Non esistono diverse regioni costanti Non è secreto Gli eterodimeri sono legati da ponti disolfuro La coda intracellulare è molto corta il sito di legame per l'antigene è costituito da lle regioni Va e VB affiancate 1dall'insieme delle CDR, sia della catena alpha che della catena beta; quindi, con una stessa catena alpha e una diversa catena beta può variare la specificità antigenica. La regione costante coincide più o meno come struttura alla prima regione costante della immunoglobina che troviamo nel frammento FAB. Non esistono varie regioni costanti ma una sola, non è secreto, gli eterodimeri sono legati tra loro tramite vari ponti di solfuro e la coda intracellulare è molto corta. Il sito di legame per l'antigene è sempre costituito dalle regioni Valpha e Vbeta affiancate.
Confronto tra Anticorpo e Recettore delle cellule T
Anticorpo sito di legame per l'antigene sito di legame per l'antigene 2 1 3 2 3 Va VB Fab Fc carboidrato Recettore delle cellule T sito di legame per l'antigene catena cx catena B regione variabile (V) CB regione costante (C) Ca regione transmembrana coda citoplasmatica cellula T In questa immagine si possono notare le zone variabili in alto, Va e Vb, e le zone costanti in basso. Le CDR sono queste anse dove abbiamo la scritta 1-2-3 deputate al riconoscimento dell'antigene, che così come nelle immunoglobine, e che risultano particolarmente stabile alle temperature. A livello di dimensioni il TCR risulta più piccola rispetto alll'anticorpo. Una volta riconosciuto l'antigene questo media un'alterazione conformazionale della molecola che fa si che si attivino le molecole associate, responsabili della trasduzione del segnale. Queste sono molecole invarianti, le stesse per ciascun TCR; la più importante di queste molecole è sicuramente la CD3 - Cluster of differentiation 3 (CD3y, CD38 e CD38) e la proteina ( accessoria, che internalizza il segnale. Questo si trova tra il dominio trans-membrana e il dominio subito sotto la membrana cellulare del linfocita T, sia dei citotossici che i T helper. È prodotto a livello del RE dove si associa con il TCR.
Rappresentazione di CD3
aß TCR Catena o Catena ₿ VB DB Ja Regioni variabili Regioni costanti Ca Doppio strato lipidico Citoplasm Il complesso CD: 2 CD3 , 1 CD3 , 1 omodimero ( - Il CD3 può essere utilizzato per misurare il numero di linfociti T circolanti, per fare ciò si usa un marcatore. Il CD4 e CD8 sono molecole accessorie molto importanti, hanno lo scopo di associare il TCR all'interno del linfocita T. È importante notare come non tutti i linfociti esprimano CD4 o CD8; quelli che presentano CD4 sono i linfociti T helper, mentre quelli che presentano CD8 sono quelli citotossici. 2Interazione TCR MHC:
Mentre gli anticorpi sono in grado di legare direttamente l'antigene, gli antigeni che legano ed attivano il TCR devono essere presentati nel contesto del complesso MHC. Il complesso maggiore di istocompatibilità è così detto perché è il principale responsabile del rigetto dei trapianti. Nell'uomo il complesso MHC è anche noto come HLA (human leukocyte antigen) per il suo ruolo nel rigetto dei trapianti. Questi antigeni provengono dall'interno della cellula, processati dalla cellula che esprime MHC e presentati sulla membrana. L'MHC lega i peptidi antigienici, il linfocita T in grado di riconoscere l'antigene presentato si lega al complesso e attiva una risposta immunitaria. L'MHC pur non andando incontro a riarrangiamento somatico è presente con una varietà molto elevata di alleli nella popolazione, da individuo ad individuo cambia. Rimangano invariati dalla nascita alla morte, e si modificano rispetto all'ambiente e ai suoi patogeni. L'MHC prende i peptidi all'interno della cellula, li lega e li esprime sulla membrana plasmatica.
Classi di MHC
Esistono due classi di MHC che interagiscono con peptidi diversi: Le molecole MHC di classe I sono deputate alla presentazione di peptidi citoplasmatici (es. quelli derivanti da infezioni virali) ed interagiscono col TCR di linfociti T esprimenti la molecola co-stimolatoria CD8, che lega solo con MHC di classe I (T citotossici). Queste molecole di MCH classe I si trovano su tutte le cellule del nostro organismo. Lega tutti i peptidi all'interno del reticolo endoplasmico, e li esprime sulla membrana plasmatica. Le molecole MHC di classe II sono deputate alla presentazione di peptidi derivanti dalla degradazione degli antigeni in vescicole intracellulari delle APC (antigen presenting cells, che sono le cellule dendritiche, i macrofagi e i linfociti B), all'interno del fagosoma, ed interagiscono col TCR di linfociti T esprimenti la molecola co-stimolatoria CD4 (T helper). Gli antigeni esposti da MHC di classe II sono processatti all'interno del fagosoma delle APC e sono presubilmente di natura patogena.
Ruolo delle cellule T
Le cellule T svolgono il loro ruolo stabilendo un contatto e inducendo modificazioni in altri tipi di cellule Cellula T Altra cellula Contatto cellulare Altra cellula alterata 33 3 celuia T CD8 celula infettata da virus celula infetata da virus celula infettata da virus morta ceochina V4 + cellula T CD4 citochine macrofago macrotago macrofago attivato otochine 9 g anticorpi cellula T CD4 plasmacellula do colule B colula B In quest'immagine si vedono le interazioni tra linfociti e il complesso MCH: nella prima riga si vede la cellula T che induce la cellula infetta in apoptosi. Nella seconda riga si vede il macrofago che si attiva a seguito di interazione con CD4 il quale inizia a produrre una serie di citochine, come l'interferone 4 che attiva la fagocitosi del macrofago. 3Molecola MHC di classe ! Molecola MHC di classe Il soico di legame del peptide solco di legame del peptide B. Bz Bz-microglobulina solco di legame del peptide solco di legame del peptide B1 5 (B2-microglobulina B2 L'interazione tra CD4 e linfocita B è molto specifica, poiché il linfocita B presenta all'interno del MHC di classe II lo stesso antigene che viene riconosciuto dal suo anticorpo. Questo perché nel momento che il linfocita B lega l'antigene, il complesso antigene- anticorpo viene internalizzato e l'antigene viene degradato nel fagolisosoma. L'interazione inoltre ha un effetto duplice, il linfocita T produce citochine che portano la cellula B a diventare plasmacellula, che poi produrrà anticorpi. L'MHC di classe I è fondamentale per il contrasto tumorale, sono stati infatti sviluppati da patogeni e cellule cancerogene meccanismi per contrastarlo.
Interazione CD8 e CD4 con MHC
CD8 lega il dominio czy della molecola MHC di classe | CD4 lega il dominio B2 della molecola MHC di classe II cellula bersaglio cellula che presenta l'antigene B2-microglobulina- B α B CD8 B2 CD4 B antigene- recettore della cellula T B cellula T CD8 cellula T CD4 Interazione CD8 e CD4 con MCH: Il CD8 interagisce con la subunità Alpha3 del MCH di classe I. Questo è formato da tre subunità: -Alpha-1, Alpha-2: zona di riconoscimento del peptide; -Alpha-3: ancorato alla membrana plasmatica, che si aggrega alla B2- microglobulina. Il CD4, invece, interagisce con la subunità Beta-2 del MHC di classe II che presenta una struttura diversa: -Alpha-1, Beta-1: sono le zone di legame al peptide; -Alpha-2, Beta-2: interagiscono con la membrana. 4Presentazione dell'antigene attraverso MHC-1:
Tutte le proteine presenti nel citosol, quando devono essere degradate, vengono mandate nel proteasoma grazie al legame con l'ubiquitina. I peptidi generati dall'ubiquinazione vengono trasportati nel RE grazie alla proteina TAP - transporter associated with antigen processing. Presentazione dell'antigene attraverso MHC-I Degradazione nel proteasoma le proteine non self come tutte le altre proteine citoplasmatiche sono degradate di continuo da un complesso proteolitico detto proteasoma La TAP è costituita da due molecole TAP1 e TAP2, entrambi trasportatori selettivi di peptidi dalle Legame all'ubiquitina dimensioni variabili dagli 8 ai 15 amminoacidi. Nel RE gli antigeni peptidici citoplasmatici sono legati dalle molecole MHCI. Fondamentale è il fatto che i peptidi devono entrare nel RE per essere caricati sull'MHCI.
Ingresso degli antigeni esogeni
Ingresso degli antigeni esogeni Ingresso mediato dal BCR Fagocitosi Fagocitosi mediata dai Recettori per il complemento Pinocitosi Fagocitosi mediata dal recettore per Fc Di seguito vediamo come gli antigeni esogeni possono entrare nella cellula: tramite fagocitosi, pinocitosi ... maturazione dell' MHC classe II e catena invariante Nel reticolo endoplasmico CLIP li chain L'antigene, tramite queste varie vie, entra negli endosomi (vescicole intracellulari), che si fondono all'interno della cellula con i lisosomi. Quest'ultimi libereranno catepsine B, D e le proteasi L attivate dal pH acido, in grado di tagliare le proteine, generando peptidi da 10-30 aa. L' MHCII nel reticolo endoplasmico non interagisce con E' necessario prevenire il la catena invariante stabilizza I'MHCII formando un complesso proteico che blocca il legame di peptidi all' MHCII nel reticolo legame di proteine self neosintetizzate all'MHCII qualsiasi peptide, in quanto è legato a una proteina (la catena invariante) che blocca il sito di interazione. Questa catena invariante è legata alla CLIP che si trova nel sito di legame in viola nell'immagine. Questo è necessario per prevenire il legame di proteine self neosintetizzate. Gli endosomi che portano MHCII si fondono con il fago-lisosoma e qui viene degradata la catena invariante, ma non la CLIP. La rimozione di quest'ultima è mediata da un processo catalitico, che è lo stesso processo che favorisce il legame di peptidi specifici all'interno del sito variabile del MCHII. 5