Enzimi: caratteristiche, azione catalitica e cinetica enzimatica
Documento sugli enzimi, la loro azione catalitica e i meccanismi di interazione con i substrati. Il Pdf di Biologia, adatto per l'Università, descrive i modelli di legame enzima-substrato, i principi della cinetica enzimatica e i tipi di inibizione enzimatica.
Mostra di più13 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Principali caratteristiche degli enzimi
Gli enzimi:
- aumentano la velocità di reazione
- non modificano l'equilibrio della reazione
- presentano specificità di reazione: ogni enzima lega uno o più specifici substrati trasformandolo/i in prodotto/i
- richiedono condizioni di reazione blande: in effetti gli enzimi funzionano a PH fisiologico e alla temperatura corporea
- sono soggetti a regolazione: vi sono molecole che possono agire da attivatori o inibitori nei confronti dell'enzima stesso
- l'integrità strutturale degli enzimi è necessaria per la funzione catalitica: quindi la struttura tridimensionale dell'enzima si deve mantenere integra.
Enzimi come proteine coniugate
Gli enzimi possono essere proteine coniugate. In questo caso la parte non amminoacidica è detta "co fattore".
Apoenzima: solo parte amminoacidica (senza il cofattore) Oloenzima: complesso enzima - cofattore
I cofattori possono essere metalli oppure specifiche molecole organiche. In quest'ultimo caso prendono il nome di coenzimi.
Interazione enzima-substrato
Considerando un generico enzima e un generico substrato Il substrato si lega ad una regione particolare dell'enzima che è il sito attivo (o "sito catalitico") dell'enzima. Il substrato reagisce solo con il sito attivo e si forma il complesso enzima - substrato.
+ sito attivo o sito catalitico enzima substrato complesso enzima-substrato E +S = ES
In realtà il complesso enzima - substrato può, in alcuni casi, tornare a dare singolarmente enzima e substrato. Ciò è però difficile che accada. Quando il substrato si trova nel sito catalitico viene trasformato in prodotto. Questo viene poi rilasciato e l'enzima ritorna libero per poter legare una nuova molecola di substrato e formare un nuovo prodotto. Infatti l'enzima "non si consuma" nella reazione.Stato di Transizione (#)
Energia libera e coordinata di reazione
Energia libera, G AG* 'S->P AGp _>S S JAG10 Stato basale P Stato basale Coordinata di Reazione
Il grafico descrive l'andamento di una reazione chimica da un punto di vista energetico In questo grafico non è presente l'enzima Affinché il substrato si trasformi in prodotto è necessario fornire energia al sistema, ossia energia di attivazione. Quando viene fornita la massima energia ci si trova nello stato di transizione. Allo stato di transizione non si parla ne di substrato ne di prodotto ma di un qualcosa di intermedio tra i due.
Ruolo dell'enzima nell'energia di attivazione
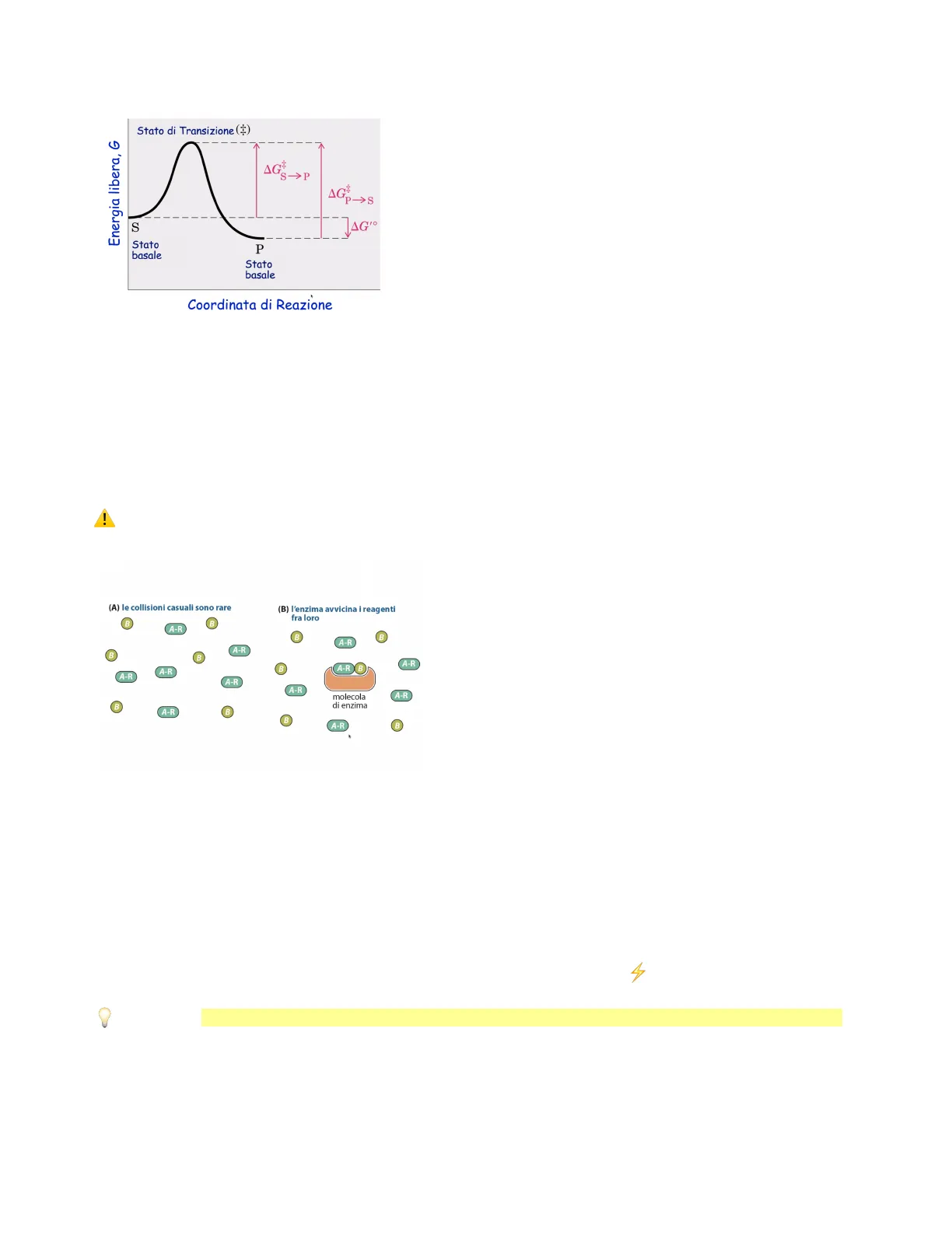
Domanda d'esame -. (A) le collisioni casuali sono rare B A-R (B) l'enzima avvicina i reagenti fra loro B R A-R A-R B B A-R A-F A-R A-R A-F B A-R B B 4-R B
L'energia che deve essere fornita è sempre la stessa L'enzima, quando presente, permette di fornire la stessa energia e facilita l'unione tra le due molecole di substrato. In effetti:
- quando non è presente l'enzima le collisioni casuali tra i substrati sono rare, tant'è che è necessario fornire parecchia energia affinché i substrati collidano tra loro.
- quando è presente l'enzima le molecole possono invece raggiungere il sito catalitico (con una quantità di energia + bassa rispetto al caso precedente), e quindi avvicinarsi tra di loro interagendo. La presenza dell'enzima permette dunque una sorta di "risparmio di energia ”
Definizione: Gli enzimi accelerano le reazioni avvicinando e orientando in modo corretto i gruppi reagenti A-R B A-R B molecola di enzima
Modelli di formazione del complesso enzima-substrato
Il complesso enzima - substrato si può formare secondo due modalità principali:
- modello - serratura
- modello dell'adattamento indotto
Modello chiave-serratura
Modello chiave-serratura ame Substrato + 1 Sito attivo 2 3 Enzima 2 Complesso 3 enzima- substrato
Nel modello chiave-serratura, la forma del substrato e la conformazione del sito attivo sono rigidamente complementari e non subiscono alcun cambiamento conformazionale
Nel modello chiave - serratura il substrato è perfettamente complementare alla struttura del sito catalitico
Modello dell'adattamento indotto
Modello dell'adattamento indotto Enzima Complesso 3 enzima-substrato b) a)
Nel modello dell'adattamento indotto, l'enzima subisce una transizione conformazionale legandosi al substrato. La forma del sito attivo diventa complementare alla forma del substrato soltanto dopo che il substrato si è legato all'enzima
Nel modello dell'adattamento indotto invece, sempre da un punto di vista strutturale, il substrato non è complementare al sito catalitico. Inoltre quando il substrato si avvicina al sito catalitico nell'enzima avviene un cambiamento conformazionale che porta il sito catalitico ad essere completamentare al substrato
Cinetica enzimatica
Per cinetica enzimatica si intende
- lo studio della velocità di una reazione enzimatica
- lo studio dell'influenza dei parametri sperimentali sulla velocità della reazione enzimatica
In quest'ultimo caso variando alcuni parametri (come es. pH, temperatura, ecc) varia anche la velocità di reazione.
cofattore E + S ES > E + P
La velocità di una reazione enzimatica può essere determinata:
- valutando la velocità di scomparsa del substrato
- osservando la velocità di comparsa del prodotto
- osservando, per alcune reazioni, la velocità di trasformazione del cofattore
Substrato 1 3!
Grafico di Michaelis - Menten
Domanda d'esame: cosa è il grafico di Michaelis - Menten?
Vmax Velocità iniziale, Vo 5 Vmax Km Concentrazione del substrato, [S] (mM) asse x: concentrazione del substrato asse y: velocità
Questo grafico, riguardante la cinetica enzimatica, descrive il comportamento di un enzima all'aumentare della concentrazione del substrato, e quindi ci dice come varia la velocità al variare della concentrazione del substrato. Il grafico si ottiene mantenendo costante la concentrazione dell'enzima Es. supponiamo di lavorare con una quantità costante di enzima (6 molecole) Se aumenta il numero di substrati e quindi di complessi enzima - substrato aumenta anche la velocità di reazione Quindi vi è una proporzionalità diretta tra l'aumento dei complessi enzima - substrato e l'aumento della velocità di reazione. Quindi mantenendo costante la concentrazione degli enzimi e aumentando la conc del substrato come varia la velocità? Se in seguito aggiungo 8 molecole di substrato, e ho ancora 6 molecole di enzima, avrò due molecole di substrato senza enzima. Ciò vuol dire che l'enzima è completamente saturato, e quindi anche se aggiungo continuamente substrato la velocità non aumenta più in quanto non ci sono più enzimi liberi. In effetti quando vengono occupate tutte le molecole di enzima si raggiunge la max velocità Quando invece vengono occupate solo la metà delle molecole enzimatiche si ottiene una velocità che è la metà di quella max raggiungibile.
La Km
La Km è
- la concentrazione di substrato a cui corrisponde 1/2 (metà) della velocità max
- la concentrazione di substrato in corrispondenza della quale metà dei siti catalitici dell'enzima sono occupati
Tutto ciò vale solo quando la concentrazione dell'enzima rimane costante !! Il grafico rappresenta tra l'altro un iperbole.
- Nel primo tratto dell'iperbole vi è un andamento rettilineo ed esiste una proporzionalità diretta tra concentrazione e velocità.
- Nel secondo tratto all'aumentare della concentrazione aumenta sempre la velocità ma non si parla di proporzionalità diretta.
- Nell'ultimo tratto invece indipendentemente dalla concentrazione la velocità non cambia più, in quanto tutti i siti catalitici dell'enzima sono occupati. Si è raggiunta dunque la max velocità per quella specifica concentrazione di enzima.
Inibitori enzimatici
Inibitori enzimatici (piccole molecole o ioni) Gli inibitori possono essere piccole molecole o ioni Gli inibitori possono essere irreversibili, ossia che si legano covalentemente all'enzima, o reversibili quando formano legami deboli con l'enzima. Indipendentemente da ciò si otterrà sempre la formazione di un complesso enzima - inibitore (E-I).
Inibitori reversibili
Inbitori reversibili Tra gli inibitori di tipo reversibile vi è
- inibizione competitiva: quando l'inibitore e il substrato competono per il sito catalitico dell'enzima. In questo tipo di inibizione cambia il valore della Km ma non cambia quello della Vmax.
- inibizione non competitiva: inibitore e substrato si legano su siti differenti dell'enzima. In questo tipo di inibizione la Km rimane costante, mentre varia il valore della Vmax.
- inibizione incompetitiva: in questo caso l'inibitore si lega soltanto al complesso enzima - substrato, e cambiano sia il valore della Km sia quello della Vmax.
Inibizione competitiva
Inibizione competitiva (! domanda esame) Reazione enzimatica classica in assenza di inibitore E+SES ->E+P + I 1 S EI
In presenza di un inibitore competitivo l'enzima può reagire e legare o il substrato o l'inibitore. Entrambi si dirigono ovviamente verso il sito catalitico. Se nel sito catalitico entra il substrato non può entrare l'inibitore e viceversa. Quindi o entra uno o entra l'altro! Se nel sito catalitico entra l'inibitore si forma il complesso enzima - inibitore, il quale blocca l'azione dell'enzima stesso. Pertanto le due molecole (substrato e inibitore) competono perché sono strutturalmente simili.
V. Vmax + 1/2 V max -- 0 4 [S] Km Km app Rappresentazione grafica in presenza e in assenza dell'inibitore competitivo Curva rossa: presenza dell'inibitore competitivo Curva azzurra: assenza dell'inibitore competitivo
I due grafici si ottengono mantenendo costante la conc dell'enzima Le due concentrazioni (in assenza e presenza di inibitori) devono essere le stesse, pertanto ci sarà lo stesso numero di molecole enzimatiche.Per ottenere la curva rossa bisogna scegliere una certa conc di inibitore, la quale rimane costante per tutta la curva, pertanto il numero di molecole di inibitore non cambia. Le due curve raggiungono lo stesso valore di Vmax Quindi quando la conc. di substrato è molto elevata si raggiunge lo stesso valore di Vmax (sia in presenza che in assenza di inibitore). Ciò vuol dire che tutte le molecole di enzima sono occupate soltanto dal substrato, anche in presenza di inibitore. Se la Vmax è la stessa anche 1/2 della Vmax sarà la stessa sia in assenza sia in presenza dell'inibitore. A cambiare è il valore della Km, in quanto in presenza di inibitore si parla di Km apparente. Questo cosa significa? es. se io ho 6 molecole di enzima e 10 di substrato avrò una conc. di substrato molto elevata. Questo vuol dire che tutte le molecole enzimatiche potranno legare il substrato e quindi verrà raggiunta la Vmax. Se supponiamo però di avere in tutto ciò anche 2 molecole di inibitore, ecco che esse, dato che sono in minoranza, non riusciranno in ogni caso a "predominare" sulle molecole di substrato, le quali si legheranno a tutti i siti catalitici a disposizione sugli enzimi saturandoli. Inoltre l'inibitore non possiede la stessa affinità a legarsi al sito catalitico dell'enzima come la possiedono i substrati. se invece ho 6 molecole di enzima, 10 di substrato e 30 di inibitore accade che le molecole di inibitore sono in eccesso rispetto a quelle del substrato e quindi "predomineranno" su di esse e riusciranno ad entrare nel sito catalitico dell'enzima. Abbiamo detto che 1/2 della Vmax sarà la stessa sia in assenza sia in presenza dell'inibitore.
- consideriamo la situazione in assenza di inibitore vi sono 6 molecole di enzima e 3 di substrato, pertanto al valore di 1/2 della Vmax le 3 molecole di substrato occuperanno metà dei siti catalitici.
- consideriamo la situazione in presenza di inibitore vi sono 6 molecole di enzima, 3 di substrato e 2 di inibitore. In questo caso la conc. tra substrato e inibitore è quasi la stessa, quindi per l'inibitore è + facile competere con il substrato per entrare nel sito catalitico. Quindi avviene la reale competizione substrato - inibitore, in seguito alla quale possiamo avere (per esempio) 2 molecole di enzima occupate dal substrato e 1 occupata dall'inibitore. Se accade questo non avremo più 1/2 della Vmax ma la velocità sarà + bassa Pertanto se vogliamo far occupare i 3 siti catalitici solo dal substrato, quando sono presenti gli inibitori, devo per forza aumentare la conc. di substrato. Dovrò pertanto lavorare con magari 5 molecole di substrato (invece delle 3 originarie) e ciò permetterà a queste ultime di occupare la metà dei siti catalitici e di raggiungere quindi 1/2 della Vmax. Quindi la Km apparente si ha soltanto in presenza dell'inibitore e corrisponde alla conc. di substrato che deve essere aumentata affinché si possa raggiungere 1/2 della Vmax occupando soltanto la metà dei siti catalitici.
Domanda: se lascio la stessa conc. di enzima e aumento il numero delle molecole di inibitore si avrà un altro valore di Km apparente? Si, perché bisogna trovare una nuova conc di substrato per "spiazzare" l'inibitore e occupare la metà dei siti catalitici per raggiungere 1/2 della Vmax.