La Cinetica Enzimatica: misurazione e fattori che influenzano l'attività
Slide sulla Cinetica Enzimatica, che esplora la misurazione della velocità delle reazioni catalizzate dagli enzimi. Il Pdf analizza i fattori che influenzano l'attività enzimatica, come pH, temperatura e concentrazione del substrato, ed è adatto per lo studio universitario di Biologia.
Mostra di più19 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
La Cinetica Enzimatica
La cinetica enzimatica si occupa della misura della velocità delle reazioni catalizzate dagli enzimi e di come questa velocità possa essere influenzata da alcuni elementi. Innanzitutto, come si studia o si può studiare la velocità di una reazione catalizzatore da un enzima? Per studiare la velocità, in primo luogo, bisogna mettersi nelle condizioni affinché quella reazione avvenga. La prima condizione necessaria è avere una miscela nella quale la reazione enzimatica possa avvenire. Questa miscela dovrà avere delle caratteristiche: dovrà essere una miscela in cui non abbiano delle variazioni di pH, quindi useremo un sistema tampone (un sistema che tampona le possibili variazioni di pH), garantendo così che l'enzima che stiamo studiando si trovi sempre al pH ottimale affinché possa catalizzare la reazione. È chiaro che in questa miscela in cui vogliamo far avvenire la reazione, l'enzima dovrà essere nella sua conformazione nativa. Abbiamo detto ripetutamente che la perdita della conformazione nativa e, quindi, la denaturazione dell'enzima, determina la perdita di attività dell'enzima stesso. Inoltre l'enzima, per catalizzare la reazione, può avere la necessità di altre sostanze (possono essere dei cationi), come nel caso delle esochinasi in cui se volessimo osservare la velocità della reazione catalizzata dovremmo aggiungere del magnesio, perché il magnesio è importante nella stabilizzazione delle cariche negative dell'ADP, per cui dovremo aggiungere dell'ATP. (Non si capisce bene ciò che dice).
Quindi bisogna, se vogliamo misurare la velocità di una reazione, dobbiamo metterci nelle condizioni o mettere l'enzima nelle condizioni in cui possa operare meglio, quindi nelle condizioni ideali. Stabilite le condizioni ottimali, che cambiano da enzima ad enzima per cui ogni enzima esprime la sua attività catalitica, dovremmo trovare un modo di osservare effettivamente il procedere della reazione.Potremmo valutare, come descritto dal grafico, l'aumento della concentrazione del prodotto nel tempo della reazione oppure la diminuzione della concentrazione del substrato/reagente nel tempo. Questi sono due approcci utili per seguire, quindi, l'andamento di una reazione catalizzata da un enzima.
Misurazione della Velocità di Reazione con Deidrogenasi
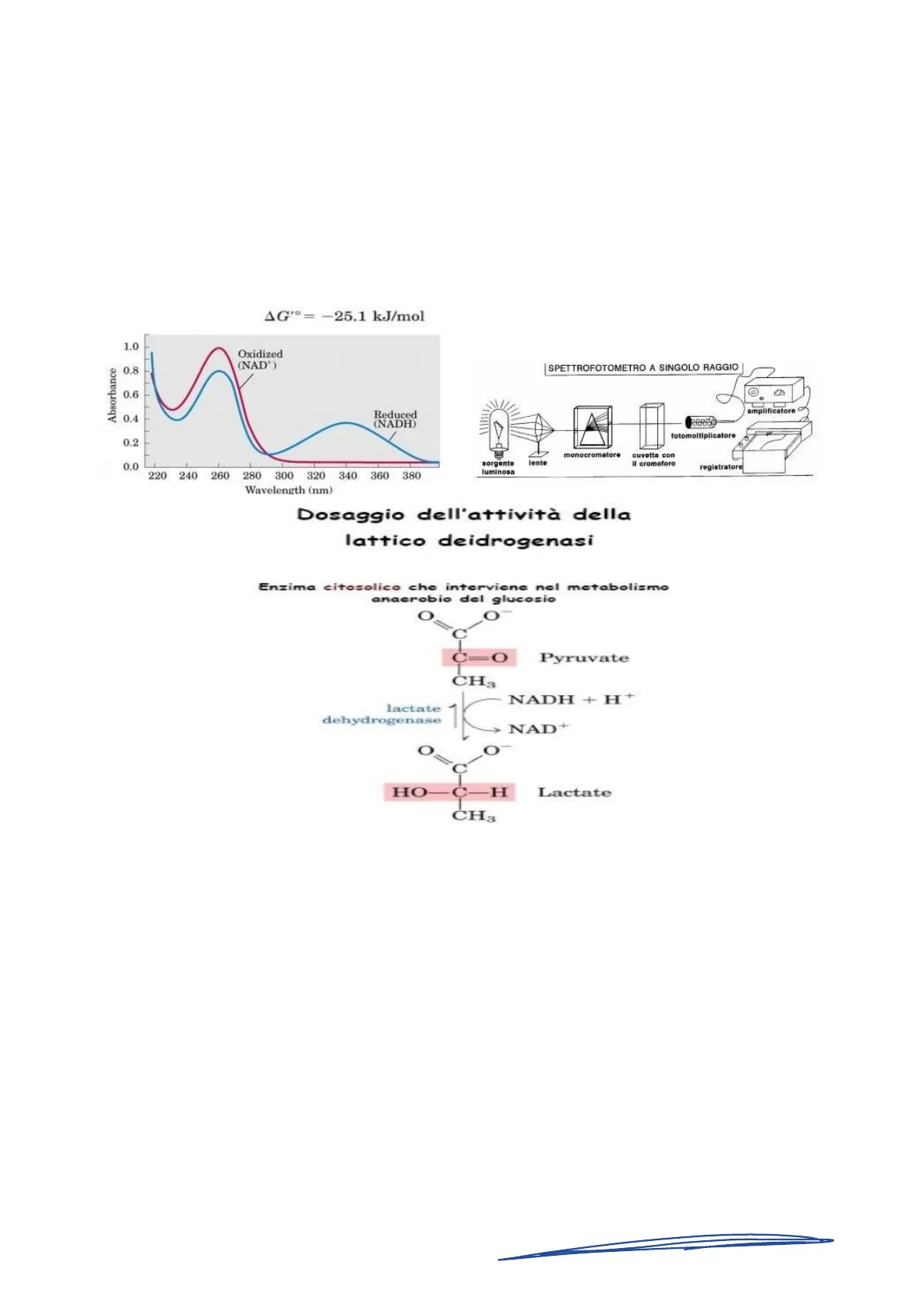
Ora, passando al concreto, immaginiamo di voler misurare la velocità di reazione catalizzata da un tipo di deidrogenasi. Questo enzima ci è già noto, abbiamo parlato della lattico deidrogenasi come esempio di isoenzima. La lattico deidrogenasi può catalizzare la reazione in cui il piruvato viene convertito in lattato, anzi il piruvato viene ridotto a lattato, mentre il NADH viene ossidato a NAD+. Se noi volessimo misurare la velocità di questa reazione potremmo seguire la concentrazione del prodotto (il lattato) o la diminuzione della concentrazione di piruvato. Siccome l'approccio sperimentale per fare una valutazione di questo tipo è generalmente spettrofotometrico, noi possiamo seguire una molecola che in realtà presenta un assorbimento a una specifica lunghezza d'onda. In questo caso, in realtà, noi non possiamo seguire né il piruvato né il lattato, però questa reazione prevede l'ossidazione del NADH. Questo presenta un caratteristico picco di assorbimento a 340nm. Il NADH, la forma ridotta, nel momento in cui passa nella sua forma ossidata NAD+, quel picco di assorbimento non c'è più. Pertanto se noi volessimo analizzare la velocità di reazione catalizzata dalla lattico deidrogenasi, potremmo seguire come cambia lo stato di riduzione del NADH. Man mano che la reazione procede, il NADH viene ossidato, il che vuol dire che l'assorbimento 340nm diminuisce. Nel grafico, la curva rossa (dello spettro di assorbimento) è il NAD+ non presenta il picco di assorbimento. La valutazione dell'assorbimento dello spettro fotometrico ad una lunghezza d'onda a 340nm ci consente di discriminare tra la presenza del NADHe del NAD+. Se abbiamo un assorbimento a 340nm vuol dire che è presente il NADH, ma se quell'assorbimento poi scompare nel tempo, vuol dire che il NADH si sta ossidando. Quindi in questo caso, se volessimo seguire la velocità della reazione catalizzata da lattico deidrogenasi, visto che il NADH partecipa a questa reazione che per ogni molecola di piruvato viene ridotto a lattato e viene ossidata una molecola di NADH, per seguire questa reazione potremmo spettrofotometricamente seguire l'ossidazione del NADH a NAD+ e, quindi, vedere la scomparsa dell'assorbimento a 340nm.
AG"= - 25.1 KJ/mol 1.0 Oxidized (NAD*) 0.8 Absorbance 0.6 e amplificatore 0.4 Reduced (NADH) 0.2 0.0 220 240 260 280 300 320 340 360 380 Wavelength (nm)
Dosaggio dell'attività della lattico deidrogenasi
Enzima citosolico che interviene nel metabolismo anacrobio del glucosio 0 O C C=0 Pyruvate CH3 NADH + H+ lactate dehydrogenase > NAD+ 0 O HO-C-H Lactate CH3
Spettrofotometro a Singolo Raggio
monocromatore lente cuvetta con il cromoforo sorgente luminosa registratore fotomoltiplicatore Nell'immagine vi è rappresentato uno spettrofotometro che consente di seguire nel tempo l'assorbimento a una specifica lunghezza d'onda. Se noi volessimo seguire la presenza del NADH allora sceglieremmo una lunghezza d'onda di 340nm perché quella è la specifica lunghezza d'onda a cui presenta il picco di assorbimento. Che cosa noteremo? Come abbiamo detto ci dobbiamo mettere nelle condizioni che consentano all'enzima, in questo caso la lattico deidrogenasi di funzionare al meglio, quindi useremo una miscela di reazione che avrà quelle caratteristiche già dette: sistema tampone che assicuri un determinato pH, una temperatura ottimale a cui opera l'enzima. Questa miscela verrà posizionata in questo elemento dello spettrometro che rappresenta la "cuvetta", insieme a tutto quello che serve per far avvenire la reazione enzimatica. Questa miscela presente in questo elemento dello strumento verrà attraversata dalla lunghezza d'onda specifica che noi abbiamo scelto (340nm) e lo strumento ci darà un segnale che corrisponde all'assorbanza della miscela dovuta alla presenza, in questo caso specifico, del NADH. Noi partiamo dal tempo t0 in cui abbiamo la miscela di reazione che contiene l'enzima e che contiene anche il NADH. Essendo presente il NADH nella miscela e dato che assorbe ad una lunghezza d'onda di 340nm, ovviamente lo strumento legge questa assorbanza (riportato nel grafico). Nel momento in cui parte la reazioneè nella miscela c'è il NADH e anche l'enzima, nel grafico viene rappresentato un certo livello di assorbimento. La reazione non è ancora partita perché è vero che c'è l'enzima e c'è il NADH, ma cosa serve affinché l'enzima lattico deidrogenasi catalizzi la reazione? Serve il substrato, quindi il piruvato. Quindi è questo il motivo per cui l'assorbimento rimane costante. Fino a quando noi non aggiungiamo il substrato (aggiunta indicata dalla freccia nel grafico) l'assorbimento del NADH rimane costante perché non ci sono le condizioni affinché il NADH possa essere ossidato, cioè non c'è il substrato da ridurre, cioè il piruvato.
Quindi l'assorbimento rimane costante. Nel momento in cui aggiungiamo nella miscela il piruvato, comincia ad avvenire: la lattico deidrogenasi catalizza la reazione secondo la quale il piruvato viene ridotto a lattato e il NADH viene ossidato. Siccome è il NADH diminuisce perché si sta trasformando in NAD+, allora l'assorbimento diminuisce. Quindi la diminuzione di questo assorbimento indica che la reazione sta avvenendo e che il NADH sta venendo ossidato a NAD+, che sarà utilizzato dall'assenza dell'assorbimento a 340nm.
Miscela di reazione contenete enzima e NADH O O piruvato C=0 Pyruvate Tracciando la tangente al tratto lineare della curva, CH3 NADH + H+ lactate dehydrogenase NAD+ ΔΑα O AT C HO-C-H Lactate CH3 Tempo(min.)
Questo è un esempio che ovviamente può essere applicato a qualsiasi altra analisi di attività enzimatica, purché si abbia una molecola che assorbe ad una specifica lunghezza d'onda e che cambia nel tempo. Il NADH si presta benissimo innanzitutto perché le deidrogenasi che utilizzano il NADH sono tante e in più il NADH presenta questa difficoltà assorbimento a 340nm tra la forma ridotta e quella ossidata.
L'avvenimento di questa reazione, quindi il coinvolgimento della lattico deidrogenasi viene proprio rappresentata dell'assorbimento a 340nm.
Legge di Lambert e Beer
Un altro elemento che dobbiamo aggiungere per capire come si fa a valutare la velocità di reazione è l'esistenza della legge di Lambert e Beer, una legge molto utile alle applicazioni spettrofotometriche perché stabilisce una relazione diretta tra l'assorbanza e la concentrazione. È fondamentale perché noi valutando la differenza di assorbanza che si ha nel momento in cui la reazione procede (quindi il NADH viene trasformato in NAD+), possiamo sapere la differenza di concentrazione di NADH perché la legge stabilisce che: l'assorbanza è uguale a epsilon per c (concentrazione) per I. L'assorbanza è l'assorbimento che presenta una specie chimica, nel nostro caso la concentrazione di NADH.
Formula della Legge di Lambert e Beer
legge di LAMBERT e BEER: A = Ecl coefficiente di estinzione molare di una sostanza rappresenta l'assorbanza provocata da una soluzione a concentrazione molare unitaria della sostanza ad una data lunghezza d'onda, attraverso una cella di lunghezza ottica unitaria. si può calcolare la velocità iniziale della reazione
Coefficiente di Estinzione Molare e Cammino Ottico
A 340nmEpsilon prende il nome di coefficiente di estinzione molare di una sostanza rappresenta l'assorbanza provocata da una soluzione a concentrazione unitaria molare della sostanza stessa a una determinata lunghezza d'onda. Ogni sostanza che presenta un assorbimento ad una specifica lunghezza d'onda presenterà un coefficiente di estinzione molare. Tenete presente che è un parametro specifico per ogni sostanza che assorbe ad una specifica lunghezza d'onda. L, invece, rappresenta il cammino ottico, ovvero il percorso attraversato dalla luce incidente nella cuvetta, quindi lo spessore che deve attraverare la luce incidente quando dobbiamo misurare l'assorbanza di una determinata specie chimica; generalmente lo spessore di questa cuvetta è di 1cm.
Calcolo della Velocità di Reazione
Tornando alla misura della velocità di una reazione e considerato che esiste la relazione definita da Lambert e Beer tra l'assorbanza e la concentrazione, dalla variazione di assorbanza nel tempo possiamo calcolare la variazione della concentrazione nel tempo. Siccome noi per misurare la velocità della reazione catalizzata dalla lattico deidrogenasi abbiamo deciso di seguire come varia la quantità di NADH e la lettura spettrofotometrica a 340nm ci consente di vedere la diminuzione di assorbanza di NADH, il che vuol dire che quel NADH non c'è man mano, ma viene trasformato di NAD+. Noi, conoscendo la legge di Lambert e Beer potremo, conoscendo la variazione dell'assorbanza, arrivare alla variazione della concentrazione di NADH nel tempo. La misura della variazione di concentrazione del NADH nel tempo sarà una misura della velocità di quella reazione enzimatica. La variazione di assorbanza che ci consente di ottenere, tramite la relazione di Lambert e Beer la variazione di concentrazione, un modo per esprimere la velocità alla quale sta avvenendo quella reazione, che verrà espressa in nmol di NADH ossidato nel tempo o micro-mol di NADH ossidato nel tempo. Quindi la reazione di assorbanza ci consente di ottenere una variazione di concentrazione della specie assorbente nel tempo. E questo ci consente di avere una misura dell'andamento, cioè del procedere di quella reazione, della velocità con cui quella reazione procede.
Fattori che Influenzano la Velocità di Reazione
Questa era una premessa che serve per sapere che in effetti esistono delle procedure, degli approcci elementari che consentono di misurare la velocità di una reazione catalizzata da un enzima. L'approccio spettrometrico è un approccio estremamente utile per fare un'analisi di questo tipo. La velocità di una reazione catalizzata da un enzima da che cosa può dipendere? Può dipendere dalla concentrazione del substrato, dalla concentrazione dell'enzima, può dipendere dalla temperatura o anche dalla presenza degli individui. Quindi adesso noi analizzeremo come e quali sono i fattori che possono in effetti condizionare la velocità di una reazione catalizzata da un enzima. Il primo elemento che dobbiamo analizzare è la concentrazione del substrato. Gli studiosi che si occuparono di studiare la concentrazione del substrato, quindi di studiare in che modo la concentrazione del substrato può influenzare la velocità di una reazione, furono Michaelis e Menten.
Loro evidentemente si occupavano propr concentrazione di un substrato può influenzai arrivare a definire la legge e l'equazione 1 la di di in osservazioni elementari che sono state fatte cui un substrato viene quindi trasformato ir la reazione enzimatica a concentrazione costa :a enzimatica e la differenza della velocità dalla ( Leonor Michaelis & Maud Menten (1913) le condizioni. Cioè, se noi vogliamo vedere soltanto l'effetto cne na una variazione della concentrazione del substrato sulla velocità di una reazione, dobbiamo ovviamente rendere costanti gli altri parametri, che possono influenzare la velocità della reazione: la temperatura, la pressione e