Le Macromolecole: lipidi, proteine, acidi nucleici e polisaccaridi
Documento universitario sulle Macromolecole, che esplora lipidi, proteine, acidi nucleici e polisaccaridi. Il Pdf, un appunto di Biologia per l'Università, descrive in dettaglio carboidrati, proteine e amminoacidi, con classificazioni e funzioni, e analizza processi di sporificazione batterica, trasmissione genetica e metabolismo cellulare.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Le Macromolecole
Le macromolecole sono polimeri di grandi dimensioni che si formano a partire da una serie di molecole più piccole, i monomeri, legate covalentemente. Le macromolecole sono i lipidi, le proteine, gli acidi nucleici e i polisaccaridi.
- I polisaccaridi costituiscono una riserva glucidica, essi sono contenuti difatti in specifici granuli di riserva
- I lipidi, specificatamente i fosfolipidi, sono costituenti fondamentali della membrana e si possono trovare anche sotto forma di granuli di riserva
Nella cellula procariote le macromolecole sono situate nel citoplasma, come nel caso delle proteine (un esempio ne è la flagellina importante proteina costituente del flagello; accessorio dei batteri che ne permette il movimento) e gli acidi nucleici in particola RNA e DNA situati rispettivamente in ribosomi e nucleoide, parete (che presenta differente composizione da quella vegetale e funginea) e membrana plasmatica.
I Carboidrati
I carboidrati o glucidi sono sostanze formate da carbonio ed acqua e possono essere differenziati in base alla loro struttura chimica in:
- Monosaccaridi: essi possono essere pentosi (contenenti 5 atomi di carbonio come ribosio e deossiribosio) oppure esosi (contenenti 6 atomi di carbonio come glucosio che è componente principale della parete cellulare vegetale e fruttosio). Possono, inoltre essere, discriminati in chetosi o aldosi che rispettivamente presentano un gruppo chetonico e un gruppo aldeidico.
- Disaccaridi (2): essi sono composti che nascono per condensazione di due monosaccaridi con conseguente formazione di un legame glicosidico. Questo legame può verificarsi in C4 Beta e C1 Alfa oppure C1/C6)
- Oligosaccaridi (max 10)
- Polisaccaridi (da 10 a migliaia): si distinguono polisaccaridi vegetali (amidi e fibre) e polisaccaridi di origine animale (glicogeno). I polisaccaridi contenenti un unico tipo di zuccheri vengono chiamati omopolisaccaridi, mentre quelli contenenti tipi diversi di monosaccaridi vengono detti etero polisaccaridi. Inoltre, essi possono presentare una struttura lineare come nel caso della cellulosa oppure ramificata come amido e glicogeno; i polisaccaridi ramificati sono un'importante riserva energetica di glucosio.
I carboidrati costituiscono
- fonte energetica principale per le cellule, esempio comune è lo sfruttamento del glucosio per svolgere il processo di respirazione cellulare
- sostegno e rivestimento cellulare
- forniscono gli scheletri carboniosi utili per la sintesi della parete ad esempio
Le Proteine
Le proteine sono composti organici formati da sequenze di amminoacidi legate tra loro attraverso legami peptidici. Caratteristica principale di queste macromolecole è la loro elevata specificità biologica attribuibile secondo la forma e le proprietà chimica presentate; per esempio gli enzimi sono proteine specifiche in grado di velocizzare una certa reazione chimica, anche se parecchio sensibili alle alte temperature (in quanto se elevata può verificarsi la denaturazione) e pH. Le proteine possono essere classificate a seconda della funzione che esse presentano:VAILATI LUNA
- Proteine enzimatiche: accelerano selettivamente le reazioni chimiche
- Proteine di difesa: impiegate nella risposta immunitaria come anticorpi e la loro azione è specifica e diretta.
- Proteine di deposito: svolgono funzione di riserva di amminoacidi
- Proteine di trasporto: impiegate nel trasporto di sostanze di scarto provenienti dal metabolismo.
- Proteine ormonali: svolgono funzione di coordinamento di tutte le attività dell'organismo. Per esempio l'insulina che stimola l'assorbimento del glucosio da parte dei tessuti.
- Proteine a funzione recettoriale: consentono alla cellula di rispondere agli stimoli, esse son ben specifiche. Per esempio sono localizzate sulla membrana cellulare.
- Proteine contrattili a funzione motoria: consentono il movimento. Per esempio le proteine responsabili dei movimenti ondulatori di ciglia e flagelli
- Proteine strutturali: svolgono funzione di supporto meccanico.
- Proteine regolatrici: permettono lo switch on off dei geni, per esempio nei procarioti ci sono e regolano l'RNA polimerasi in RNAm per evitare o incrementare la produzione di lattosio (OPERONE LAC)
Gli amminoacidi sono i costituenti delle proteine e sono delle molecole organiche bifunzionali in quanto presentano un gruppo carbossilico un gruppo amminico. Possono reagire tra di loro, il gruppo amminico e quello carbossilico, ma il gruppo carbossilico in questo caso reagisce come un derivato (non c'è una reazione acido-base). Gli amminoacidi si legano tra di loro attraverso la formazione di un legame ammidico tra il gruppo amminico di un amminoacido e quello carbossilico di un altro.
Classificazione degli Amminoacidi
le diverse classificazioni degli amminoacidi tengono conto delle caratteristiche chimiche del gruppo R, perché gli varia molto le caratteristiche. Gli amminoacidi naturali sono 20. Di conseguenza abbiamo:
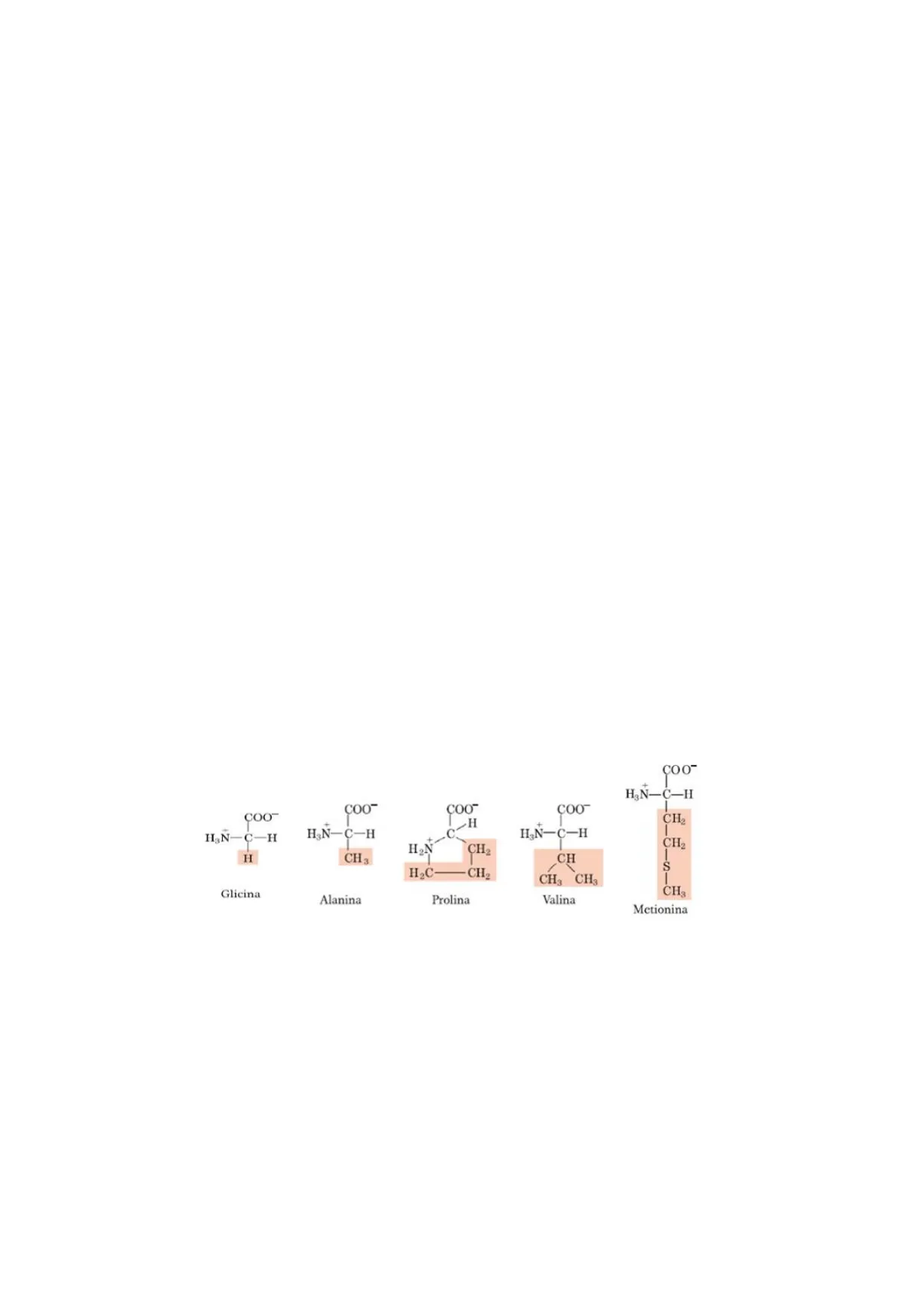
- Gruppi R apolari alifatici: gruppo amminico e carbossilico nella proiezione di Fischer si trovano nella forma ione apolare, questo perché l'idrogeno acido del carbonio può protonare il gruppo amminico. COO- H3N-C-H - COO- COO" COO COO- CH2 H3N-C-H H3N-C-H H3N-C-H - CH2 HON CH2 H CH 3 CH 1 S H2C-CH2 CH3 CH3 1 CH Glicina Alanina Prolina Valina Metionina
- Gruppi R apolari, aromatici: derivati dell'alanina e presentano un anello aromatico al posto dell'idrogeno. Il principale è la fenilalanina, molto importante è anche la tirosina che presenta in posizione para un gruppo ossidrile rispetto al CH2 che è il derivato dell'alanina. Il più complesso è il triptofano che presenta due anelli aromatici: un anello è etero aromatico perché presenta un atomo di azoto nella struttura ciclica. -C-HVAILATI LUNA COO- ÇOO" H3N-C-H H3N-C-H H3N-C-H CH2 CH2 ÇH2 C=CH NH OH Fenilalanina Tirosina Triptofano
- Gruppi R polari, non carichi: gruppi che contengono dei gruppi funzionali che hanno una polarità. COO- COO- COO- - H3N-C-H H-C-OH CH3 Treonina COO- Asparagina Glutammina
- Gruppi R polari, carichi positivamente: gruppi che contengono il gruppo amminico e questo può essere protonato facilmente in condizioni biologiche dando il gruppo NH3+. COO" COO- COO" H3N-C-H HẠN-C-H H3N-C-H CH2 CH2 CH2 CH2 CH2 CH2 CH2 NH C-N CH2 Ī +NH3 C=NH2 NH2 Lisina Arginina Istidina
- Gruppi R polari, carichi negativamente: contengono il gruppo carbossilico che in condizioni biologiche può perdere un atomo di idrogeno e diventare gruppo carbossilato. COO- ÇOO- H3N-C-H ÇH2 COO- CH2 - COO- Glutammato
Le proteine possono assumere delle strutture in sequenza da una primaria a una struttura quaternaria quando il polipeptide iniziale va ad assumere delle conformazioni complesse e differenti. La struttura delle proteine è legata alla funzione e alle sue proprietà. Le diverse strutture delle proteine possono essere:
- Struttura primaria: si intende la sequenza degli amminoacidi ed è determinata e codificata dal DNA con la sintesi proteica (sintetizza amminoacidi che si vanno successivamente a legare). Quando si CH2 1 SH Cisteina COO- H3N-C-H CH2 OH Serina H3N-C-H CH2 CH HON O=0 -000 HON H3N-C-H CH2 - AspartatoVAILATI LUNA parla di amminoacidi all'interno di una catena polipeptidica si parla di residui amminoacidici. Determina tutte le altre strutture.
- Struttura secondaria: si intende il modo in cui gli amminoacidi sono localmente legati tra loro e definiti nello spazio. La catena polipeptidica resta sempre la stessa. Può presentarsi ad alfa-elica o foglietto-beta-pieghettato.
- Struttura terziaria: si intende la disposizione complessiva di tutta la catena polipeptidica ossia come appare globalmente la proteina. Si possono avere due condizioni limite: la rappresentazione globulare (sferica, all'interno del quale è possibile osservare delle strutture ad alfa-elica o dei foglietti pieghettati) o la rappresentazione fibrosa quando invece è lineare.
- Struttura quaternaria: quando si hanno più catene polipeptidiche legate le une con le altre senza legami covalenti.
I Lipidi
I lipidi sono molecole più piccole delle altre biomolecole, e possono essere idrofobici o essere costituiti principalmente da una parte idrofobica; tuttavia può presentare una parte polare (anfifilica). Tra i lipidi vi sono:
- acidi grassi (R-COOH, elevato numero di atomi di carbonio),
- cere (idrocarburiche molto lunghi o possono essere R-COOR' con elevato numero di atomi di carbonio),
- trigliceridi o triestere del glicerolo: sono esteri del glicerolo, si compone una molecola di glicerolo con 3 molecole di estere mediante esterificazione. Gli R possono essere diversi, contemporaneamente saturi o insaturi (spesso lo sono). Digliceride : una molecola di glicerolo si combina con 2 molecole di estere; Monogliceride: una molecola di glicerolo si combina con 1 molecola di estere
- Fosfolipidi e glicolipidi
- Steroidi: categoria di molecole che presentano una struttura simile al colesterolo
acidi grassi saturi= non presentano doppi legami nella struttura, si impacchetta formando una struttura solida acidi grassi insaturi = possono presentare doppi legami nella struttura (almeno un doppio legame). I doppi legami si trovano nella forma cis e questo causa un ripiegamento della molecola (acido oleico ad esempio); così facendo, non permette l'impacchettamento e resta una struttura liquida.
Gli acidi grassi raramente si presentano, all'interno della cellula, in forma libera piuttosto tendono a legarsi ad altre molecole come nel caso dei trigliceridi (legami esterei che ne comportano un'apolarità della molecola stessa). Questa particolarità, permette ai trigliceridi di assolvere la funzione di deposito energetico sotto forma di goccioline all'interno di particolari cellule: gli adipociti. Altri tipi di molecole lipidiche sono gli sfingolipidi; gruppo di lipidi che contengono un solo acido grasso esterificato e sono spesso abbondanti nel tessuto nervoso e nella membrana cellulare. Le funzioni principali sono:
- Fonte di riserva energetica (trigliceridi nella cellula vegetale immagazzinati in oleosomi nei semi in via di sviluppo)
- Funzione strutturale (fosfolipidi) e di legame con altre componenti come le proteine funzionalizzandole soprattutto nell'apparato di golgi.
- Regolazione e isolamento termico
Gli Acidi Nucleici
Gli acidi nucleici sono dei polimeri costituiti dalla ripetizione di nucleotidi. i nucleotidi sono dei monomeri costituiti dalla combinazione di un gruppo fosfato legato a uno zucchero che a sua volta è legato alla base