Biosintesi di Amminoacidi, Nucleotidi e Molecole Correlate
Documento di Università sulla biosintesi di amminoacidi, nucleotidi e molecole correlate. Il Pdf esplora il ciclo dell'azoto, le vie di sintesi degli amminoacidi, purine e pirimidine, con diagrammi esplicativi dei processi biochimici per lo studio della Biologia.
Mostra di più18 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Ciclo dell'azoto
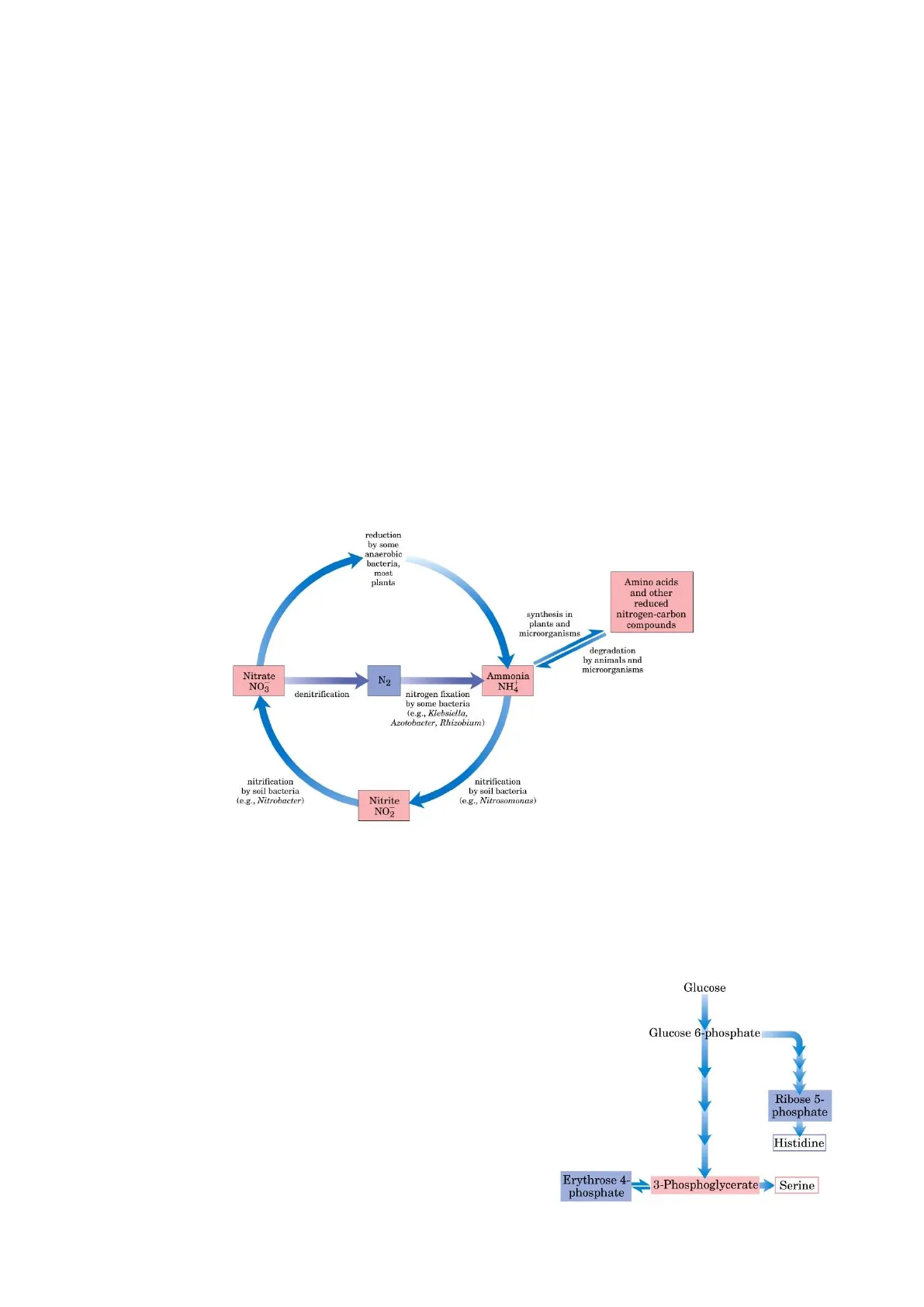
Dopo carbonio, idrogeno ed ossigeno l'azoto è uno degli elementi più abbondanti negli esseri viventi; finora abbiamo visto come esso viene rimosso sotto forma di ione ammonio dalla degradazione degli amminoacidi e convertito in urea per essere espulso. Tuttavia viceversa esso è fondamentale anche per la biosintesi degli amminoacidi stessi, e di altre molecole con vie ed intermedi strettamente interconnessi quali i nucleotidi. Prima di iniziare a percorrere questi sistemi tuttavia diamo uno sguardo al ciclo dell'azoto, con cui esso viene recuperato e riutilizzato nell'ambiente e negli organismi: innanzitutto abbiamo la fissazione dell'azoto atmosferico da parte di batteri, che lo riducono in ammoniaca. Si tratta di particolari microrganismi diazotrofi, che spesso vivono come simbionti nei noduli delle radici delle piante, e sono gli unici in grado di produrre così ammoniaca dall'azoto molecolare gassoso. Essa poi può venire utilizzata da batteri del suolo, che per produrre energia la ossidano a nitriti e successivamente nitrati: questo processo è noto come nitrificazione ed è estremamente diffuso, per cui quasi tutto l'azoto è convertito in queste forme. Esse sono poi facilmente assorbibili da piante e batteri utilizzando delle reduttasi, ed ottenendo di nuovo ammoniaca da inserire per formare amminoacidi; essi sono poi passati da questi organismi a tutti gli altri, come i mammiferi e gli esseri umani. Infine quando questi organismi muoiono la degradazione batterica fa tornare l'ammoniaca al suolo come nitriti e nitrati ricominciando il ciclo; alcuni li convertono ulteriormente in azoto molecolare con la denitrificazione, per cui si compensa anche la prima tappa.
reduction by some anaerobic bacteria, most plants Amino acids and other reduced nitrogen-carbon compounds synthesis in plants and microorganisms degradation by animals and microorganisms Nitrate NO3 N2 Ammonia NHÀ denitrification nitrogen fixation by some bacteria (e.g., Klebsiella, Azotobacter, Rhizobium) nitrification by soil bacteria (e.g., Nitrobacter) nitrification by soil bacteria (e.g., Nitrosomonas) Nitrite NO2
Biosintesi degli amminoacidi
Possiamo ora quindi procedere con la biosintesi, iniziando da quella piuttosto complicata degli amminoacidi; i loro scheletri carboniosi derivano sempre da intermedi della glicolisi, del ciclo dell'acido citrico e della via del pentosio fosfato. Invece l'azoto per il gruppo amminico viene fornito da amminoacidi come glutammato e glutammina che lo cedono ad altri composti come chetoacidi, grazie alle transamminasi; come abbiamo già detto le vie di biosintesi e di degradazione in questa classe di molecole vanno spesso di pari passo. Circa i 10 amminoacidi non essenziali sono prodotti da vie semplici con reazioni e metaboliti in comune, mentre quelli essenziali che vanno assunti nella dieta sono sintetizzati da altri Glucose organismi spesso con vie molto complicate, come accade per gli amminoacidi aromatici. Possiamo allora raggrupparli in base al Glucose 6-phosphate precursore originale del loro scheletro carbonioso; nei casi più frequenti abbiamo il 3-fosfoglicerato della glicolisi e il ribosio-5- fosfato della via dei pentosi fosfati, che sono rispettivamente a 3 Ribose 5- phosphate e 5 atomi di carbonio. Possiamo anche avere loro derivati, come il fosfoenol piruvato e il piruvato o l'eritrosio-4-fosfato, da cui si Histidine ottengono amminoacidi differenti; un caso a parte sono quelli che possiedono nello specifico 4 carboni, che invece derivano da 3-Phosphoglycerate Erythrose 4- phosphate Serineintermedi del ciclo di Krebs - chetoglutarato soprattutto ma anche ossalacetato - visto che non possono essere formati da precursori a 3 o 5C come prima. Inoltre a parte questi 6 precursori fondamentali c'è un intermedio importante sia nella sintesi di amminoacidi che di nucleotidi, ossia il 5-fosforibosil-1-pirofosfato o PRPP, prodotto dal ribosio-5-fosfato grazie ad una pirofosfochinasi che aggiunge i due gruppi in posizione 1. Questo processo consuma ATP e libera AMP, ed è regolato allostericamente da vari suoi prodotti.
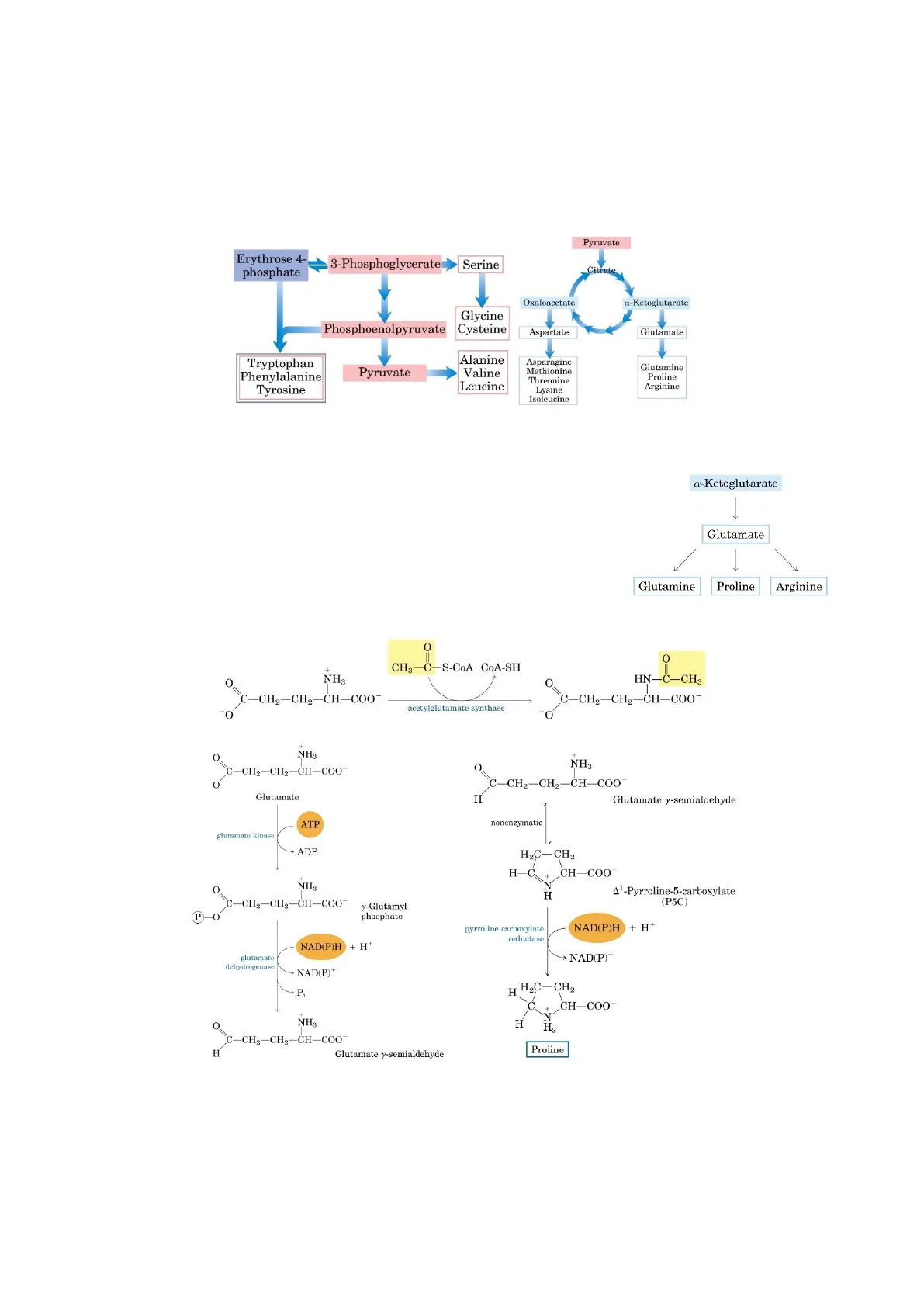
Pyruvate Erythrose 4- phosphate 3-Phosphoglycerate Serine Citrate Oxaloacetate «-Ketoglutarate Phosphoenolpyruvate Glycine Cysteine Aspartate Glutamate Tryptophan Phenylalanine Tyrosine Pyruvate Alanine Valine Leucine Asparagine Methionine Threonine Lysine Isoleucine Glutamine Proline Arginine
Sintesi da alfa-chetoglutarato
Iniziando allora dall'a-chetoglutarato esso fa da precursore per il glutammato, grazie all'enzima deidrogenasi che abbiamo visto nella degradazione degli amminoacidi; in alcuni batteri e piante esiste anche direttamente una glutammato sintasi che lo forma tramite amminazione riduttiva - in a-Ketoglutarate entrambi i casi si consuma NADPH e un gruppo ammonio. Esso poi dà origine a glutammina, come abbiamo sempre visto già parlando della degradazione, prolina ed arginina; la prima è sintetizzata in una via a 4 Glutamate tappe, che richiede una chinasi ed una reduttasi per produrre il 1 glutammato-semialdeide. Esso poi si ciclicizza spontaneamente e può Glutamine Proline Arginine essere trasformato in prolina grazie ad un'altra reduttasi (con consumo di 1ATP e 2NAPDH o NADH).
0 + O NH3 C-CH2-CH2-CH-COO O HN-C-CH3 C- -CH2-CH2-CH-COO- O 0 O NH3 -CH2-CH2-CH-COO O NH3 O Glutamate Glutamate y-semialdehyde 1 glutamate kinase ADP HỌC-CH2 H-Ć + CH-COO NH3 N H 41-Pyrroline-5-carboxylate (P5C) P y-Glutamyl phosphate NAD(P)H + H+ NAD(P)H + H+ glutamate dehydrogenase NAD(P)+ HỌC-CH2 H P C. CH-COO + + O NH3 H N HO C-CH2-CH2-CH-COO H Glutamate y-semialdehyde Proline 0 CH3-C-S-CoA CoA-SH acetylglutamate synthase C-CH2-CH2-CH-COO H ATP nonenzymatic 0 C-CH2-CH2-CH-COO C pyrroline carboxylate reductase > NAD(P)+
Sintesi dell'arginina
Invece l'arginina è prodotta con un sistema quasi identico che tuttavia parte dall'acetilazione del glutammato, in modo da evitare successivamente la ciclizzazione della semialdeide; da essa si produce invece un'acetil-ornitina e un'ornitina, da cui si procede con alcune tappe della via dell'urea per ottenere arginina. La via di sintesi completa è presente nei batteri, mentre nei mammiferi si usa direttamente il ciclo dell'urea per produrre questo amminoacido.O 0 HN-C-CH3 + H3N -- CH2-CH2-CH2-CH-COO N-Acetylornithine N-Acetylglutamate 1 ATP N-acetylglutamate kinase ADP + NH3 + H3N -- CH2-CH2-CH2-CH-COO Ornithine HN-C-CH3 C-CH2-CH2-CH-COO Carbamoyl phosphate P)-O ornithine carbamoyl- transferase Pi NAD(P)H + H+ N-acetylglutamate dehydrogenase ·NAD(P)+ P O HN-C-CH3 O C-CH2-CH2-CH-COO H argininosuccinase Fumarate NH3 HON C CH2-CH2-CH2-CH-COO HON Arginine H3N -- CH2-CH2-CH2-CH-COO N-Acetylornithine
Sintesi da 3-fosfoglicerato
Passando allora al 3-fosfoglicerato, da esso abbiamo la principale via di sintesi della serina, che poi a sua volta è precursore di glicina e cisteina. La serina si ottiene attraverso una serie di 4 tappe che coinvolgono una deidrogenazione del fosfoglicerato in fosfoidrossipiruvato, quindi un trasferimento amminico dal glutammato per ottenere la fosfoserina, e infine la rimozione del gruppo fosfato per la serina.
COO- COO H-C-OH H-C-0-P 0 3-Phosphoglycerate C=0 3-Phosphohydroxypyruvate CH2-0-P CH2-0-P HO NAD phosphoserine aminotransferase phosphoserine phosphatase Pi COO C-0 3-Phosphohydroxypyruvate H3N -- C-H 3-Phosphoserine H3N -- C-H Serine CH2-0-P CH2-0-P CH2OH
Sintesi della glicina
Da qui si può passare poi direttamente alla glicina con un'idrossimetil transferasi, che utilizza il tetraidrofolato e come cofattore il piridossal fosfato per rimuovere un'unità COO monocarboniosa. Ma la glicina può anche essere sintetizzata H3N -- C-H Serine + direttamente da anidride carbonica e ione ammonio con la glicina CH2OH sintetasi, in cui il tetraidrofolato fa da donatore piuttosto che accettore del gruppo metilico.
serine PLP HA folate hydroxymethyl- transferase N5,N10-Methylene H4 folate H2O
Sintesi della cisteina
Infine per quanto riguarda la cisteina essa necessita del contributo di ben due amminoacidi: la serina per lo scheletro carbonioso e la COO + metionina per lo zolfo, convertita in omocisteina - abbiamo già C-H Glycine visto questa via parlando della degradazione. In piante e batteri H invece lo zolfo ridotto necessario viene ottenuto dai solfati presenti nell'ambiente, con una via differente. La cisteina con il suo zolfo ha un ruolo importante nella sintesi di altre molecole, e nella formazione di ponti disolfuro.
+ H3N -- C-H 3-Phosphoserine -0-1 phosphoglycerate dehydrogenase NADH + H+ a-Ketoglutarate COO COO + 0 HN-C-CH3 C-CH2-CH2-CH-COO 0 H2O N-acetylornithinase CH3COO O O. N-Acetyl-y-glutamyl phosphate L-Citrulline ATP + aspartate argininosuccinate synthetase AMP + PPi Argininosuccinate N-Acetylglutamate y-semialdeide Glutamate aminotransferase C a-Ketoglutarate 0 HN-C-CH3 COO- GlutamateNH3 OOC-CH-CH2-CH2-SH + HOCH2-CH-COO +NH3 Homocysteine Serine PLP cystathionine B-synthase H2O NH3 OOC-CH-CH2-CH2 -S- CH-CH-COO +NH3 Cystathionine H2O cystathionine y-lyase PLP NHX + NH3 OOC-C-CH2-CH3 + HS-CH2-CH-COO a-Ketobutyrate Cysteine
Sintesi da ossalacetato e piruvato
Passiamo ora all'ossalacetato e al piruvato, da cui derivano ben nove amminoacidi, di cui 3 non essenziali e 6 fondamentali: a noi interessano solo i primi, ossia asparagina, aspartato (dall'ossalacetato) e alanina (dal piruvato) - gli altri sono prodotti in piante e funghi con vie molto complesse ed interconnesse. In particolare dall'ossalacetato si ottiene prima l'aspartato, grazie ad una transamminazione che usa il glutammato come donatore; lo stesso processo avviene dal piruvato per ottenere l'alanina. L'asparagina deriva invece a sua volta dall'aspartato per ammidazione, con glutammina come donatore di ioni ammonio. Poi dall'aspartato possiamo ottenere anche metionina, treonina e lisina, con un aspartato-ß-semialdeide come intermedio; dalla treonina a sua volta possiamo avere l'isoleucina, che altrimenti è prodotta a partire dal piruvato come valina e leucina.
Oxaloacetate > Aspartate Asparagine Methionine Lysine Threonine -> Alanine Valine Leucine Isoleucine K Pyruvate
Sintesi da fosfoenolpiruvato
Ci rimane quindi ancora il fosfoenolpiruvato, che con l'eritrosio-4-fosfato porta alla produzione di fenilalanina, tirosina (che si può ottenere anche direttamente dalla fenilalanina) e triptofano. La parte più difficoltosa è la produzione dell'anello aromatico, che avviene in piante, funghi e batteri con la chiusura di un precursore alifatico e l'aggiunta graduale di doppi legami; un intermedio fondamentale è il corismato.
Phosphoenolpyruvate + Erythrose 4-phosphate Phenylalanine Tyrosine Tryptophan 1 Tyrosine