Biochimica Lezione 23: Metabolismo delle proteine e degli amminoacidi
Documento dall'Università su Biochimica Lezione 23, che esplora il metabolismo delle proteine e degli amminoacidi. Il Pdf, un set di appunti di Biologia per l'Università, descrive come l'azoto viene incorporato ed eliminato dal corpo attraverso il ciclo dell'urea, trattando amminoacidi essenziali e non essenziali, digestione e ruolo del fegato.
Mostra di più22 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Il Metabolismo delle Proteine
Le proteine sono degli scheletri carboniosi che contengono azoto. Ma dall'azoto come si passa alle proteine? L'azoto proviene dall'atmosfera, è uno dei principali costituenti dell'aria che respiriamo, poi avviene la sua fissazione attraverso la formazione di nitriti e nitrati da parte dei batteri nel suolo e, a questo punto, viene organicato dal mondo dei vegetali, viene formata l'ammoniaca, e poi giunge agli esseri umani attraverso macromolecole organiche, da cui si può andare a creare il mondo degli amminoacidi, le basi azotate e i fosfolipidi. Noi esseri umani, dunque, riceviamo l'azoto dalla dieta.
Le proteine sono molecole che contengono azoto, carbonio, idrogeno e ossigeno, e, hanno la peculiarità di non potersi immagazzinare, quindi di queste sostanze non abbiamo una scorta a differenza di quanto accade per gli zuccheri e per i grassi, che hanno una riserva più o meno grande. Chiaramente nel nostro organismo vi sono le proteine muscolari, che, però, sono proteine d'uso, che verranno utilizzate soltanto in particolari condizioni.
Cosa significa non avere una riserva? L'organismo deve stare attento al proprio dispendio di amminoacidi, infatti, utilizza gli amminoacidi per fare le proteine del corpo e tutto il resto deve essere espulso. Sopraggiunge dunque il problema di come espellere l'azoto, azione che è gravosa per l'organismo; infatti, il ciclo dell'urea è un ciclo costoso che viene svolto dal fegato e che richiede dell'energia, non solo attraverso ATP, ma impegna anche degli intermedi che altrimenti sarebbero utilizzati per il ciclo di Krebs. Bisogna fare quindi attenzione all'assunzione di troppe proteine.
Dal mondo degli amminoacidi si costruiscono tutte le proteine del corpo, ma si ricavano anche altre sostanze, come le basi azotate. Infatti, l'azoto delle basi azotate deriva in parte proprio dal contenuto amminoacidico. Quello che rimane di un amminoacido, quando viene eliminato l'azoto attraverso il ciclo dell'urea, è carbonio ossidabile. Perciò l'amminoacido può essere visto come uno scheletro carbonioso su cui viene introdotto azoto, che, una volta eliminato, lascia un intermedio utilizzabile per fare altri metabolismi, come intermedi del ciclo di Krebs.
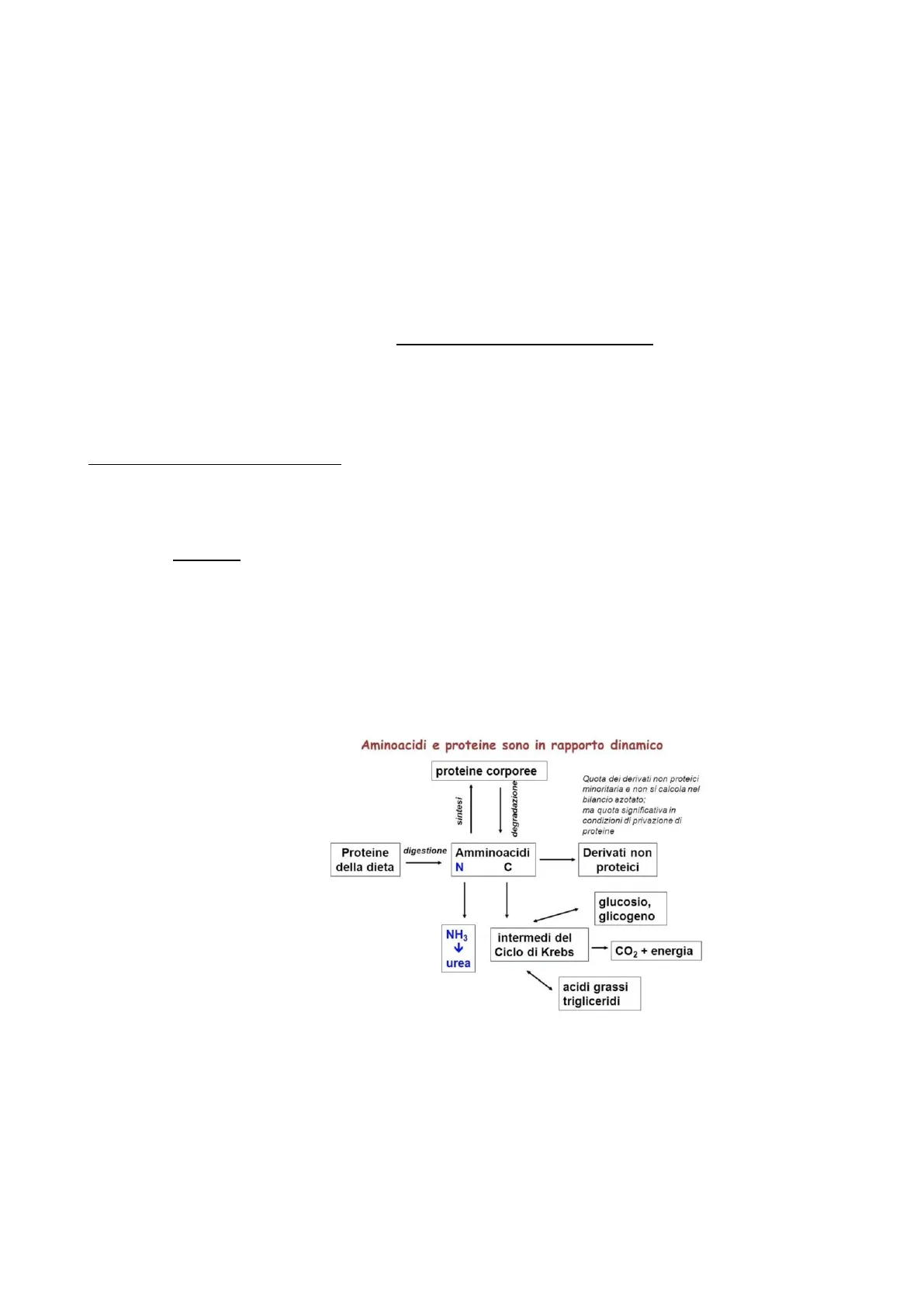
Rapporto Dinamico tra Aminoacidi e Proteine
Aminoacidi e proteine sono in rapporto dinamico proteine corporee sintesi degradazione Quota dei derivati non proteici minoritaria e non si calcola nel bilancio azotato; ma quota significativa in condizioni di privazione di proteine Proteine della dieta digestione Amminoacidi C N Derivati non proteici - glucosio, glicogeno NH3 intermedi del Ciclo di Krebs - CO2 + energia urea acidi grassi trigliceridi
Questi intermedi possono essere bruciati nel ciclo di Krebs per produrre ATP, oppure possono evolvere per fare molecole che servono nella gluconeogenesi, o, in condizione di benessere, esco dal ciclo di Krebs e vado a fare acidi grassi.Biochimica lezione 23 Ventura, Bonaldi, Sgandurra 18/05/2023
Gli Amminoacidi
Gli amminoacidi sono strutture in parte sintetizzate dall'organismo e in parte no. Infatti, gli amminoacidi che non vengono sintetizzati dall'organismo devono essere introdotti con l'alimentazione. Si tratta di 9 amminoacidi essenziali, ovvero: fenilalanina, isoleucina, istidina, leucina, lisina, metionina, treonina, triptofano e valina.
I rimanenti 11 amminoacidi sono:
- sintetizzati a partire da amminoacidi essenziali, possono essere definiti semi-essenziali; è il caso della tirosina che deriva dalla fenilalanina.
- sintetizzati ex-novo dagli scheletri carboniosi che si hanno come intermedi di altri metaboliti; per sintetizzare questi, è necessario avere un apporto di azoto che possa essere incorporato e avere la capacità di organicare dell'azoto.
Gli intermedi da cui si può partire per costituire gli amminoacidi sono i chetoacidi: piruvato, ossalacetato e a- chetoglutarato, oppure da 3-fosfoglicerato, ovvero un intermedio glicolitico.
I 9 amminoacidi essenziali sono essenziali solo per gli esseri umani, poiché si possono reperire dall'alimentazione. Ciò non vale, per esempio, nel mondo dei batteri, dove avvengono delle biosintesi molto complesse in grado di sintetizzare tali amminoacidi. Dunque, la possibilità di omettere queste reazioni poiché si è in grado di assumere tali amminoacidi attraverso la dieta, ha garantito un risparmio energetico.
Valore Nutrizionale delle Proteine
Il valore nutrizionale delle proteine che ingeriamo dipende non soltanto dalla quantità di proteine presenti nell'alimento, ma dipenderà dalla loro digeribilità, ovvero dalla capacità di degradarle e dal fatto che tali proteine siano in grado di ricoprire il fabbisogno, ovvero, se presentano un quantitativo sufficiente di quegli amminoacidi essenziali. Facendo una scala decrescente di tipologie di alimenti più o meno nutrienti, in base al loro valore biologico, si ha:
- tuorlo dell'uovo (porta una grande quantità e variabilità di amminoacidi essenziali)
- latte
- carne
- pesce
- proteine vegetali
- legumi
Spesso le proteine in sostanze come i legumi sono particolarmente legate ad altre sostanze, e dunque sono molto meno digeribili rispetto, ad esempio, alla carne.
Digestione delle Proteine
Le proteine sono l'unico alimento che ha una fase digestiva importante nello stomaco. Infatti, i grassi transitano velocemente per lo stomaco, anche se vi è una lipasi gastrica che attacca alcune classi di acidi grassi e i trigliceridi in posizione 1 e 3; mentre, per quanto riguarda gli zuccheri non succede nulla.
Le proteine hanno una fase digestiva importante, perché hanno una struttura terziaria, e, quando presente, quaternaria caratterizzata da numerosi legami. Questi legami sono altamente sensibili a pH e temperatura.Biochimica lezione 23 Ventura, Bonaldi, Sgandurra 18/05/2023
Tutti questi legami rendono l'interno della proteina non aggredibile, non è possibile scompaginare questa struttura e attaccarla con enzimi sui legami carbo-amminici.
Per questo motivo è necessario denaturare la proteina, rendendo lineare la struttura precedentemente aggregata.
Dunque, a priori è necessario scompaginare la struttura terziaria o quaternaria, sia grazie alle contrazioni dello stomaco, sia grazie al pH fortemente acido.
Nella bocca avviene la frammentazione del cibo, ma non succede nient'altro per quanto riguarda la digestione delle proteine. Una importante denaturazione avviene a livello dello stomaco, dove agiscono numerosi enzimi, che si dividono in due categorie principali:
- Endopeptidasi: idrolasi dei legami peptidici interni
- Pepsina => stomaco
- Tripsina, chimotripsina ed elastasi => duodeno
- Esopeptidasi: idrolisi dei legami peptidici degli amminoacidi esterni
- Carbossipeptidasi, aminopeptidasi e dipeptidasi => duodeno
Endopeptidasi: Enzimi e Specificità
Endopeptidasi Enzima Presenza PH ottimale Specificità Pepsina Stomaco 1,5 - 2,5 Tyr, Phe, Leu -NH Tripsina Intestino 7,5 - 8,5 Arg, Lys -COOH Chimotripsina Intestino 7,5 - 8,5 Trp, Phe, Tyr, Met, Leu -COOH Elastasi Intestino 7,5 - 8,5 Ala, Gly, Ser -COOH
Esopeptidasi: Enzimi e Specificità
Esopeptidasi Enzima Presenza PH ottimale Specificità Sono METALLO PROTEASI -> necessario assumere SALI per garantire la digestione Carbossipeptidasi Lume intestinale -COOH Terminale Aminopeptidasi Mucosa intestinale pH del succo -NH3 intestinale Terminale Dipeptidasi e tripeptidasi Mucosa intestinale Dipeptidi e tripeptidi
1. Anidrasi Carbonica e Formazione di HCl
Una volta che il cibo entra nello stomaco, la sua parete si dilata, attivando le anidrasi carboniche, degli enzimi della parete intestinale, che trasformano la CO2 presente nel sangue in acido carbonico H2CO3. A questo punto l'acido carbonico si dissocia e vengono prodotti una grossa quantità di H+ e di carbonati HCO3 . Gli H+ vengono espulsi nel lume dello stomaco, (in antiporto con gli ioni potassio K+, che invece vanno nel plasma), insieme ai Cl- che arrivano dal sangue, in questo modo ho quindi la formazione di HCl. I carbonati, invece, tornano indietro nel sangue, (in antiporto con gli ioni cloro, che invece entrano nel lume dello stomaco), e vanno nel plasma insieme al potassio. Dunque, l'attivazione dell'anidrasi carbonica comporta un'acidificazione del lume dello stomaco e contestualmente l'eliminazione della base coniugata dell'acido carbonico nel sangue. Dopo un pasto abbondante si ha una basificazione delle urine e un aumento dei carbonati nel plasma.
2. Gastrina e Pepsinogeno
L'acidificazione dell'ambiente e le contrazioni dello stomaco, porta delle specifiche cellule ghiandolari dello stomaco: le cellule G, a produrre la gastrina, un ormone che accelera la produzione di acido carbonico e induce il rilascio di pepsinogeno (proteina inattiva), il precursore della pepsina (versione attiva). Quando viene secreto in ambiente acido, per un processo di autocatalisi: la proteina taglia una parte di sé stessa: dalla rottura del pepsinogeno si ricava: la pepsina e una piccola parte rimasta dal taglio che funzionerà da inibitore della pepsina stessa, la pepstatina.
3. Pepsina e Autoregolazione
La pepsina è un enzima che taglia tutti i tipi di legame peptidico: con più specificità alcuni legami peptidici e con meno specificità altri. Questo enzima, ci è utile quando c'è il cibo perché va ad attaccare le proteine ingerite con l'alimentazione, poi, però, può agire in maniera dannosa verso le strutture proteiche della mucosa dello stomaco. Esiste quindi un inibitore, chiamato pepstatina, che, è in competizione con le proteine degli alimenti per legarsi con la pepsina, quando gli alimenti sono presenti la pepsina agisce contro di essi, ma, quando questi scemano, la pepsina si lega alla pepstatina che va ad inibire l'attività catalitica della pepsina: questo è un meccanismo di autoregolazione. La pepsina è un'endopeptidasi, cioè un enzima che taglia i legami peptidici all'interno della struttura. Quindi taglia in più parti la sequenza, formando i primi frammenti. La gastrectomia, la rimozione chirurgica dello stomaco comporta un rallentamento nella digestione delle proteine. Avendo analizzato una prima digestione delle proteine da parte dello stomaco, attraverso il piloro si passa nella prima parte dell'intestino.
4. Colecistochinina e Enzimi Pancreatici
Nell'intestino ci sono due tipologie di enzimi: quelli pancreatici e quelli dell'intestino. Appena arriva il cibo, la parete intestinale produce secretina e colecistochinina. La colecistochinina ha il compito di avvisare il pancreas esocrino di rilasciare gli enzimi necessari alla digestione. Gli enzimi del pancreas esocrino sono: il tripsinogeno, il chimotripsinogeno, la proelastasi e delle procarbossipeptidasi. Tutti questi enzimi vengono rilasciati dal pancreas in forma inattiva.
NB= Il suffisso -geno indica sempre la presenza di un precursore immaturo dell'enzima.
5. Tripsinogeno e Attivazione Enzimatica
Il tripsinogeno rilasciato dal pancreas raggiunge l'intestino e viene attivato da delle enteropeptidasi, cioè enzimi che vengono prodotti localmente dagli enterociti: sono enzimi esocellulari che vanno a tagliare il tripsinogeno e lo trasformano in tripsina attiva. La tripsina attiva si farà promotrice dei tagli che attivano gli altri enzimi pancreatici: infatti, va a tagliare e rendere attivi il chimotripsinogeno (che diventerà chimotripsina), la proelastasi (che diventerà elastasi) e la procarbossipeptidasi (che diventerà carbossipeptidasi). Tripsina, chimotripsina ed elastasi sono delle endopeptidasi, cioè enzimi che contribuiscono al processo avviato precedentemente dalla pepsina, riducendo ulteriormente le dimensioni dei peptidi, riconoscendo specificamente dei particolari legami peptidici, appoggiandosi sulla catena peptidica.
6. Carbossipeptidasi A e B
Le carbossipeptidasi, A e B, invece, sono degli enzimi, rilasciati sempre dal pancreas esocrino, che intervengono all'estremo carbossilico, e sono perciò delle esopeptidasi, che servono per lasciare amminoacidi singoli alla catena C-terminale. Una volta attivate, agiranno staccando amminoacidi terminali.
7. Amminopeptidasi e Dipeptidasi
Oltre alla enteropeptidasi, le cellule intestinali sono in grado di produrre delle altre peptidasi terminali, sia per il C-ter che per I'N-ter, che però non vengono propriamente rilasciate, ma rimangono all'interno delle cellule intestinali. Tali sostanze possono finire nel lume intestinale poiché le cellule della mucosa intestinale che le producono si sfaldano continuamente. Servono perché non sono presenti solo amminoacidi semplici, ma anche dei piccoli peptidi, che, possono attraversare dei traslocatori ed entrare nella cellula dell'intestino, qui possono essere processate nella parte terminale, divenendo scissi in singoli monomeri di amminoacidi,