Spettrometria di Massa: tecnica diagnostica e interpretazione degli spettri
Documento da C.i. di Diagnostica di Laboratorio su Spettrometria di Massa. Il Pdf esplora questa tecnica diagnostica fondamentale in Chimica per l'Università, illustrando applicazioni, definizioni e analizzatori come quelli a quadrupolo e tempo di volo, con frammentazione dello ione molecolare.
Mostra di più19 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Spettrometria di Massa: Introduzione e Applicazioni Diagnostiche
C.I. di DIAGNOSTICA DI LABORATORIO MODULO DI TECNICHE DI LABORATORIO Prof. Edmondo Ceci Lezione n. 9 Data: 11/04/2024 Sbobinatore: Lombardi Nica Revisionatore: Zingariello Lorenzo SPETTROMETRIA DI MASSA Parliamo di spettrometria di massa una tecnica che ormai è di interesse a livello diagnostico, molto prevalente rispetto a tante altre tecniche. È una tecnica che fino a qualche anno fa era compresa prevalentemente in tantissime analisi che prevedevano il "food", quindi frutti alienanti, frodi, qualsiasi cosa inerente la gestione del "medding" ("medding food"="mischiare il cibo") questo in merito alla "nostra sicurezza alimentare". Da queste applicazioni, alimentari, si è compreso come effettivamente la spettrometria di massa poteva essere di ausilio in laboratorio analisi. Per cui ormai ha preso piede da qualsiasi tipo di laboratorio, qualsiasi ospedale e i primi passi gli ha compiuti a livello di screening metabolico neonatale. È stata la prima tecnica utilizzata per il monitoraggio dei disguidi metabolici. Parliamo ancora una volta di quelli tutti nati nel territorio nazionale, quelli che vengono sottoposti alla puntura del tallone e sulla goccia, sullo "spot di sangue" vengono testate 40 malattie metaboliche, negli USA lo screening ormai si è evoluto notevolmente e sono arrivati a testare 90 malattie rare. In puglia siamo tra gli ultimi ad aver adottato questa tecnologia. Per tutti i nati nella regione puglia c'è un centro di riferimento a cui tutti i centri di nascita fanno riferimento per mandare i talloncini, gli spot di sangue. Tecnica molto importante quindi, molto versatile, accoppiata ad una tecnica che separi le molecole. Tecniche cromatografiche (di cui abbiamo già parlato precedentemente nelle altre lezioni). Abbiamo parlato di cromatografia sia liquida che gassosa, che vi permettono di isolare i singoli analiti per poi evidenziarli con questo tipo di tecnica. La spettrometria è una tecnica molto potente e molto costosa.
La spettrometria di massa è una tecnica analitica applicata sia all'identificazione di sostanze sconosciute, sia all'analisi in tracce di sostanze note. La spettrometria di massa combinata alla spettroscopia a risonanza magnetica nucleare (NMR) e infrarossa (IR) riesce a fornire la struttura completa di una molecola organica (nessuna tecnica è «autosufficiente»). La spettrometria di massa ci fornisce la massa delle molecole.
Applicazioni della Spettrometria di Massa
- Rivelare e identificare l'uso di steroidi da parte di atleti.
- Determinare se il miele è stato adulterato con l'uso di sciroppi zuccherini.
- Determinare la presenza di diossine in pesce contaminato.
- Effettuare analisi in medicina legale come la conferma e la misura quantitativa di droghe e del loro abuso.
- Effettuare analisi di sostanze inquinanti per l'ambiente.
- Identificare e determinare quantitativamente i componenti di miscele organiche complesse.
Potenza della Spettrometria per Sostanze Sconosciute
Perché la spettrometria è una tecnica molto potente? -perché possiamo utilizzarla anche per identificare sostanze sconosciute. Fino ad oggi abbiamo visto tecniche che permettevano la codificazione, la quantificazione di sostanze attraverso degli standard di riferimento. Con questo tipo di tecniche è possibile andare ad identificare sostanze sconosciute attraverso banche dati molto grandi, residenti nel computer che possono accessibili a icloud. Quindi abbiamo ad esempio il caso del "food", ma anche dei dati che riguardano tutti i possibili pesticidi ad oggi noti, stessa cosa per gli inquinanti, quelli che sono i maggiori inquinanti 1C.I. di DIAGNOSTICA DI LABORATORIO ambientali "diossina", idrocarburi aromatici ecc ... tantissime sostanze di natura completamente differente. Questa tecnica si basa su un concetto fondamentale cioè sull'identificazione del peso molecolare della sostanza. La spettrometria ci fornisce la massa delle molecole. E già questo è un aspetto importante che vi fa risalire ad un esatto PM. Il problema però è per le piccole molecole, ad esempio: "ormoni tiroidei", ecc ... , che allo stesso peso molecolare possono essere attribuiti vari composti. Quindi il solo criterio di identificazione del Peso Molecolare non è sufficiente per discriminare la presenza di una determinata molecola. Per cui non possiamo limitarci a questo unico indizio. Che cos'è effettivamente il PM di una sostanza?
- Il peso molecolare non è altro che la somma dei pesi atomici di ciascun atomo presente all'interno della molecola moltiplicato per il coefficiente stechiometrico, ma ovviamente oltre alla massa esatta di una molecola c'è da considerare il contributo isotopico, perché ogni atomo presente in natura ha un corredo di isotopi.
Definizioni Chiave nella Spettrometria di Massa
- Massa Nominale: massa della molecola basata solo sugli isotopi più abbondanti, approssimata all'intero più vicino.
- Massa Ponderale: Massa mediata sulla distribuzione isotopica (= peso atomico). Presenta due cifre decimali.
- Massa Esatta: Massa esatta di una molecola, tenendo conto dei rapporti isotopici, a 4-5 cifre decimali.
- lone Molecolare: lone di peso corrispondente alla massa nominale.
- Pattern Isotopico: Set di ioni molecolari a peso diverso dovuti alla distribuzione isotopica.
Misurazione e Unità di Massa/Carica
Uno spettrometro di massa è uno strumento che misura la massa di una molecola dopo che è stata ionizzata. In spettrometria di massa si misura quindi il rapporto m/z.
- Unità di misura della massa:
- 1 Da (= u) è 1/12 della massa di un atomo di 12C
- Unità di misura della carica:
- carica elementare = carica posseduta da un e- (o da un protone)
- m/z
- Z = carica di uno ione, numero di cariche elementari posseduto dallo ione
- se z =1 allora m/z è la massa in Dalton
- Se z = 2 e lo ione ha massa 200 Da, vedrò un segnale a m/z = 100
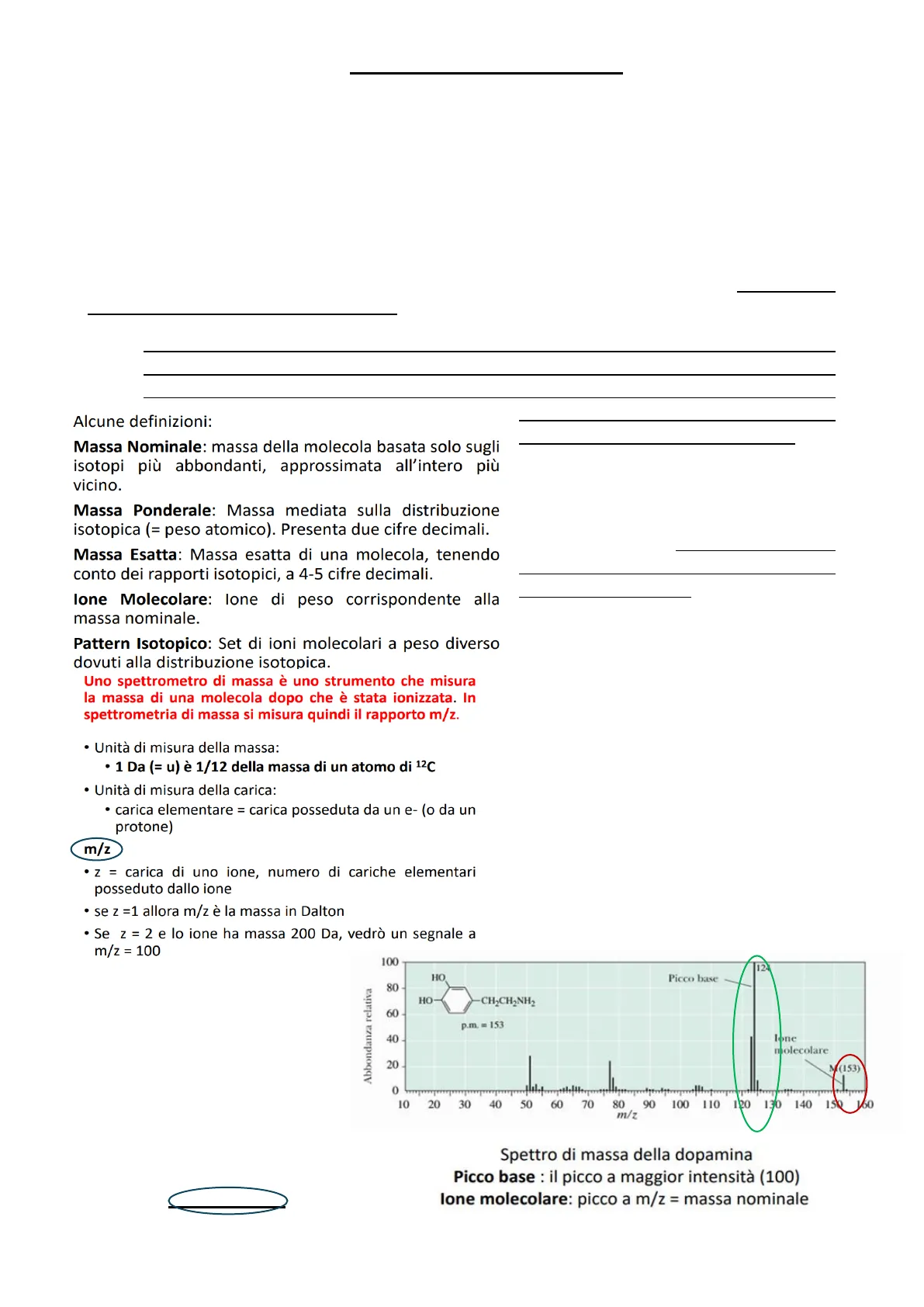
ionizzazione della molecola, la sua decomposizione in frammenti e l'identificazione a seconda dei frammenti della molecola madre. Generando uno ione, ovviamente non possiamo ragionare in termini di massa unitaria, ma ragioniamo in termini di massa/carica, solo Quindi questa tecnica si basa effettivamente sull'analisi della massa di una molecola, quando noi esprimiamo il peso molecolare di una sostanza grammi/moli. L'unità di massa è effettivamente il Dalton. 1 Dalton è 1/12 di quella che è la massa dell'atomo di Carbonio naturale. Come sapete dalla formazione di fisica, l'unità di massa è una delle 7 grandezze fondamentali. Quindi il calcolo dei pesi atomici di tutti gli atomi presenti nella tavola periodica è rapportato all'atomo di carbonio. Quando invece parliamo di esperimenti stiamo parlando di massa/carica. Quello che accade nello spettrometro di massa è: la 100 12 HO Picco base 80 Abbondanza relativa HO- -CH2CH2NH2 60 p.m. = 153 40 Ione molecolare 20 M(153) 0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 150 m/z Spettro di massa della dopamina Picco base : il picco a maggior intensità (100) lone molecolare: picco a m/z = massa nominale 2C.I. di DIAGNOSTICA DI LABORATORIO che essendo uno ione monovalente al denominatore è 1, quindi la massa corrisponde effettivamente al peso molecolare della molecola. Quello che accade è che una molecola neutra entrando in questa particolare strumentazione viene ionizzato si genera uno ione, lo ione a più alto peso molecolare che rappresenta il peso effettivo della molecola da questo poi si generano dei frammenti con peso molecolare via via più piccolo. Cioè la molecola organica si frammenta in tanti di quei pezzetti. Unendo quei pezzi noi riusciamo a comprendere com'è fatta quella molecola. In questo esempio (vedi immagine sovrastante), solito grafico x y, sull'asse delle ascisse (x) abbiamo i pesi molecolari (massa/carica), sull'asse delle ordinate (y) l'abbondanza relativa, quindi in termini di quantità, degli ioni che vengono prodotti si esegue una lettura che va da dx verso sx. Quindi andiamo ad identificare il peso molecolare più alto che rappresenta il PM della molecola, in questo caso il PM: 153. Esiste un libro che contiene tutti i composti molecolari, organici noti e vengono rappresentati in funzione della loro formula, degli atomi di N, C,H, e il pm. Se avessimo questo libro con pm 153 vedremmo rappresentate almeno, 50-60 molecole diverse le vedremmo rappresentate con la loro formula e il peso molecolare, stesso peso molecolare ma con caratteristiche chimiche una diversa dall'altra. Quindi il solo peso molecolare non può essere l'informazione base per capire di che molecola stiamo parlando. Dopo di che andiamo a interpretare lo SPETTRO DI MASSA andando a identificare gli altri frammenti. La molecola che entra nello spettrometro di massa risulta ionizzata ha perso l'elettrone, quindi il rapporto massa/carica, la sua massa è rimasta intatta ha perso un elettrone, la sua massa molecolare continua as essere 153. Quindi: il pm 153 molecola intatta, ionizzata, e questo è di picco 124 quindi come si ragiona? In termini di differenza 153-124= è un frammento che pesa (massa/carica) 29. Cosa si è staccato di quella molecola?cosa la molecola ha perso? Perché la molecola si frammenta da dx verso sx avremo valori di massa molecolari sempre più piccoli. E cosi vado ad identificare tutti i frammenti. Si è creata una banca dati andando andando a identificare tutti quanti i frammenti e andadno ad acquisire questo spettro di massa. Si e' creata una banca dati andando a frammentare a ionizzare tutte le molecole vuote ed ad acquisire tutto questo spettro di massa. Lo strumento cosa fa? Acquisisce questo spettro di massa lo va a paragonare con quello che ha nella sua banca dati e va a fare un "fittinhg" quando trova dei frammenti identici con la stessa intensità riesce ad identificare di che molecolasi tratta. Ogni molecola frammenta si spezza in modi completamente differente, dunque non è solo un'identificazione della massa molecolare ma è tutto il pattern di frammentazione che ci porta a considerare, a valutare effettivamente di che molecola stiamo parlando. Questa era una Amina biogena la "dopamina" pesa 153 e qualsiasi strumento, spettrometro di massa, frammenteranno sempre generando questo tipo di frammento. E' come se quel pattern di frammentazione fosse l ` impronta digitale di quella molecola, solo di quella molecola. Quindi nel momento in cui noi non siamo in grado di avere lo "standard" di dopamina - cosa impossibile - comunque ho la possibilità attraverso una banca dati di dire per me questo composto effettivamente è dopamina. E' ovvio che il software da uno score es: ci da delle % via via anche più basse che significa che il fittinhg dei frammenti che vengono generati non è perfettamente coincidente. Non ci sono sostanze organiche che non ionizzino. Posso avere bisogno di una più alta o più bassa energia ma tutte frammentano e questo modo di frammentare segue delle regole. La spettrometria di massa non hanno fatto altro che un po' di mesi fa con il progetto del genoma umano hanno classificato tutte le proteine e in questa maniera si sono caratterizzate tutte le molecole organiche ad oggi note. 3