Spettrometria di massa: analizzatori e tecniche di ionizzazione
Documento di Università sulla spettrometria di massa e gli analizzatori. Il Pdf, un insieme di appunti universitari di Chimica, esplora la spettrometria di massa, descrivendo analizzatori e tecniche di ionizzazione, come quella elettronica e chimica.
Mostra di più20 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Proteomica: Spettrometria di massa - Analizzatori
Prof. Fulvio Magni - Data Lezione (04/03/2021) - Autore sbobina: Danilo Morelli - Revisore: Giosuè Moscato Riprendiamo la descrizione delle parti che compongono uno spettrometro di massa. Nell'ultima lezione abbiamo introdotto la spettrometria di massa, abbiamo visto alcuni cenni storici, abbiamo visto alcune informazioni sulle caratteristiche dello spettrometro di massa in modo tale da avere una visione e una ragione del motivo per il quale lo spettrometro di massa viene utilizzato in un campo di applicazioni sempre più variegate. Lo spettrometro di massa trova utilizzo in settori diversi, in laboratori che hanno finalità diverse per la sua capacità di poter analizzare molecole con caratteristiche chimico-fisiche totalmente diverse (carboidrati, lipidi, proteine, gas ecc.). È in grado di dare un segnale molto specifico anche in presenza di piccole quantità e indipendentemente dalle dimensioni delle molecole. L'unica limitazione dello spettrometro di massa è che non può analizzare le molecole che non possono essere portate allo stato gassoso e ionizzato; dunque, i requisiti essenziali sono portare allo stato gassoso, perché all'interno dello spettrometro c'è il vuoto, e ionizzare perché siamo in grado di manipolare ioni e non molecole neutre. Avevamo anche cominciato ad entrare più nel dettaglio: avevamo visto il sistema da vuoto, come funziona e perché dobbiamo avere un valore di vuoto molto elevato. Nello spettrometro c'è la sorgente ionica, l'analizzatore e il rivelatore. Avevamo già descritto due delle tante tecniche di ionizzazione e le prime ad essere introdotte: la tecnica di ionizzazione elettronica (e abbiamo anche spiegato come mai il termine "impatto elettronico", che veniva usato nel passato, non vada bene) e la ionizzazione chimica. Avevamo descritto come è fatta una sorgente ionica e quali sono i fenomeni cinetici che avvengono all'interno di una sorgente ionica:
-
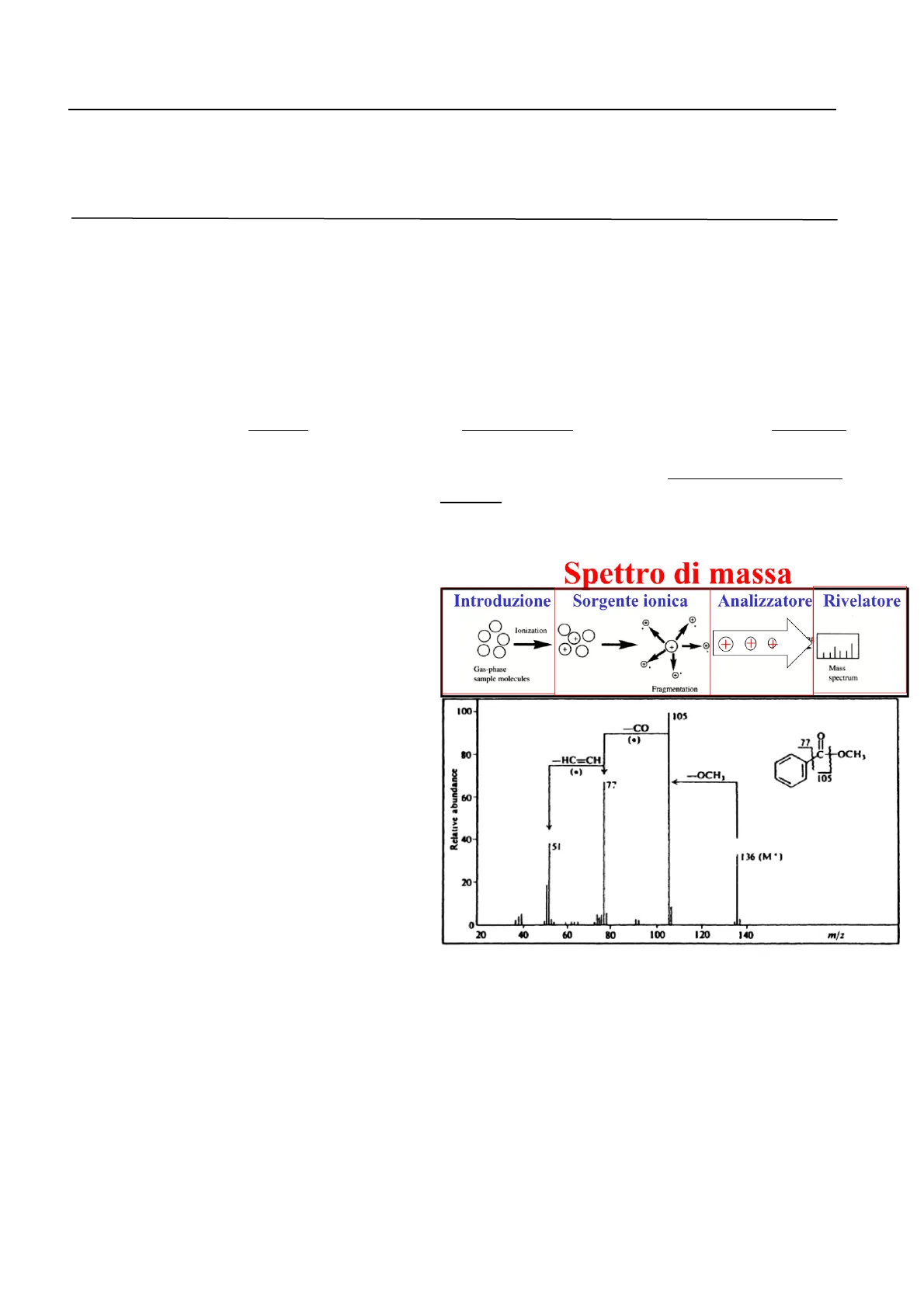
Nel caso della ionizzazione elettronica avevamo descritto come avviene il processo di ionizzazione e che cosa accade durante questo processo. Si forma lo ione molecolare, ma si formano anche dei frammenti perché durante la ionizzazione elettronica vi è un grosso trasferimento di Spettro di massa Introduzione Sorgente ionica Analizzatore Rivelatore Ionization T Gas-phase sample molecules Mass spectrum Fragmentation 100- 105 -CO (·) 77 80- C++-OCH, -HC=CH Relative abundance (·) -OCH, 105 60 8 40 51 136 (M *) 20 0 20 40 60 80 100 120 140 m/z energia, un grosso trasferimento di elettroni. Avevamo anche compreso come mai è stato stabilito universalmente di utilizzare elettroni con un contenuto energetico pari a 70 eV.
-
Con la ionizzazione chimica il processo di ionizzazione, sempre operato da elettroni, è inizialmente a carico del gas reagente; è il gas reagente che, una volta ionizzato, va a ionizzare l'analita tramite una reazione acido- base che, come tutte le reazioni, ha il suo AH di formazione che ci dice se durante la reazione l'energia viene assorbita dai prodotti o viene rilasciata (ci dice se la reazione è endotermica o esotermica). L'energia che viene rilasciata viene ceduta all'analita.
Il processo di ionizzazione chimica è una "ionizzazione soffice" perché il processo di frammentazione è molto limitato, così come la quantità di energia che entra in gioco. Durante il processo di ionizzazione chimica gli elettroni, dopo aver ionizzato il gas, rimangono in sorgente, ma hanno un contenuto energetico inferiore, per cui possono 4 73essere facilmente catturati dall'analita e formare ioni negativi. Per questo motivo, se nella ionizzazione elettronica abbiamo solo ioni positivi (99%), nella ionizzazione chimica abbiamo a disposizione ioni sia negativi sia positivi e possiamo sfruttare le caratteristiche di questi ioni, in quanto già durante la ionizzazione chimica aumenta l'intensità dello ione molecolare, ovvero migliora la LOD strumentale, nel caso della ionizzazione chimica negativa, dato che il rumore di fondo diminuisce, abbiamo un incremento di LOD; quindi bastano meno molecole di analita per aver un buon rapporto segnale-rumore. FINE RIASSUNTO LEZIONE PRECEDENTE. In questa lezione prenderemo in considerazione gli analizzatori. Anche in questo caso descriveremo solo alcuni analizzatori e nelle prossime lezioni ne vedremo degli altri. Nella descrizione didattica degli analizzatori, esattamente come è stato fatto per le tecniche di ionizzazione, seguiremo l'excursus storico descrivendo il primo analizzatore che è stato introdotto e cosa è successo nel tempo. Iniziamo quindi a descrivere l'analizzatore, poi descriveremo i sistemi di rivelazione e infine cercheremo di entrare nel dettaglio, in maniera molto semplice, sulle informazioni presenti all'interno di uno spettro di massa.
Caratteristiche tipiche degli analizzatori
Le caratteristiche tipiche di tutti gli analizzatori sono: il range di massa, la risoluzione, la velocità di scansione e l'efficienza di trasmissione. Di queste quattro caratteristiche, quelle più importanti per noi sono il range di massa e la risoluzione.
Range di massa
Il range di massa, o intervallo di massa, è quell'intervallo entro il quale l'analizzatore è in grado di separare. Noi potremmo avere un analizzatore che utilizza lo stesso principio, ad esempio un analizzatore quadrupolare, che descriveremo poi nel dettaglio. In commercio esistono dei quadrupoli che separano da m/z 1 a m/z 650, da m/z 1 a m/z 3000, a 4000 ecc. Cosa vuol dire? Il range di massa ci dice che siamo in grado di separare lo ione a m/z 1 dallo ione a m/z 2, dallo ione a m/z3 ... fino a m/z 650, 3000 o 4000 poi non riesce a separare più. Fate attenzione perché lo stesso tipo di analizzatore può avere un intervallo di massa diverso entro il quale funziona; ovviamente questo impatta anche sul costo.
Risoluzione degli analizzatori
L'altra caratteristica degli analizzatori è la risoluzione, ovvero la capacità di separare ioni con un valore diverso di m/z. Ad esempio, esistono degli analizzatori in grado di separare ioni che si differenziano di 1 Dalton (separano il 100 dal 101, il 101 dal 102 ecc.), ma esistono anche analizzatori in grado di separare ioni che si differenziano da una sola cifra decimale (separano lo ione a m/z 100,0 da quello a m/z 100,1). La risoluzione è la parola che noi utilizziamo per indicare questa caratteristica dell'analizzatore. Tutti gli analizzatori, indipendentemente dal modo con cui separano, sono caratterizzati dall'intervallo entro il quale funzionano e la risoluzione.
Significato della risoluzione
Cerchiamo di capire meglio il significato della parola "risoluzione". Su questa parola c'è molta confusione; nelle slide sono presenti due articoli che potete andare a leggere per cercare di capire. Noi cercheremo di avere un'idea generale in modo da poterci districare nella confusione con cui questi termini vengono utilizzati. Quando parliamo di risoluzione sappiamo che tutte le macchine fotografiche hanno una risoluzione diversa e sappiamo benissimo che la risoluzione di una macchina fotografica è la capacità della macchina di dare immagini nitide, ben chiare e che ci mostrino bene anche i dettagli più piccoli. Quindi potremmo dire che la risoluzione è "la capacità di vedere nel dettaglio"; tanto più è piccolo il dettaglio che siamo in grado di vedere, tanto maggiore sarà la risoluzione. Nel nostro caso, quando parliamo di analizzatori il dettaglio è il segnale che lo strumento ha ottenuto costringendo l'analita - o gli analiti - a generarlo. La risoluzione è la capacità dell'analizzatore di separare il segnale dello ione a m/z Am = 1 Da 578.4 10 Relative Abundance 80 40 20 8 8 8 8 579.3 580.3 581.3 0 578 579 580 581578,4 dal 579,3 (figura pagina precedente). L'analizzatore dell'immagine è in grado di separare due ioni che differiscono di 1 Dalton. Spesso questa risoluzione non è adeguata perché potrebbe succedere che sotto il segnale di 1 Dalton possano esserci 3 analiti diversi (figura e descrizione successive). Guardando la figura a destra si vede un picco che è largo 1 Dalton. Potrebbe succedere che sotto questo segnale ci siano 3 segnali di 3 analiti diversi. Ad esempio, se nel soggetto sano questo segnale vale 1000 e nel soggetto malato vale 500 e volessi capire quale di questi analiti causa la riduzione di intensità tra il soggetto sano ed il soggetto malato, in realtà non lo potrei sapere. Per poter avere questa informazione devo per forza avere un analizzatore che sia in grado di separare questi tre ioni a m/z leggermente diversi. Esistono quindi analizzatori che separano nel modo appena descritto (prima figura a destra), ma noi possiamo aumentare la capacità di risoluzione. Se ricordate quando abbiamo visto la colonna cromatografica, tanto più la risoluzione è alta, tanto più il picco è stretto. Se il picco è stretto possiamo 578.4 100 vedere anche tutto ciò che è compreso in 80 Relative Abundance 60 questa zona (punto rosso del secondo grafico a 40 destra) che, con un potere risolutivo come 20 quello nella figura in alto, non saremmo stati in grado di vedere. 0 578 ISOBARIC IONS 100 95 90 85 80 75 70 65 Relative Abundance 60 50 oxidated methionine (C5H11NO3S) 147.035 phenylalanine (CgH11NO2) 147.068 35 30 25 20 15 10 5 248.8 249. 249.2 249. 249.6 RISOLUZIONE 578.2 100 80 Relative Abundance 60 40 579.2 20 580.3 581.3 T 0 578 579 580 581
Risoluzione e potere risolutivo: Isopro
Guardiamo ora il primo dei due grafici a destra. Noi siamo in grado di separare la prima molecola che ha 27068 151611 R = 64350 un valore di massa molecolare di 142,062567 dalla molecola che ha una massa molecolare di 142.07825 142.07825 142,07825. Il primo analizzatore è in grado di 0,015683 = 10000 R Methylnaphtalene 12C10H814N1 0,00447 Methylquinolene Am 12C11H10 = 142.07825 = 142.062567 separare due ioni che differiscono di 0,015683 Methylnaphtalene 12C10H314N1 = 142.062567 Dalton. Guardando nella valle che separa i due ioni, lì potrebbe esserci un terzo segnale (indicato dalla freccia nera) che potrebbe essere anche una 12C1013C1Hg = 142.07378 12C13C1Hg = 142.07378 oscillazione del rumore di fondo. Come facciamo a sapere se questo è un segnale di un analita che c'è Am nel campione? Dobbiamo aumentare il potere risolutivo. Passiamo da 10.000 a 32.000 (secondo 142.454 142.490 142.525 142.4700 142.4842 grafico) e riesco a separare anche questi due ioni (i picchi più a destra) che differiscono di 0,00447 Dalton. Il potere risolutivo, la risoluzione, è la caratteristica di un analizzatore di separare il numero intero alla prima, alla seconda, alla terza, ... cifra decimale. Con questi due esempi stiamo cominciando a capire il significato della parola risoluzione e qual è l'impatto e la conseguenza pratica che la risoluzione ha sui risultati che noi vogliamo ottenere. 58006 = 32000 R Methylquinolene 12C11H10 = 142.07825 142.4985
Mass Resolving Power e Resolution
Abbiamo due termini che utilizziamo: Mass Resolving Power e Resolution. Il Mass Resolving Power, il potere risolutivo, secondo la IUPAC è la capacità di distinguere due ioni che differiscono di un certo 4. Quindi, se abbiamo uno ione il potere risolutivo è la capacità di vedere questo ione ben definito rispetto ad uno che gli sta di fianco separato da un certo Am. La risoluzione è la più piccola differenza fra due ioni di uguale intensità quando la loro sovrapposizione è una piccola percentuale rispetto alla loro intensità. La risoluzione è espressa come R = m/Am. Se andiamo a consultare la IUPAC vediamo come viene definita la risoluzione nella spettrometria di massa. Ci sono 580.2 581.2 579 580 581 lons having the same nominal mass, but different chemical compositions lysine (C6H12N2O) 128.095 glutamine (C5H3N2O2) 128.059 45 40 579.3