Introduzione e Definizioni di Termodinamica, Unimore Presentazione
Slide da Unimore su Introduzione e Definizioni della Termodinamica. Il Pdf illustra i principi base della materia, definendo concetti chiave come sistema termodinamico, ambiente, contorno, stati di equilibrio e processi. Questo materiale di Fisica, adatto per l'Università, è stato prodotto per fornire una panoramica chiara e concisa.
Mostra di più21 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Introduzione e Definizioni
- Sistema Termodinamico
- Sistemi e loro comportamento termodinamico
- Unità di misura e dimensioni
- Volume specifico
- Pressione
- Temperatura
Alcune immagini nel presente documento possono essere ispirate a quanto proposto in M.J. Moran, H.N. Shapiro, D.D. Boettner, M.B. Bailey, B.R. Munson, D.P. DeWitt, Elementi di fisica tecnica per l'ingegneria, Edizione italiana a cura di M.A. Corticelli, McGrawHill, 2022, Capitolo 2
UNIMORE 1Introduzione e Definizioni 1
Sistema Termodinamico
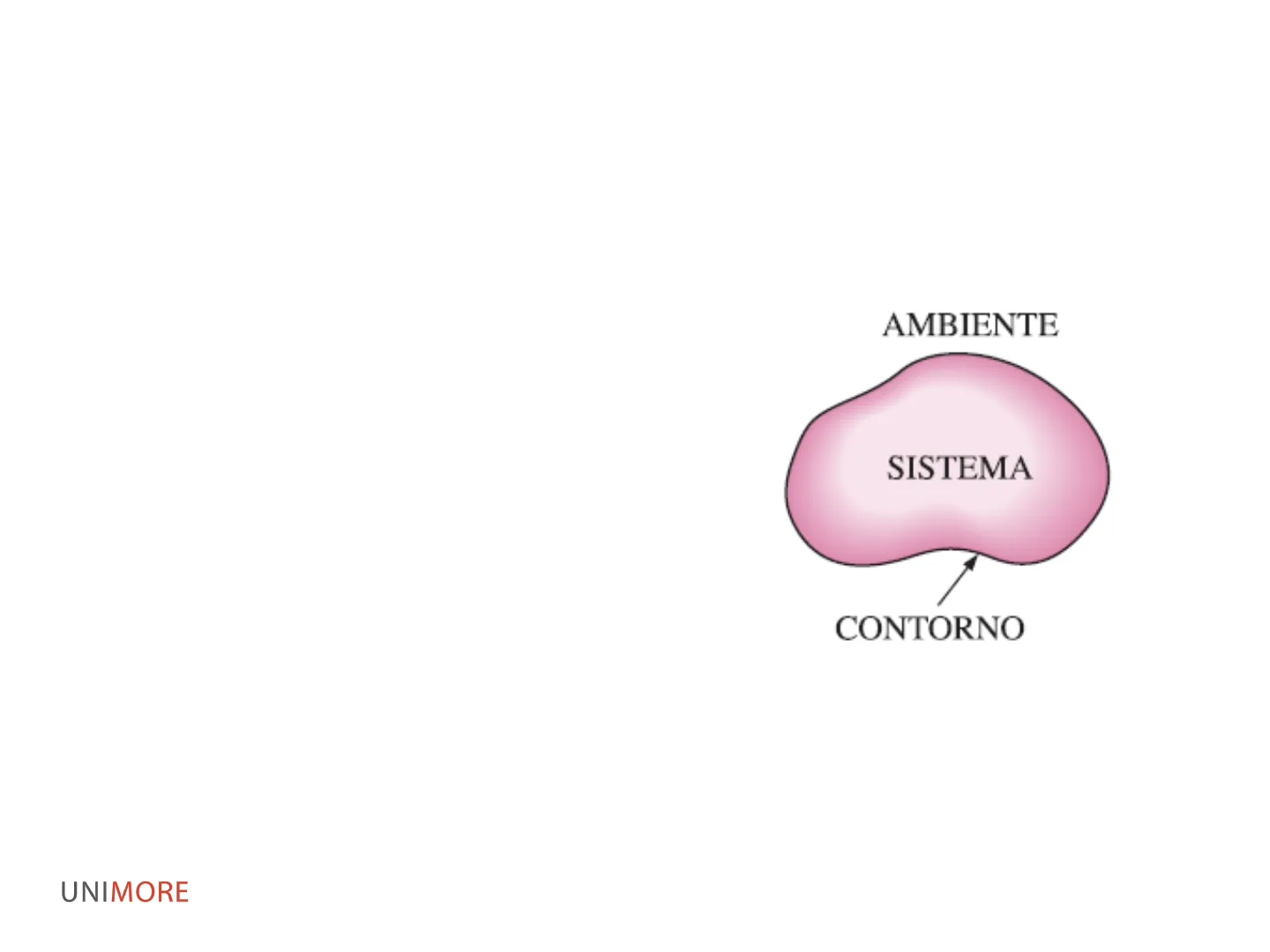
- Sistema: regione di spazio o quantità di materia che è oggetto del nostro studio
- Ambiente: regione o materia esterna al sistema
- Contorno: superficie reale o immaginaria che separa il sistema dall'ambiente
- contorno può essere fisso o mobile
- sistema può essere chiuso o aperto
AMBIENTE SISTEMA CONTORNO
UNIMORE 2Introduzione e Definizioni 2
Sistema Chiuso
- Massa invariante (massa di controllo)
- Non vi è flusso di materia attraverso il contorno
- Può essere soggetto a scambi di energia (interazioni) sotto forma di lavoro o di calore
Contorno Gas
UNIMORE 3Introduzione e Definizioni 3
Sistema Aperto
- Volume invariante (volume di controllo)
- Regione definita nello spazio attraverso il cui contorno fluisce materia.
- Di solito il volume di controllo racchiude un dispositivo a scambio di massa (compressore, turbina, ugello, ecc ... )
- contorno del VC (superficie di controllo, reale o immaginaria) può essere interessato da flussi di energia oltre che di massa
Aria in ingresso Albero motore Aria in ingresso Fumi di scarico Carburante in ingresso Carburante in ingresso Albero motore Fumi di scarico Contorno (superficie di controllo) Contorno (superficie di controllo)
UNIMORE 4Introduzione e Definizioni 4
Descrizione Termodinamica di un Sistema
- Definizione del confine
- Definizione della composizione
- Definizione dello stato
- Proprietà termodinamiche
UNIMORE 5Introduzione e Definizioni 5
Descrizione Termodinamica di un Sistema: Confine
Definizione del confine:
- Aperto / chiuso:
- Estensione di un sistema aperto: volume V [m3]
- Estensione di un sistema chiuso: massa m [kg]
- Fisso / mobile:
- pareti fisse: no scambi di energia sotto forma di lavoro - sistema meccanicamente isolato (dal proprio ambiente)
- Adiabatico / conduttivo:
- pareti adiabatiche: no scambi di energia sotto forma di calore - sistema termicamente isolato (dal proprio ambiente)
Un sistema sia meccanicamente che termicamente isolato si dice semplicemente sistema isolato. Il sistema isolato per antonomasia è l'universo
UNIMORE 6Introduzione e Definizioni 6
Descrizione Termodinamica di un Sistema: Composizione
Definizione della composizione:
- Fase: frazione di sistema chimicamente e fisicamente omogenea (in cui le proprietà variano con continuità)
- Sostanza pura: sostanza chimicamente omogenea
- Stati di aggregazione: solido, liquido, gassoso
UNIMORE 7Introduzione e Definizioni 7
Descrizione Termodinamica di un Sistema: Stato e Proprietà
Definizione dello stato: descrizione del sistema eseguita mediante i valori di quantità macroscopiche misurabili = proprietà Proprietà: una qualsiasi caratteristica macroscopica del sistema, funzione unicamente dello stato. Le proprietà si distinguono in:
- Proprietà intensive: proprietà indipendenti dall'estensione del sistema (e.g. temperatura, pressione)
- Proprietà estensive: il valore della proprietà dipende dalle dimensioni del sistema (e.g. massa, volume, energia)
- Proprietà specifiche: rapporti tra proprietà estensive (densità, volume specifico)
UNIMORE 8Introduzione e Definizioni 8
Stati di Equilibrio
- Stato di equilibrio: stato per il quale non vi sono potenziali (forze motrici) non equilibrati all'interno del sistema
- Equilibrio termico: la temperatura è uniforme entro il sistema
- Equilibrio meccanico: in ogni punto del sistema la pressione non cambia nel tempo
- Equilibrio di fase: se il sistema presenta più fasi la massa di ciascuna fase non cambia nel tempo
- Equilibrio chimico: la composizione chimica del sistema non cambia nel tempo (assenza di reazioni chimiche)
- Equilibrio elettrico: il potenziale elettrico è uniforme e non cambia nel tempo (assenza di correnti elettriche)
m = 2 kg T1 = 20°℃ V1 = 1.5 m3 m = 2 kg T2 = 20℃ V2 = 2.5 m3 (a) Stato 1 (b) Stato 2 20℃ 23℃ 32℃ 32℃ 32℃ 30℃ 35℃ 40°℃ 42℃ 32℃ 32℃ 32℃ (a) Prima (b) Dopo Sistema chiuso che tende all'equilibrio termico.
UNIMORE 9Introduzione e Definizioni 9
Processi Termodinamici
- Processo (Trasformazione): una qualsiasi modificazione dello stato del sistema
- Percorso del processo: la serie di stati attraverso i quali il sistema passa nel corso del processo
- La descrizione completa del processo prevede che sia possibile identificare gli stati iniziale e finale, il percorso e le interazioni con il contorno.
- Processo quasi-statico o di quasi-equilibrio: processo che si svolge attraverso stati (intermedi) sempre infinitamente prossimi a stati di equilibrio
- Processo ciclico (Ciclo): processo per il quale stato iniziale e finale coincidono
UNIMORE 10Introduzione e Definizioni 10
Sistema Internazionale di Unità di Misura
Il Sistema Internazionale (SI) di unità di misura è un sistema completo e coerente che definisce:
- 7 dimensioni fondamentali (massa, lunghezza, tempo, temperatura, intensità di corrente elettrica, intensità luminosa, quantità di materia) e le rispettive unità di misura
- le relazioni di definizione delle unità derivate
- i multipli e sottomultipli delle unità base
UNIMORE 11Introduzione e Definizioni 11
Sistema Internazionale di Unità di Misura: Grandezze e Prefissi
Grandezze Fondamentali del Sistema Internazionale
TABELLA 1.1 Le sette grandezze fondamentali del Sistema Internazionale (SI) e le loro unità di misura con i relativi simboli
Grandezza Unità di misura lunghezza metro (m) Massa kilogrammo (kg) Intervallo di tempo secondo (s) Temperatura kelvin (K) ampere (A) Intensità di corrente elettrica Intensità luminosa candela (cd) Quantità di materia mole (mol)
Prefissi delle Unità di Misura nel Sistema Internazionale
TABELLA 1.2 Prefissi delle unità di misura nel Sistema Internazionale
Multipli Prefissi .... ... ... .... .. ... ... .... .. 1012 tera, T 109 giga, G 106 mega, M 103 kilo, k ... .... ... ... .. 10-2 centi, c .. .... ... .... ...... 10-3 milli, m .. ... .... ... ... .... ... ........ 10-6 micro, µ 10-9 nano, n 10-12 pico, p
UNIMORE 12Introduzione e Definizioni 12
Unità di Misura e Dimensioni
- L'unità di misura di una grandezza fisica è una quantità predefinita di tale grandezza
- La misura di una grandezza fisica è data dal rapporto tra la grandezza stessa e l'unità di misura scelta
- Le grandezze derivate sono definite come combinazione delle grandezze fondamentali
- Le grandezze/dimensioni fondamentali della termodinamica sono:
- Massa [M]
- Lunghezza [L]
- Tempo [t
- Temperatura EEEE
UNIMORE 13Introduzione e Definizioni 13
Unità di Misura e Dimensioni: Formule Dimensionali
La formula dimensionale di una grandezza ne identifica la dimensione in rapporto alle dimensioni fondamentali:
- Velocità [L.t-1]
- Forza [M.L.t-2]
- Energia e lavoro [M.L2.t-2]
- Potenza [M.L2.t-3]
- Pressione [M.L-1.t-2]
- Densità [M.L-3]
UNIMORE 14Introduzione e Definizioni 14
Densità e Volume Specifico
Densità (0) Volume specifico (v)
V p = m V (kg/m3) V = = 1 r m (m3/kg)
Peso specifico (1): peso dell'unità di volume
Y = F V p = pg (N/m3)
UNIMORE 15Introduzione e Definizioni 15
Pressione
Pressione (p): forza normale esercitata da un fluido per unità di area
F1 F : forza normale agente sull'area A p = F A 1 (Pa) 1 Pa = 1 N/m2 A 1 bar = 10 Pa = 0.1 MPa = 100 kPa 1 atm = 101,325 Pa = 101.325 kPa = 1.01325 bars 1 kgf/cm2 = 9.807 N/cm2 = 9.807 × 104 N/m2 = 9.807 × 104 Pa = 0.9807 bar = 0.9679 atm
UNIMORE 16Introduzione e Definizioni 16
Pressione: Tipi di Pressione
Pressione assoluta: valore di pressione riferito al vuoto assoluto (cui corrisponde il valore zero di pressione assoluta) Pressione relativa (effettiva): differenza tra pressione assoluta e valore locale della pressione atmosferica Pressione di vuoto: valore di pressione inferiore alla pressione atmosferica
1 A Pressione relativa in 1 Pressione Pressione atmosferica locale di riferimento 2 Pressione assoluta in 1 Pressione relativa in 2 (in depressione o sottovuoto) Pressione assoluta in 2 Pressione zero
UNIMORE 17Introduzione e Definizioni 17
Temperatura
- Principio Zero della termodinamica: se due corpi sono in equilibrio termico con un terzo corpo essi sono anche in equilibrio termico tra loro
- Sostituendo il terzo corpo con un termometro, il principio zero si può riformulare come segue: due corpi sono in equilibrio termico se entrambi hanno la stessa temperatura anche se non si trovano a contatto
UNIMORE 18Introduzione e Definizioni 18
Temperatura: Equilibrio Termico
sistema C sistema A sistema B se A e B sono separatamente in equilibrio termico con C, allora (a) sistema C sistema A sistema B A e B sono in equilibrio termico fra loro (b)
UNIMORE 19Introduzione e Definizioni 19
Scale di Temperatura
Le scale di temperatura si basano su alcuni stati di una sostanza facilmente riproducibili, quali i punti di solidificazione e di ebollizione dell'acqua
- Punto del ghiaccio: miscela di acqua e ghiaccio in equilibrio con aria satura di vapore ad 1 atm (0 ℃ o 32 ºF)
- Punto di ebollizione: miscela di acqua liquida e di vapor d'acqua (in assenza di aria) in equilibrio ad 1 atm (100 °℃ o 212 ºF)
- Scala Celsius: in unità SI
- Scala Fahrenheit: in unità del sistema anglosassone
- Scala Termodinamica delle temperature: scala indipendente dalle proprietà di qualsiasi sostanza (scale Kelvin e Rankine)
UNIMORE 20Introduzione e Definizioni 20
Scale di Temperatura: Riferimenti e Conversioni
- La temperatura di riferimento originale per la scala Kelvin era il punto del ghiaccio, 273.15 K
- Attualmente si è scelto un riferimento più preciso e riproducibile, il punto triplo dell'acqua (stato al quale le tre fasi, solido, liquido, vapore, dell'acqua coesistono all'equilibrio), cui si assegna il valore 273.16 K
T(C)=T(K)-273.15 AT(C)= AT(K) T(R)=1.8T(K) T(ºF)=1.8T(C)+32 AT(OF)= AT(R) CELSIUS (°C), KELVIN (K), FAHRENHEIT (ºF), RANKINE (R)
UNIMORE 21