Piano di Clapeyron e Primo Principio della Termodinamica: Appunti
Documento di Fisica sul Piano di Clapeyron e il Primo Principio della Termodinamica. Il Pdf universitario esplora la conservazione dell'energia nei processi termodinamici, le equazioni di stato e le relazioni matematiche che descrivono questi concetti fondamentali.
Mostra di più15 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Piano di Clapeyron
Prima di addentrarci nella trattazione del Primo principio della termodinamica è opportuno introdurre uno dei diagrammi fondamentali impiegati in termodinamica: il piano di Clapeyron. Il piano di Clapeyron è un diagramma cartesiano che ha in ascissa il volume e in ordinata la pressione del gas. Come vedremo, un gas viene ad essere univocamente determinato da un punto nel piano di Clapeyron.
In presenza di una sostanza pura le equazioni che legano tre proprietà termodinamiche intensive quali la Temperatura, il volume specifico e la Pressione sono chiamate equazioni di stato. Il piano di Clapeyron può pensarsi come uno dei piani coordinati dello spazio a tre dimensioni P-v-T, nel quale un fluido è rappresentato dalla superficie di equazione f(P, v, T)=0. Se si assegnano valori prefissati T1, T2 ... Ti ... Tn alla temperatura, a questi valori corrispondono, sulla superficie del fluido, le linee rappresentative delle isoterme, proiettabili sul piano coordinato P-v. L'insieme di queste operazioni equivale a disegnare sul piano P-v un certo numero di linee aventi equazione:
f (P, v, Ti ) = 0 (1)
Una delle più note equazioni di stato più nota è quella dei gas perfetti ottenuta dagli studi di Robert Boyle e da Charles e Joseph Gay-lussac.
PV = nRUT (2)
Equazione dei gas perfetti
dove: P = pressione, [Pa] V= volume occupato dal gas, m3n = numero di moli di gas, kmol Ru = costante universale dei gas, pari a 8314 J/(kmol ·K) T = temperatura assoluta, [K]
Si rammenta che il numero di moli di una sostanza può essere ricavato dl rapporto tra la massa espressa in kg e il peso molare M e la 2 può esprimersi come:
PV = mRT o Pv = nRUT (3)
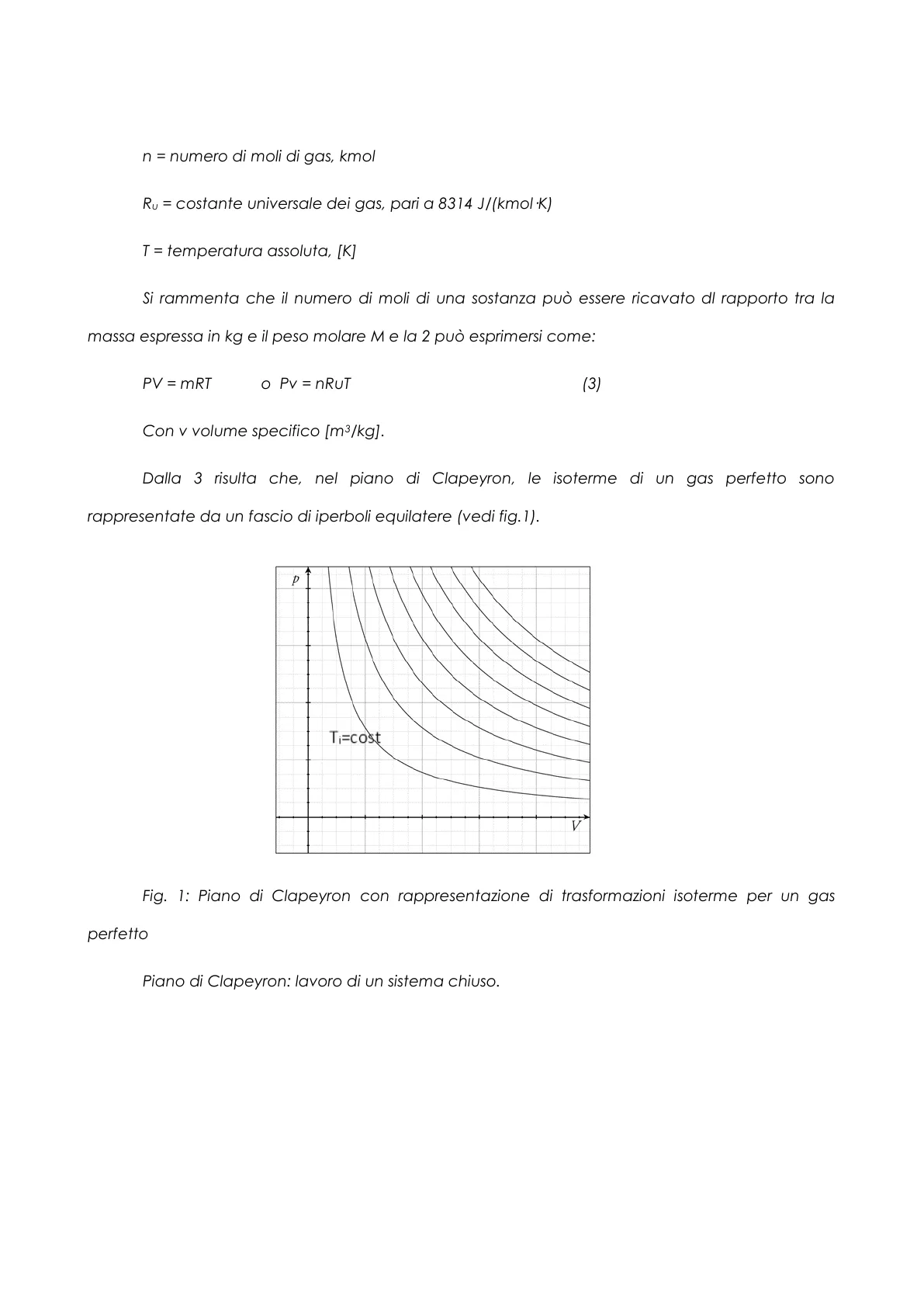
Con v volume specifico [m3/kg]. Dalla 3 risulta che, nel piano di Clapeyron, le isoterme di un gas perfetto sono rappresentate da un fascio di iperboli equilatere (vedi fig.1).
P Ti=cost V Fig. 1: Piano di Clapeyron con rappresentazione di trasformazioni isoterme per un gas perfetto
Piano di Clapeyron: lavoro di un sistema chiuso
Fx P . S dx cilindro pistone biella x Fig.2: Pistone in fase di espansione.
Si consideri un sistema chiuso quale il pistone in figura 2. Inizialmente la pressione ambiente PA è uguale alla pressione interna P, allora il pistone non si muove.
Se P aumenta lentamente (trasformazione quasi-statica spostandosi di un dx in modo reversibile:
8L = F .dx = (P .S)dx = P(S .dx) = P.dV (4)
P è lo stesso in tutto il volume del gas (stato di equilibrio).
Il lavoro reversibile in un sistema chiuso totale, in una trasformazione che parte da un punto A ad un punto B si calcola come:
LAB = ms " Pdv (5)
- Lavoro fatto dal sistema (espansione) è POSITIVO
- Lavoro fatto sul sistema (compressione) è NEGATIVOp
A B LAB O VA VB V Fig.3: lavoro scambiato da un sistema chiuso: rappresentazione grafica sul piano di Clapeyron.
Nel piano di Clapeyron il lavoro scambiato con l'esterno da un sistema chiuso è misurato dall'area sottesa dalla linea che rappresenta la trasformazione; al variare del percorso seguito per andare dallo stato A allo stato B, varia anche l'entità del lavoro assorbito o ceduto dal sistema: il lavoro non è una grandezza di stato.
In relazione all'equazione 3, il lavoro reversibile di una massa unitaria lungo una trasformazione isoterma per un gas perfetto che si porta da uno stato A ad uno stato B si può esprimere:
LARGE RT -dv B1 JAV B LAB = RT . In( V V B )
Mentre per una trasformazione ciclica (Lo stato iniziale coincide con quello finale) il Lavoro complessivo:(7)
$ Pdv = f5, Pdv-S51, Pdv p A L B V1 V2 V Fig.4: Lavoro in una Trasformazione ciclica.
Il Lavoro in un sistema può essere compiuto anche attraverso lo spostamento di elettroni (N) per effetto di una differenza di potenziale V (Forza elettromotrice). Riferendosi all'unità di tempo, la Potenza elettrica è:
L = VI (9)
con I corrente elettrica. Ne consegue che il Lavoro compiuto in un intervallo At è esprimibile come:
L = VIAt.
Si stabilisca che il simbolo del punto sopra la lettera significhi che la grandezza è derivata nel tempo( Esempio da Lavoro La potenza L).
L'equilibrio termico. Principio Zero della Termodinamica
Il principio zero della termodinamica stabilisce che, se un corpo A è in equilibrio termico con un corpo B, e il corpo B è a sua volta in equilibrio termico con un altro corpo C, allora A è senz'altro in equilibrio termico con il corpo C.
A C B Fig. 5: Dispositivo sperimentale per l'illustrazione del Principio Zero della Termodinamica.
Pur sembrando un'ovvietà il principio non può essere dimostrato a partire dagli altri principi della termodinamica, e va quindi specificato a parte. Questo principio viene utilizzato per effettuare una misura della temperatura, se viene intesa come proprietà che determina se un corpo è in equilibrio termico con altri corpi oppure no. Due corpi in equilibrio termico fra loro sono alla stessa temperatura. Sebbene sia concettualmente un'assunzione basilare, la sua funzione è stata riconosciuta dopo la formulazione e la popolarizzazione del primo e secondo principio della Termodinamica, ed è stato pertanto deciso di attribuirgli il nome di "principio zero".
Per estensione, può affermarsi che tutti i sistemi pensabili ed in equilibrio termico con il sistema C, sono in equilibrio termico fra di loro. Questo non significa che gli stati termodinamici dei sistemi menzionati siano identici, ma soltanto che fra tutti questi sistemi, comunque accoppiati, non avviene trasferimento di calore; quando ciò succede, si dice che i sistemi presentano uno stesso valore della temperatura.Il Principio Zero consente dunque l'introduzione del concetto di temperatura; ogni tecnica di misura della temperatura è basata sull'applicazione di questo Principio.
Primo Principio della Termodinamica
Il primo principio della termodinamica è essenzialmente il principio di conservazione dell'energia per i processi termodinamici. Un'analisi critica delle caratteristiche dei cicli termodinamici fu portata avanti da Mayer, Joule ed altri scienziati, a partire dagli anni 1840, con l'intento di spiegare il funzionamento delle macchine termiche a vapore. Vale la pena di ricordare che, all'epoca, non era affatto chiaro che calore e lavoro fossero due aspetti sotto i quali si presentava una stessa entità, l'energia. Anzi, il funzionamento delle prime macchine termiche, nate dall'osservazione sperimentale delle proprietà elastiche del vapore d'acqua, appariva misterioso e non era spiegato scientificamente. Furono dunque Mayer e Joule i quali, per mezzo di osservazioni sperimentali sul funzionamento di queste macchine, portarono a conclusione una lunga disputa del pensiero scientifico moderno, riguardante la natura fisica del calore, ed introdussero quei concetti generali che sono alla base del Primo Principio della Termodinamica.
Si consideri un sistema termodinamico, assoggettato a percorrere un ciclo chiuso di trasformazioni, nel corso del quale esso scambia calore e lavoro con l'esterno (vedi fig. 6). Si constata sperimentalmente che, se durante il ciclo chiuso il bilancio del calore scambiato è positivo, valendo per convenzione il segno + nel caso di calore assorbito dal sistema ed il segno - in caso contrario, allora anche la somma dei lavori scambiati dal sistema con l'esterno è positivo, valendo, in questo caso, la convenzione di assumere come positivo il lavoro compiuto dal sistema sull'esterno e negativo quello compiuto dall'esterno sul sistema. Le circostanze ora enunciate, derivanti dall'esperienza, conducono ad avanzare l'ipotesi che possa esistere un legame tra gli scambi di calore e quelli di lavoro, lungo i cicli chiusi; l'ipotesi risulta avvalorata dalle ulteriori esperienze che appresso si descrivono.Il sistema, inizialmente è nello stato K1e percorre il ciclo chiuso 1 Misurato il calore Q1 e il lavoro L1 scambiati dal sistema durante il ciclo, sia C1 il rapporto:
Q1/L1 = C1.
Venga ripetuta la misurazione per altrettanti ciclici chiusi scelti in modo arbitrario e modificando anche la posizione dello stato iniziale K1, e si considerino i valori Ci quali rapporto tra Qi/Li.
P CILCO 1 CICLO 3 CICLO 2 K1 V Fig.6: rappresentazione di trasformazioni termodinamiche chiuse sul piano P-v
Si constata che tali rapporti sono poco differenti tra di loro e la differenza è compresa nei limiti degli errori di misura, cioè:
C1 = C2 = . . .. = Cn = C (10)
La costanza dei rapporti evidenza l'esistenza di un legame tra calore e lavoro scambiato: il lavoro prodotto è legato alla quantità di calore scomparso (e viceversa) e si può ipotizzare che calore e lavoro siano forme diverse sotto le quali si presenta una medesima entità, l'energia, e che possano avvenire trasformazioni da una forma all'altra. Misurando il calore inkilocalorie e il lavoro in Joule, il rapporto C vale 1/4186; ciò significa che per ogni kilocaloria che scompare, compaiono 4186 Joule, e viceversa.
Consideriamo adesso un sistema termodinamico che percorre una trasformazione aperta, passando dallo stato iniziale A allo stato finale B. Il sistema segua successivamente due percorsi: linea 1 e linea 2 (vedi fig. 3): se si misurano il calore Q1 e il lavoro L1 scambiati seguendo linea1 e si fa il rapporto Q1/L1 = R1, ci si accorge che RI # C. Se poi si ripetono le medesime operazioni anche per Linea 2 si trova Q2/L2 = R2, con R2 #R1 #C; ossia non si evidenza nessun legame tra i rapporti lavoro- calore, essendo però legati al tipo di trasformazione seguita. Conviene allora osservare che, in base alle equazioni precedenti per i cicli chiusi si può scrivere:
Q-CL=0 (11)
P Linea 1 B Linea n Linea 2 A VFig. 3: trasformazioni diverse fra due stati A e B.
La funzione (Q-CL) ha invece valori diversi da zero se si percorre una trasformazione aperta fra uno stato iniziale A ed uno finale B; però, se si considerano i percorsi Linea1, Linea 2, ..... Linea n diversi fra loro, per andare da A a B e si calcolano le differenze:
(2.12) (QAB - ALAB )= AU1 (lungo Lin1) (QAB - AL AB )= AU2 (lungo Lin2)
ci si accorge che le differenze AUi differiscono fra loro di una quantità inferiore all'errore di misura, dunque:
AU1 = 4 U2 = = A Un = AU
Si conclude che AU dipende soltanto dallo stato iniziale e finale della trasformazione; ciò significa che l'espressione QAB - CLAB è la differenza fra i valori assunti da una grandezza di stato, di tipo estensivo, alla quale viene attribuito il nome di energia interna; cioè:
QAB - ALAB= UA - UB (13)
Si conclude che la differenza tra il calore e il lavoro scambiati nel passaggio fra due stati prefissati non dipende dalla trasformazione seguita ed è uguale alla variazione di energia interna fra i due stati (Primo Principio della Termodinamica).
Si noti che non si è definita l'energia interna, bensì una sua variazione fra due stati prefissati; perciò non si è in grado di definire il valore assoluto dell'energia interna, come si fa per altre grandezze di stato, quali pressione e volume. Per associare un valore numerico all'energia interna, si deve individuare uno stato di riferimento, per mezzo dei valori assunti da altre grandezze di stato; fissato arbitrariamente il valore numerico di U nello stato di riferimento, si può calcolare l'energia interna in qualsiasi altro stato termodinamico del sistema.