Bioquímica Enzimología: Naturaleza, historia y regulación de enzimas
Documento de Universidad sobre Bioquímica Enzimología, Grado Veterinaria. El Pdf aborda la enzimología, definiendo enzimas como catalizadores biológicos y su descubrimiento, naturaleza química, mecanismos de regulación como fosforilación y ruptura proteolítica, e isozimas, útil para estudiantes de Biología.
Ver más32 páginas
Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Bioquímica 2024-25. Enzimología. Grado Veterinaria
Tema 1: INTRODUCCIÓN
1.1 CONCEPTO DE ENZIMA
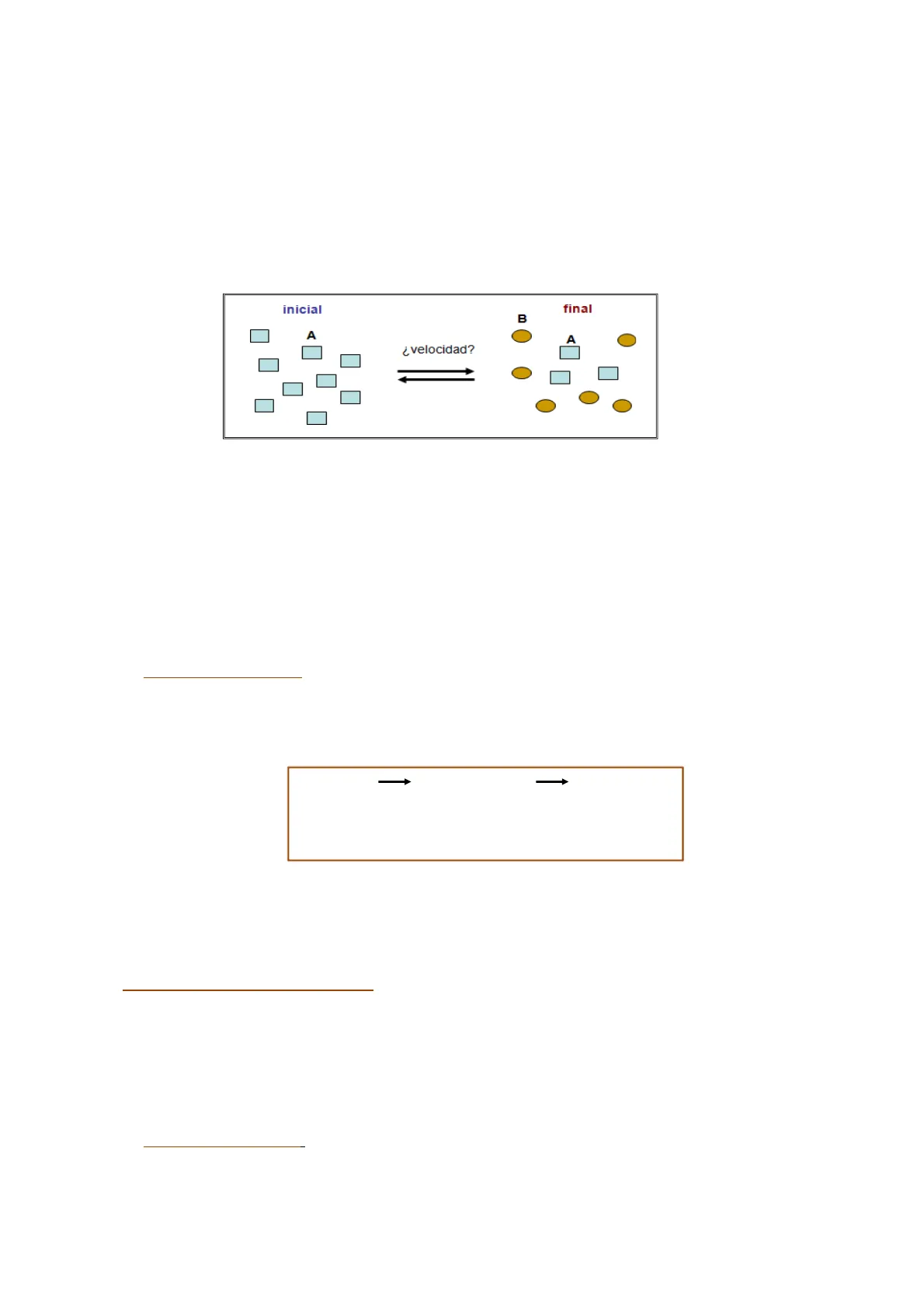
Las enzimas son los catalizadores de reacciones químicas que ocurren en los seres vivos, es decir, de las reacciones bioquímicas. Un catalizador de una reacción química es una sustancia que acelera la velocidad de la reacción.
inicial final B A A ¿velocidad?
1.2 HISTORIA
La historia de la investigación sobre las enzimas está íntimamente ligada a la historia de la Bioquímica, y esta disciplina avanzó a medida que lo hacia el conocimiento de estas moléculas. Cronológicamente y citando los aspectos fundamentales de este avance, tenemos:
Mediados del siglo XIX. Louis Pasteur, importante microbiólogo francés, "padre" de la pasteurización, es contratado por viticultores de su país para que descubriese las razones de la acidificación del vino. Llega a la conclusión de que la transformación de la glucosa en etanol la realizan catalizadores (fermentos) contenidos en la levadura.
C6H12O6 CH3CH2OH CH3COOH ácido acético D-glucosa etanol bacterias levadura (fermentos)
Según Pasteur, para que tuviese lugar la fermentación alcohólica era preciso la presencia de la levadura viva. El término enzima fue acuñado por Kuhne en 1878, y etimológicamente viene de "en la levadura".
Finales del s. XIX-comienzos del s. XX. Los hermanos Buchner trabajando con levaduras trituradas con arena (células rotas, muertas), descubren, por casualidad, que las enzimas de la fermentación alcohólica permanecen activas en ausencia del organismo vivo. Surge la Bioquímica moderna y aparece el término in vitro (en el tubo de ensayo) en contraposición al in vivo (en la célula viva).
Primer cuarto del s. XX. En este periodo es Summer el que aísla, purifica y estudia la naturaleza química de la ureasa, describiéndola como la primera enzima y atribuyéndole naturaleza proteica.
1Bioquímica 2024-25. Enzimología. Grado Veterinaria NH3-CO-NH3 2NH3 + CO2 urea ureasa (proteína)
Cerca de este periodo también Northrop (1930), aisla, purifica y determina la naturaleza química de distintas enzimas digestivas que degradan a las proteínas de la dieta (tripsina, quimiotripsina, etc.). Confirma que las enzimas son proteínas.
1.3 NATURALEZA QUÍMICA
Hasta la década de los 50 del s. XX se daba por hecho, como hemos mencionado antes, que casi todas las enzimas eran proteínas, esta afirmación ha de ser revisada cuando Cech descubrió que algunos tipos de ARN tenían capacidad catalítica sobre otros ARN. A estos enzimas de naturaleza poli-ribonucleotídica se les llamó ribozimas. No obstante, dado que la abrumadora mayoría de las enzimas son proteínas, en lo que sigue siempre nos estaremos refiriendo a las enzimas de naturaleza proteica.
Las enzimas son proteínas (recordar la excepción de los ribozimas). Están constituidas por una o varias cadenas polipeptídicas que forman una o varias subunidades, tal y como hemos visto en el tema anterior. Algunas enzimas son sólo proteína, mientras que otras contienen, además del componente proteico, uno no proteico. En el segundo caso, al total de la enzima se le llama holoenzima, al componente proteico apoenzima y al no proteico cofactor.
solo proteína inorgánico enzimas proteína + componente no proteico apoenzima cofactor coenzima (unido débilmente) orgánico holoenzima grupo prostético (unido fuertemente)
La presencia de un cofactor en una enzima indica que dicho cofactor es indispensable para la catálisis. Este cofactor puede ser inorgánico (ejemplo, Fe2+, Cu+, Zn+, K+, etc.), u orgánico. En este último caso, puede estar unido debilmente a la apoenzima, en cuyo caso se le llama coenzima, o puede estar unido fuertemente (covalentemente) a la apoenzima, llamandosele entonces grupo prostético. La mayoría de los cofactores orgánicos son o derivan de las vitaminas hidrosolubles (complejo B y vitamina C). Una vitamina es una sustancia indispensable para la vida, que un animal no puede sintetizar y que le debe de ser suministrada en la dieta.
2Bioquímica 2024-25. Enzimología. Grado Veterinaria
1.4 CATÁLISIS QUÍMICA
Para entender la catálisis enzimática es necesario recordar algunos aspectos de la catálisis química. Es preciso saber que todo lo descubierto en el mundo inanimado por la Química y por la Física es aplicable a lo que sucede en los seres vivos.
Recordemos pues, que cualquier reacción química, A + B> C + D 1 .- supone ruptura y/o formación de enlaces covalentes 2 .- procede desde un estado inicial hasta uno final llamado de equilibrio en el que no existe formación/ruptura neta de enlaces químicos y donde tampoco existe flujo (variación) neto de energía. 3 .- obedece a la ley de acción de masas y al principio de Le Chatelier, es decir, si se altera la concentración de una de las especies químicas participantes, el sistema evoluciona hasta contrarrestar ese efecto. 4 .- obedece a las leyes de la termodinámica (bioenergética en las reacciones bioquímicas): a) la energía no se crea ni se destruye, solo se transforma (1º ley). b) todo sistema (o reacción) evoluciona espontáneamente hacia un estado de máximo desorden (máxima entropía) (2º ley).
Fijémonos en la energía. Lo que determina la espontaneidad o dirección en la que discurre una reacción es la segunda ley de la termodinámica. Aunque existen diferentes formas de energía, a nosotros nos es útil un tipo: la energía libre de Gibbs (G). La energía libre de Gibbs la asumimos como aquella energía que es de calidad, es decir, que puede ser empleada para realizar un trabajo biológico. Ejemplos de trabajo biológico son: la síntesis de moléculas, el transporte activo, la contracción muscular, etc.
Una reacción como la del esquema anterior evoluciona desde un estado inicial hasta uno final, o desde la izquierda hasta la derecha, porque el contenido en G del estado inicial (Gi) es mayor que el contenido en G del estado final (Gf). Dicho de otra manera, porque el cambio de energía libre que acompaña a la reacción (AG) es menor que cero, es negativo. AG = Gf - Gi < 0. Una reacción así se dice que es exergónica o espontánea. Se entiende que la diferencia de G entre el estado final y el inicial se ha perdido en forma de energía no útil para la célula. En el caso contrario, cuando 4G > 0, la reacción es endergónica y no ocurre espontáneamente en la dirección que se ha propuesto.
Se puede demostrar que el AG que acompaña a una reacción como la planteada antes, se puede calcular a partir de la ecuación [E-1]:
AG' = AGO' + R x T x In [C]i x [D] [A]¡ x [B]i [A], [B]], [C]iy [D]; son las concentraciones iniciales de las moléculas reaccionantes AGº es el cambio de energía libre AGº' = cambio de energía libre en condiciones estándar fisiológicas R = constante de los gases = 1,98 x 10-3 Kcal /mol x °K 1 Kcal = 4,184 KJ T = temperatura absoluta = °K (°Kelvin) = 273 + ℃ 1 KJ = 0,24 Kcal ln = logaritmo neperiano = 2,3 lg (logaritmo decimal) a 25 °℃, R xT x 2,3 = 1,36 a 37 °C, R XT x 2,3 = 1,41
3Bioquímica 2024-25. Enzimología. Grado Veterinaria
cuando las condiciones iniciales son las condiciones estándar. Condiciones estándar son: concentración de 1M para cada una de las especies químicas participantes en la reacción, presión de 1 atm en el caso de que una de ellas sea un gas, y temperatura de 25 ºC.
Se puede calcular AGº si suponemos que nos encontramos en el estado final (estado de equilibrio químico de la reacción). En ese estado AG = 0, y por consiguiente,
AGº = - 1,36 x lg [C]e x [D]e [A]e x [B]e
Donde, [A]e, [B]e, [C]e y [D]e son las concentraciones de los sustratos y productos en el equilibrio. Como sabemos, la relación de concentraciones en el equilibrio ([A]e [B]e/ [C]e [D]e) es característica de cada reacción y se llama constante de equilibrio (Keq). Por consiguiente,
AGº = - 1,36 x log Keq.
Cuando tratamos de reacciones bioquímicas (que suceden en los seres vivos), más que hablar de AG, AGo y Keq, hablamos de AG', AGo' y Keq', donde la prima (') indica que se trata de condiciones fisiológicas. La condición fisiológica que se quiere especificar es el pH, por tanto, nos estamos refiriendo a que el pH en el que transcurre la reacción es el 7 (neutro) ([H+] = 10-7 M).
1.5 ESTADO DE TRANSICIÓN
En la teoría de la reacción química se admite que la transformación de una sustancia (S) en otra (P): A B, depende de una barrera energética asociada a un estado intermedio en la reacción llamado estado de transición. Esta barrera energética del estado de transición se llama energía (libre) de activación (G*). Sólo las moléculas de A que alcanzan ese nivel energético pueden convertirse en B. Intuitivamente se pueden entender que la G* del estado de transición es un indicador de que el choque entre las moléculas reaccionantes es eficaz o de que existe la adecuada distorsión en el enlace de una molécula. Naturalmente, a mayor AG+ (diferencia entre la G+ y la Gi), menor será la velocidad de la reacción, y viceversa.
A = B S =P Estado intermedio asociado a una barrera energética: energía libre de activación (G*) Estado de transición (¿) Energía libre, G AG* 'S->P AG# P->S - S JAG' P
4Bioquímica 2024-25. Enzimología. Grado Veterinaria
TEMA 2: CATÁLISIS ENZIMÁTICA
2.1 RELACIÓN ENTRE LA ACCIÓN ENZIMÁTICA Y LAS VARIABLES QUÍMICO-FÍSICAS DE UNA REACCIÓN BIOQUÍMICA
Es importante tener en cuenta, que las enzimas:
S+E ESEPE+P Como acelera una enzima la velocidad de una reacción? Estado de transición (+) Energía libre, G AG+ no cat AG# cat -ES EP S LAG P_ Reacción no cat cat 1) No modifican el equilibrio químico de una reacción, ni, en consecuencia, la constante de equilibrio. 2) No influyen en el cambio de energía libre que acompaña a una reacción. Por consiguiente, no afectan a la espontaneidad de la reacción. 3) Aceleran la velocidad de una reacción disminuyendo la energía libre de activación (G*), es decir, disminuyendo la barrera energética que deben de superar las moléculas en el estado de transición para que se produzca su transformación en otras moléculas.
2.2 EFICACIA Y EFICIENCIA DE LA CATÁLISIS
Las enzimas son catalizadoras eficaces. Es frecuente que aumenten la velocidad de la reacción miles de veces, llegando, en ocasiones, a multiplicarla por 107-1014. De un modo simplificado, una reacción catalizada por una enzima se puede expresar así:
S+E ZES E + P
De esta expresión se extrae lo siguiente: 1) Las enzimas no se modifican en el proceso de catálisis. 2) Una molécula de enzima puede transformar infinitas moléculas de sustrato (S) en producto (P). En consecuencia, las enzimas están presentas en concentraciones bajas. 3) No se producen subproductos en la catálisis, esto es, las enzimas son catalizadores eficientes.
2.3 ESPECIFICIDAD DE LA CATÁLISIS
Otra característica importante de la catálisis enzimática es la especificidad. Esta especificidad puede ser referida a la reacción, o también puede darse la especificidad de sustrato.
La especificidad de reacción es presentada por todas las enzimas. Prueba de esta especificidad nos la proporciona los distintos destinos metabólicos que puede tener la D-glucosa-6-fosfato en la célula animal: 1) D-glucosa-6-fosfato => D-glucosa + fosfato inorgánico 2) D-glucosa-6-fosfato <= > D-fructosa-6-fosfato 3) D-glucosa-6-fosfato <= > D-glucosa -1-fosfato
5