Fisiología de la Sangre: composición, funciones y hemostasia
Documento de Universidad sobre Fisiología de la Sangre. El Pdf detalla la composición y funciones de la sangre, incluyendo el plasma, proteínas plasmáticas y el proceso de hemostasia. Este documento de Biología es útil para estudiantes universitarios, abordando la hemostasia primaria y el mecanismo del tapón plaquetario.
Ver más35 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
INTRODUCCIÓN
El cuerpo humano está compuesto principalmente por agua (57%). Además, encontramos otros componentes:
- Liquido intersticial: rodea a las células y tejidos. Su composición es similar al linfa.
- Flujo vascular: incluye el plasma sanguíneo (componente principal), fase líquida de la sangre, que contiene los elementos formes y está dentro de los vasos sanguíneos.
- Fluidos transcelulares o líquido transluminal: líquidos especializados y que no están compartidos por los tejidos puesto que se situan dentro de las cavidades (LCR, humor vítreo, humor acuoso ... ).
Células Nutrientes Plasma sanguíneo S Líquido intersticial
GENERALIDADES DE LA SANGRE
La sangre es un tejido líquido, opaco y rojo. Está constituido por elementos formes suspendidos en un líquido complejo y de color amarillento denominado plasma.
- pH bastante neutro => 7,35 - 7,45
- Las proteínas que alberga le aportan viscosidad
- Sus electrolitos (iones) le dan un sabor salado
- Cuando está oxigenada su color es rojo intenso, pero si está desoxigenada es rojo granate.
- Conforma del 6-8% del peso corporal. En hombres son unos 5 o 6 litros mientas que en mujeres solo 4,5 o 5,5 litros.
- Es 4-5 veces más viscosa que el agua, debido a la presencia de células y macromoléculas Presión oncótica: presión osmótica de las proteínas plasmáticas Hematocrito: relación en % entre el volumen celular y el de la sangre. Porcentaje de sangre formado por hematíes (mujeres 38-46% y hombres 40-54%; en condiciones fisiológicas). Si bajan los hematocritos (anemia) y si suben (aumenta la viscosidad de la sangre y puede conllevar a problemas cardiovasculares). Volemia => término para determinar el volumen de sangre en el cuerpo.
FUNCIONES DE LA SANGRE
- Transporte: transporta O2, CO2, nutrientes, hormonas y productos de desecho.
- Regulación: mantiene la homeostasis. Regula el pH (sistemas tampon), temperatura, concentración de iones y de agua. La sangre es una fuente de calor y además con el sudor también regula la temperatura.
- Protección: Frente a la pérdida de sangre mediante la coagulación y frente a enfermedades.
COMPONENTES DE LA SANGRE
- Plasma: Líquido amarillento formado por un 91,5% de agua Tiene 8,5% en solutos 7% => proteínas (albúmina, globulinas, fibrinogeno y protrombina) 1,5% => electrolitos, nutrientes, enzimas, hormonas bilirrubina ...
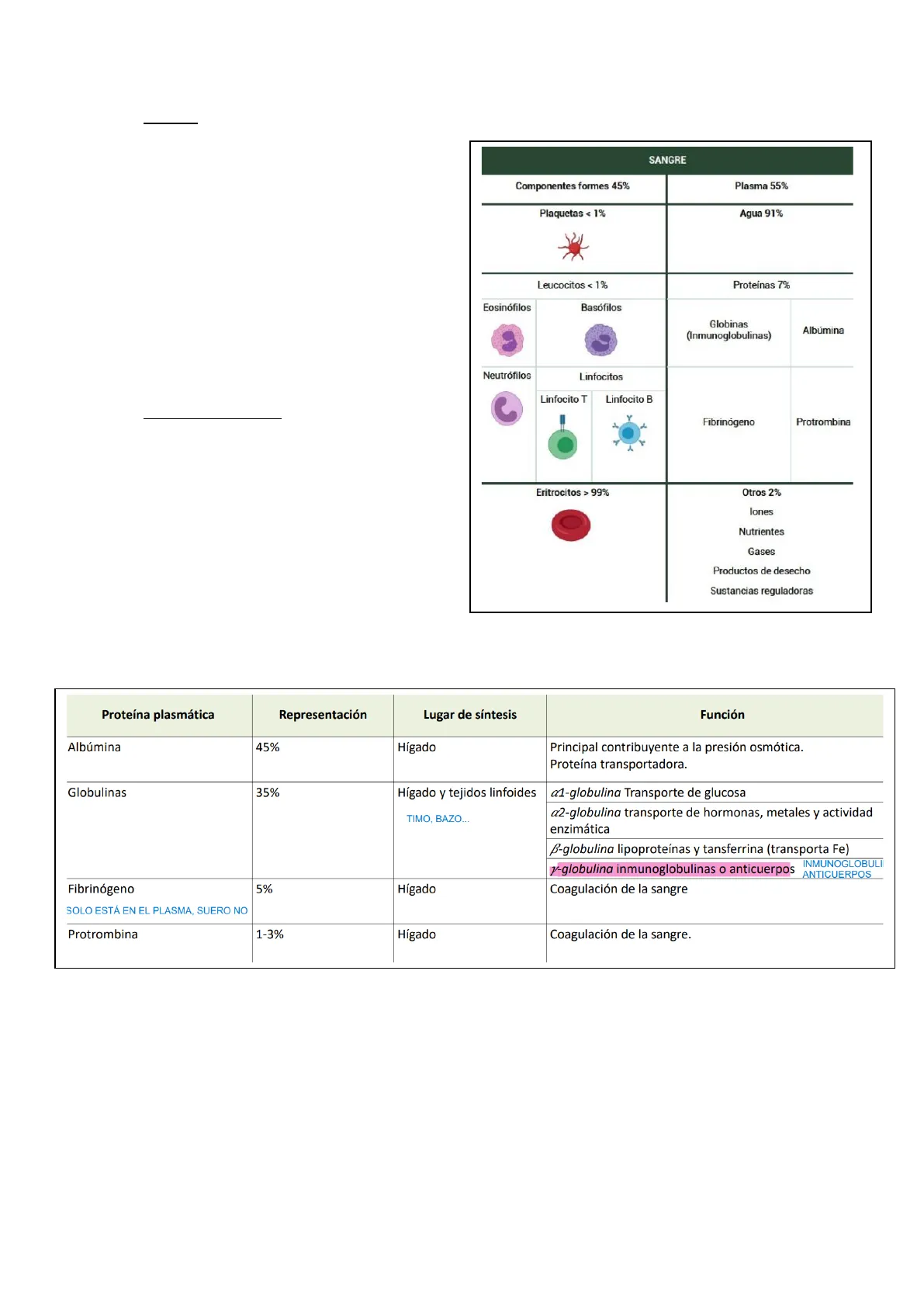
- Elementos formes: Glóbulos rojos / eritrocitos (99%) Glóbulos blancos / leucocitos y plaquetas (1%) *Los niveles de leucocitos podrían indicarnos el estado de la persona, es decir si está enfermo o no. Ya que forman parte del sistema inmunitario.
SANGRE Componentes formes 45% Plasma 55% Plaquetas < 1% Agua 91% Leucocitos < 1% Proteínas 7% Eosinófilos Basófilos Globinas (Inmunoglobulinas) Albúmina Neutrófilos Linfocitos Linfocito T Linfocito B Fibrinogeno Protrombina Eritrocitos > 99% Otros 2% lones Nutrientes Gases Productos de desecho Sustancias reguladoras
PROTEÍNAS PLASMÁTICAS
Proteína plasmática Representación Lugar de síntesis Función Albúmina 45% Hígado Principal contribuyente a la presión osmótica. Proteína transportadora. Globulinas 35% Hígado y tejidos linfoides TIMO, BAZO ... a1-globulina Transporte de glucosa @2-globulina transporte de hormonas, metales y actividad enzimática ß-globulina lipoproteínas y tansferrina (transporta Fe) INMUNOGLOBULII y-globulina inmunoglobulinas o anticuerpos ANTICUERPOS Fibrinógeno SOLO ESTÁ EN EL PLASMA, SUERO NO 5% Hígado Coagulación de la sangre Protrombina 1-3% Hígado Coagulación de la sangre. La proteína más abundante es la albúmina, seguida de las globulinas, el fibrinogeno y la protombina.
- Albumina => presión osmótica y transporte
- Globulina => inmunidad
- Fibrinogeno y protrombina => coagulación
PROTEINOGRAMA
Técnica que se utiliza en clínica en la que mediante una electroforesis (separación de proteínas según su tamaño y forma) se obtienen bandas que indican que tipo de proteína es. En función de la representación gráfica de las bandas se puede saber si hay alguna patología. Estas tienen unos valores y todo aquello que no entre en los parámetros será una anomalía. Y + Por ejemplo, si la última banda tiene una curva baja se obtiene que el paciente tiene pocos anticuerpos, bien porque está combatiendo contra alguna enfermedad o porque acaba de pasar por una.
ELEMENTOS FORMES
- Eritrocito: transporte de 02 (de los pulmones a los tejidos) y CO2 (de los tejidos a los pulmones)
- Leucocito: protege al cuerpo frente a patógenos (inmunidad)
- Plaquetas: liberan sustancias químicas que promueven la coagulación sanguínea
ERITROCITO
GENERALIDADES DEL ERITROCITO
Un hombre adulto presenta 5,4 x 10 (elevado a 6) eritrocitos/yL de sangre. Una mujer adulta presenta 4,8 x 10 (elevado a 6) eritrocitos/yL de sangre. El proceso mediante el cual se producen los eritrocitos se denomina eritropoyesis y la eritrocatersis o hemolisis hace referencia a la eliminación de los eritrocitos.
ANATOMÍA DEL ERITROCITO
Estructura de disco bicóncavo, es decir, tienen forma redonda y son más planos por el centro para así tener más facilidad para la difusión (pasan más fácilmente por los vasos). Tienen glucolípidos en la membrana plasmática responsables de los grupos sanguíneos ABO y Rh. No presentan núcleo debido a que cuando salen de la eritropoyesis ya no se pueden dividir ni modificar más y por tanto no requieren de material genético, y tampoco tienen orgánulos (en el caso de la mitocondria aún menos ya que el glóbulo rojo se encarga de transportar oxígeno y si tuviera mitocondria consumiría todo el oxígeno). No pueden reproducirse ni realizar actividades metabólicas. Contienen hemoglobina. 8 um Globinas (cadenas polipeptidicas beta) CH2 Hemo CH HC C - Hierro (Fe2*) HC-C = N C&c/CH3 N Fe -N -C C= CH2 CH2 =C CH Globinas (cadenas polipeptidicas alfa) CH2 -OOC (b) Molécula de hemoglobina (c) Hemo con hierro
FISIOLOGÍA DEL ERITROCITO
Son los responsables del transporte de O2. Cada eritrocito presenta en su interior 280M de moléculas de hemoglobina. Cada hemoglobina es una globina formada por 4 cadenas polipeptídicas (2 cadenas alfa y 2 cadenas beta) y un grupo hemo. El grupo hemo tiene en el centro un ion Fe+2 y este se une con el O2 de manera reversible (para poder soltar el oxígeno). Como cada cadena tiene un grupo hemo, en total se podrán unir 4 moléculas de oxígeno. La hemoglobina transporta el 23% del CO2 (tiene más afinidad con el oxígeno). La hemoglobina contiene la anhidrasa carbónica que cataliza la reacción entre el CO2 y el H2O formando H2CO3. La hemoglobina también regula el flujo sanguíneo y la presión sanguínea => responde la hormona óxido nítrico (NO) la cual tiene afinidad por la hemoglobina y produce una vasodilatación provocando así un aumento de tamaño y por consiguiente, del flujo sanguíneo.
HEMOGLOBINA
La hemoglobina combinada con el O2 forma la oxihemoglobina (oxígeno + hemoglobina). Esto es gracias a que el ion de hierro está en estado ferroso (Fe2+). La metahemoglobina no tiene capacidad de transportar O2. Solo puede transportar O2 el Fe+2. El ion de Fe2+ se ha oxidado estado ferrico Fe+3. Alveolus - Hemoglobin Carbon dioxide 1 2 3 1 Red blood cell Oxygen 1. Oxygen bind to hemoglobin 2. Haemoglobin in the blood carries oxygen from the lungs to rest of tissues 3. Red blood cells carries of carbon dioxide back from the tissues to the lungs Cells En resumen => el Fe+2 se oxida y cambia a Fe+3 (ya no puede transportar oxígeno), ahora pasará a ser la metahemoglobina. La hemoglobina neonatal presenta 2 cadenas gamma 2 cadenas beta (cambian los nombres de las cadenas). Los humanos, durante la vida fetal presentan una hemoglobina diferente a la de los adultos (hemoglobina fetal; HbF). Esta hemoglobina tiene mayor afinidad por el O2 => se une con mucha facilidad al oxígeno pero le cuesta más trabajo desunirla. Vista superficial -OOC CH2 HC-CEN SC=CH Vista de corte transversal (a) Forma del eritrocito C=CH HaCc-C.El grupo hemo se sintetiza en las mitocondrias, principalmente. La globina se sintetiza en los ribosomas. Se habla de hemoglobina saturada cuando está transportando todo el oxígeno que puede. Chloride shift CI >CI ...- CO2+ Hb -> Hb-CO2+O2 Carbonic anhydrase co ....... > CO2. CO. ... "> CO2 + H2O >H,CO,->HCO, + H+ HCO 4 .. O2 4 .... O2 + Hb-H+ Hb-O3< Interstitial fluid Plasma Tissue cell Red blood cell Systemic capillary wall
HEMOGLOBINA: TRANSPORTE DE O2
El O2 se transporta de dos formas disuelto en el plasma sanguíneo (2%) y unido químicamente a la hemoglobina (98%). La cantidad de O2 unida a la hemoglobina representa la saturación de la Hb. Cooperatividad de la Hemoglobina (Hb): las moléculas de Hb que ya están unidas a algún oxígeno tienen más facilidad a unirse a otro que aquellas que no se han unido a ninguno. La curva representa la afinidad que tiene la Hb para unirse al oxígeno (cuando cambie su afinidad, también lo hará la gráfica). La afinidad dentro de nuestro cuerpo cambiará según los cambios físicos y químicos que se produzcan. En la parte horizontal se representa el oxígeno disponible que hay en el medio (X) y en la parte vertical se representa el porcentaje de saturación de la hemoglobina (Y). Conforme aumenta la cantidad de oxígeno, aumentará la cantidad de saturación de la Hb. Porcentaje de saturación de la 100 Hemoglobina 50 0 50 100 PO2 (mmHg) La forma dependerá de estos factores:
- pH: cuando haya CO2 el ambiente será más ácido y, al haber un pH ácido la afinidad del oxígeno con la Hb disminuirá. Ejemplo: practicar deporte (no hay mucho CO2 y por tanto, el pH será básico => mayor afinidad de Hb con el oxígeno).
- Temperatura: Un aumento de la temperatura disminuye la afinidad de la hemoglobina por el oxígeno. Una disminución de temperatura aumentará la afinidad de la hemoglobina por el oxígeno.
- Concentración de Co2: Cuando haya poco CO2 la afinidad de la Hb tendrá que aumentar para captar oxígeno.
Efecto de Bohr: la disminución en la afinidad de la hemoglobina por el oxígeno implica una mayor liberación de oxígeno en los tejidos (esto puede ocurrir cuando hay una disminución del pH) Efecto Haldan: si la Hb-O2 disminuye podrá unir Co2. Si la H-O2 aumenta el Co2 se transportará en forma de HCO3 -. (disponibilidad de hemoglobina para poder unir o no CO2) Efecto Bohr 100- 100- 100- PCO2 20 pH 7,6 20 °℃ 80 80- 80- Pco, 40 60- `pH 7,4 60 ¥37 ℃ 9, 40 40- 40- 43 ℃ 20- 20- 20- J. Perkins MS, MFA 20 40 60 80 100 20 40 60 80 100 20 40 60 PO2 (mmHg) 80 100 Po, (mmHg) PO2 (mmHg)
HEMOGLOBINA: TRASPORTE DE CO2
En el transporte de gases no solamente se incluye la incorporación de O2 sino también la eliminación del Co2. Es esencial eliminar el Co2 o por el contrario se produce un aumento del pH. Co2+H2O <->H2CO3 <-> H+ + HCO3 (la forma mayoritaria que tiene de viajar). Este gas es producido durante la respiración celular. El 7% del CO2 se transporta por la sangre disuelto en el plasma y el 93% en el interior de los glóbulos rojos de dos formas diferentes: se hidrata y genera HCO3- (70%) o unido a la hemoglobina, cuando el O2 abandona su sitio de unión (23%).
HEMOGLOBINA: INTERCAMBIO DE GASES EN TEJIDO
La presión de CO2 en los tejidos es mayor a la de los capilares, esto permite que el CO2 difunda hasta los capilares entrando en la sangre y posteriormente en los glóbulos rojos (combinándose con la hemoglobina o formando HCO3 - y H+). En este momento se produce el efecto Bohr, al disminuir el pH y aumentar la presión de CO2, la afinidad de la hemoglobina por el O2 disminuye lo que provoca su liberación y la oxigenación de los tejidos. A medida que la hemoglobina se desoxigena, esta es capaz de c facilitar la incorporación de CO2 a la sangre. Tejido CO2 CO2 02 Endotelio capilar Plasma H2O + CO2 <> HCO3-+ H+ CO2 + HbO2 <> HbCO2+ O2 Glóbulo Rojo ₹ 60 Efectos de Pco2, PH y temperatura en la curva de disociación de O2 PCO2 80 pH 7,2