Diseños experimentales en estudios nutrigenéticos en humanos
Diapositivas sobre Diseños Experimentales en Estudios Nutrigenéticos en Humanos. El Pdf, un recurso de Biología de nivel universitario, explora la investigación original y secundaria, con un enfoque en el metabolismo de la vitamina A y la bioética en la investigación animal, incluyendo diagramas y datos experimentales.
Ver más14 páginas
Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
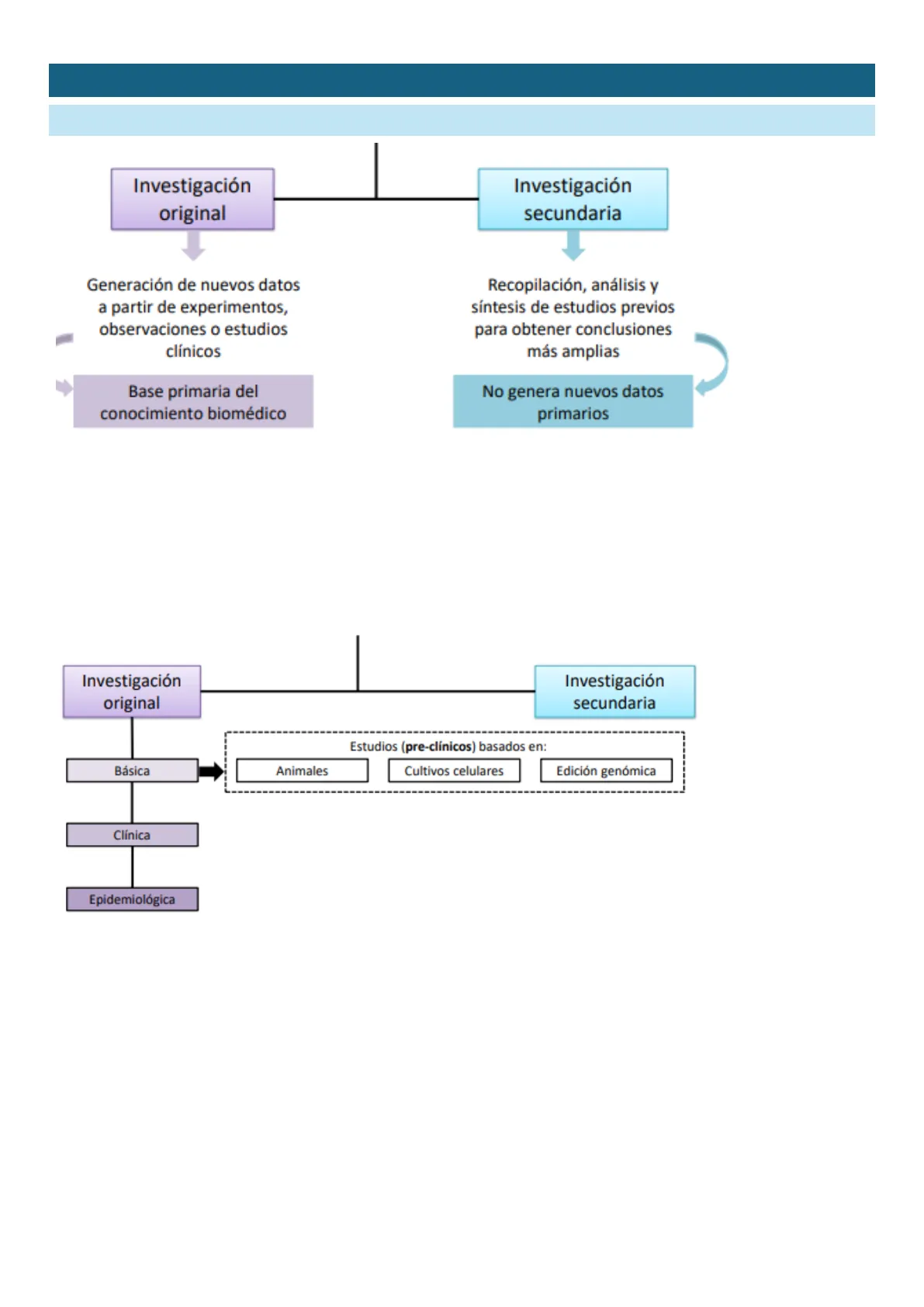
TIPOS DE ESTUDIOS EN INVESTIGACIÓN BIOMÉDICA
Investigación
original
Generación de nuevos datos
a partir de experimentos,
observaciones o estudios
clínicos
Base primaria del
conocimiento biomédico
Investigación
secundaria
Recopilación, análisis y
síntesis de estudios previos
para obtener conclusiones
más amplias
No genera nuevos datos
primarios
La principal diferencia es que en la original es la investigación que se hace sobre todo en laboratorio y
se obtiene información que no se tenia hasta este momento y la investigación se estudian y
comparan dos estudios o más sobre el mismo tema para comparar y obtener conclusiones más
amplías, pero no se obtiene información nueva.
Investigación
original
Estudios (pre-clínicos) basados en:
Básica
Animales
Cultivos celulares
Edición genómica
Investigación
secundaria
Clínica
Epidemiológica
La básica se hace sobre todo en laboratorios para obtener la base y primero en animales, se está
intentado desplazar las investigaciones en animales sobre cultivos > bioética
INVESTIGACIÓN BÁSICA
Investigación básica: estudios en ANIMALES
REGLA DE LAS 3 R
- Reemplazar siempre que se pueda llevar a cabo un método alternativo (cultivo celular)
- Reducir el numero de animales, siempre que se pueda pero que los resultados sean significativos
- Refinar en cuanto a las técnicas y procedimientos que se hace sobre los animales
Estimación 100 - 190 millones de animales de investigación (si hay que sacrificarlos que sea de la
forma en que menos sufran)
95% de los animales que se utilizan son roedores, pájaros y peces.
EE. UU. > No tienen obligación de informar del número de animales (ratas, ratones y aves) utilizados
en experimentos
Los estudios en animales (in vivo) permiten la caracterización de potenciales efectos estructurales,
funcionales y metabólicos en principales tejidos implicados en el metabolismo y la homeostasis
energética, considerando los efectos holísticos de un ser vivo
Un ejemplo: el metabolismo de la vitamina A
Forma activa vitamina A es el acido retinoico y la forma proactiva es el retinol y el betacaroteno, estos
son ingeridos por la dieta y se metabolizan en la forma activa de vitamina A
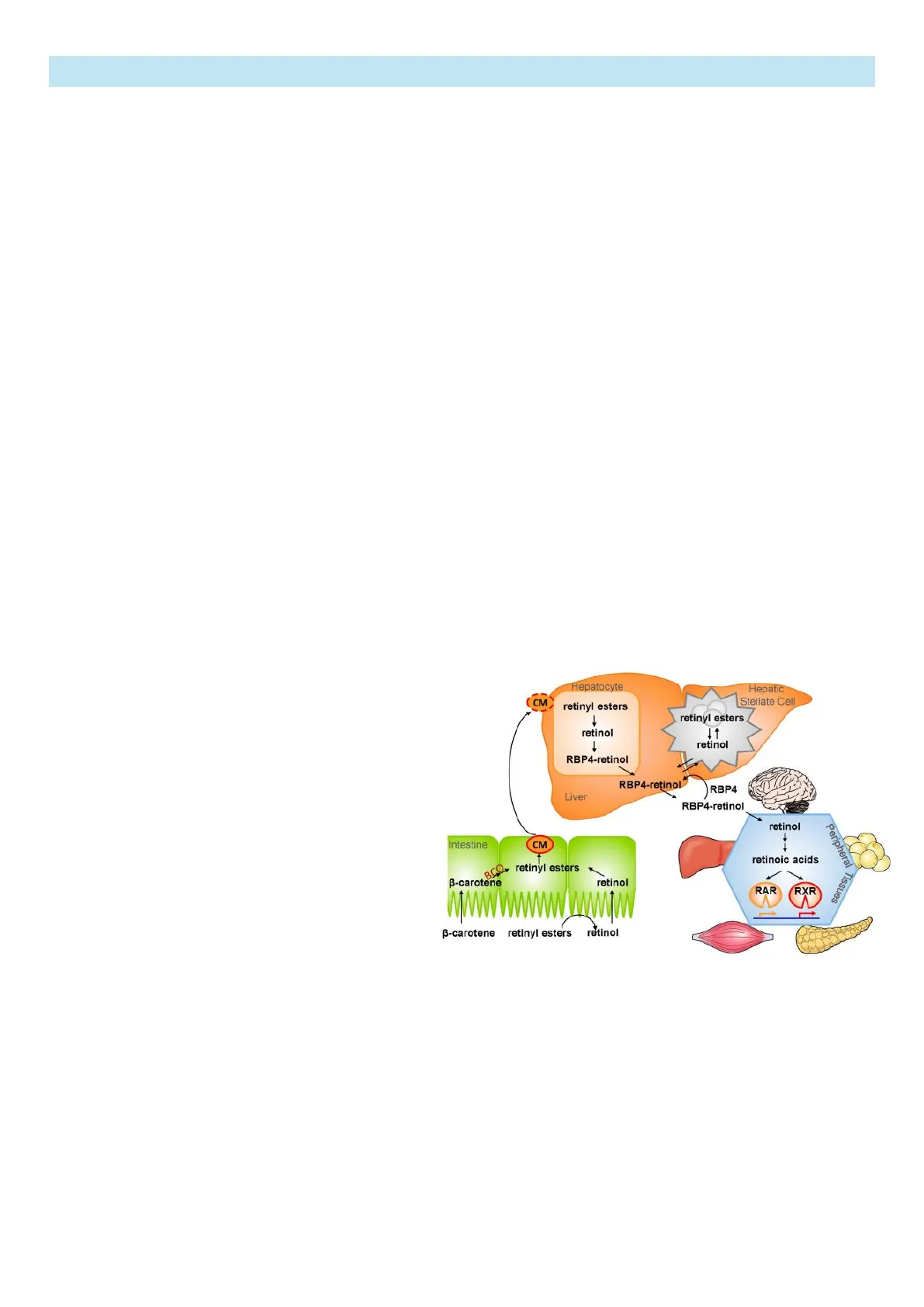
Absorción en el intestino:
· El ß-caroteno (provitamina A) es convertido en
retinol mediante la enzima BCO.
· El retinol se esterifica en ésteres de retinilo, que
son transportados por los quilomicrones (CM)
hacia el hígado.
Metabolismo en el hígado:
. Los hepatocitos almacenan la vitamina A en
forma de esteres de retinilo.
· Puede ser liberada como retinol unido a RBP4
(proteína de unión al retinol) para su transporte
en sangre.
· También puede almacenarse en las células
estrelladas hepáticas como ésteres de retinilo.
Hepatocyte
Hepatic
Stellate Cell
CM
retinyl esters
1
retinyl esters
retinol
1
RBP4-retinol
retinol
RBP4-retinol
RBP4
Liver
RBP4-retinol
retinol
Intestine
CM
retinoic acids
BC - retinyl esters
B-carotene
retinol
RAR
RXR
Peripheral Tissues
@-carotene
retinyl esters retinol
Distribución en tejidos periféricos:
· El retinol llega a los tejidos (músculo, cerebro, tejido adiposo, páncreas).
· Se convierte en ácidos retinoicos, que activan receptores nucleares RAR y RXR, regulando la expresión génica y
funciones biológicas.
Importancia biológica:
La vitamina A es clave para procesos como la visión, el crecimiento celular, la inmunidad y la diferenciación celular a
través de los receptores RAR y RXR.
IMPORTANTE ESTUDIAR VIT A
Molécula que tienen efecto durante todos los estadios de la vida, en la adultez temprana regula el
sistema inmunitario, la visión y el control de la obesidad (relación entre los niveles de vit A y el control
de los niveles de grasa visceral)
¿Cómo afecta una mutación en un gen clave (BCO2) para el procesamiento de los carotenos a
nivel metabólico?
Estudio donde una mutación en el BC02 del metabolismo de los betacarotenos
En los animales Mut acumulación de betacarotenos en el hígado debido a que no la podían
metabolizar, como consecuencia de esta mutación se da el estrés oxidativo y efectos perjudiciales.
WT
Gen
BCO2
Análisis de
los tejidos
UD OU
Mut
C
En Mut:
Acumulación de los
carotenos en los
tejidos
Estrés oxidativo
derivado de esta
acumulación
En distintas especies de mamíferos, las mutaciones en el gen BCO2
afectan la función de la proteína que descompone los carotenoides en
provitamina A. Como resultado, los carotenoides se almacenan en los
tejidos animales, lo que les confiere un color amarillo.
El genotipo de deleción al no poder metabolizar los betacarotenos se
queda en el hígado dándole ese color amarillo al tejido del animal.
Diferencias en la concentración de algunos compuestos relacionados
con el metabolismo de la vitamina A en el tejido adiposo.
7
0.5
B
B
0.4
D
B-carotene
0.3
0
00
8
2
0
1
0.1
84
0
0.0
del/del
n=30
ins/del
n=30
ins/ins
n=30
del/del
n=30
ins/del
n=30
ins/ins
n=30
ins/ins or ins/del
genotype for BOC2 gene
del/del genotype for
BOC2 gene
A
B
B
d
A
4
Lutein
3
0.2
Da
La suplementación con fructosa incremento
progresivamente la presión sanguínea sistólica hasta
niveles de hipertensión y el tratamiento con licopeno
redujo este incremento, aunque no alcanzó los valores
de los animales control.
El suplementado con fructosa la presión sanguínea
aumentaba significativamente, si los animales están
suplementados con fructosa y licopeno esta baja, pero
no esta al mismo nivel que el grupo control.
El grupo suplementado con licopeno no se ve ningún
cambio, es igual al grupo control.
1601
+C OL
+ F
-O- F-L
140-
HH *
SBP (mmHg)
*#
120-
** ******
100-
80-
0
4
8
12
Time (weeks)
Los niveles de insulina y el índice HOMA aumentaron en las ratas alimentadas con fructosa con
respecto al grupo control, y
disminuyeron significativamente en el
B
C
15-
grupo suplementado con licopeno. El
50-
T
licopeno administrado por sí solo no
10
*
alteró estos parámetros en
25
T
H*
comparación con el grupo control.
Insulin (ulU/mL)
HOMA-IR
#
5
0-
C
L
F F-L
Investigación básica: estudios en CULTIVOS CELULARES
Cultivos celulares = lineas celulares concretas, del cual conocemos sus
características.
¿Qué proteínas (genes con potenciales SNPs) intervienen en la captación de
carotenos por parte de las células?
- Células control: estándar
- Células SR-B1 o CD36: sobre-expresan la proteína BCO2
y Se añade al medio de cultivo la misma cantidad de B-caroteno '
ß-carotene uptake (%)
b
200
a
100
I
0
Control SR-BI
ß-carotene uptake (%)
240
b
160
a
80
0
Control CD36
y Análisis de la captación de ß-caroteno (por desaparición en el medio de cultivo)
Las placas de las células SR B1 y CD36 absorben más betacaroteno (la absorción se mide sabiendo
la cantidad que has puesto y posteriormente la cantidad que ha quedado y así calculas la cantidad
absorbida)
Los animales suplementados solo con
licopeno están igual que el grupo
0
C
L
control y los animales suplementados
con fructosa sufren un aumento respecto el grupo control.
¿Qué proteínas (genes con potenciales SNPs) intervienen en la captación de
carotenos por parte de las células
- Células control: estándar
- Células SR-B1 o CD36: sobre-expresan la proteína BCO2
- Células SR-B1 o CD36 + agente bloqueante
y Se añade al medio de cultivo la misma cantidad de ß-caroteno
y Análisis de la captación de ß-caroteno (por desaparición en el medio de
cultivo).
Como tenemos el agente bloqueante el betacaroteno no se absorbía igual y
el porcentaje de absorción disminuía.
ß-carotene uptake (%)
b
200
a
a
100-
0
Control
SR-BI
SR-BI
+ BLT1
240
b
a
160
a
80
0
Control CD36
CD36
+ SSO
La absorción de B-caroteno mostró un patrón dependiente
de la dosis y el tiempo en todas las líneas celulares
estudiadas.
Permite establecer un sistema óptimo de administración
de ß-caroteno a las células estudiadas, lo que proporciona
una base fiable para la evaluación del tratamiento.
120
P<0,05
100
pmol/mln cells
80
60
T
T
40
20
I
0
24h
48h
72h
10UM BC
El porcentaje de absorción va aumentando con el tiempo y
1uM BC
3UM BC
este va a depender de la cantidad de betacaroteno que le
des, no hay un umbral máximo, sino que dependiendo de la cantidad va a absorbes más o menos,
patrón dependiente de tiempo y dosis.
Los estudios en cultivos (in vitro) permiten analizar aspectos mecanísticos de procesos biológicos en
un entorno aislado (¿extrapolable?) y controlado (temperatura, dosis, atmosfera, ... )
Estos estudios están más controlados que los estudios en animales.
Potencial de traslación a humanos Variantes genéticas en dichos genes pueden influir en la
biodisponibilidad de esta vitamina
Jugar con los cultivos celulares nos da pie a estudiar el metabolismo y como influyen las variantes
genéticas sobre los niveles de betacarotenos (absorción, metabolismo ... )
Investigación básica: estudios de EDICIÓN GENÓMICA
- Se añade al medio de cultivo la misma cantidad de ß-caroteno
- Comparar los efectos diferenciales del ß-caroteno en función del SNP portador > absorción,
beneficios, dosis, efectos perjudiciales ...
B
B-carotene uptake (%) UD
INVESTIGACIÓN CLÍNICA
Investigación clínica: ensayos clínicos
Se quiere analizar el efecto de un fármaco o un compuesto.
Los ensayos clínicos de fármacos, tratamientos, o
dispositivos pueden proceder a través de 4 fases:
Investigación clínica: los ensayos y sus fases
3
1
Fase 1 -> ¿Es seguro?
2
Fase 2 -> ¿Funciona?
Fase 3 -> ¿Es mejor que lo actual?
>
4
Fase 4 -> ¿Qué pasa a largo plazo?
Fases de un ensayo clínico
FASE 1
- Evaluar la seguridad.
- Determinar la dosis
segura.
- Identificar efectos
secundarios.
FASE 2
- Evaluar la eficacia
de la prueba.
- Evaluar a fondo la
seguridad.
FASE 3
- Confirmar efectividad.
- Monitorear efectos
secundarios.
- Comparar con otros
tratamientos.
FASE 4
- Proporcionar
información adicional
después de la aprobación,
incluido el riesgo, los
beneficios y el mejor uso.
- Recolectar información.
*Aproximadamente el
70% de las drogas pasa a
la siguiente fase.
*Aproximadamente el
33% de las drogas pasa a
la siguiente fase.
*Aproximadamente el
25-30% de las drogas pasa
a la siguiente fase.
Fuente: FDA
¿Farmacogenética?
Es como la genética que tenemos también puede influir en la respuesta de los fármacos.
Cómo la variabilidad genética puede influir en la respuesta a los fármacos (eficacia y seguridad).
Gen ABCB1/MDR1 y su polimorfismo rs1045642 (C/T):
- Existen tres posibles variantes genéticas: CC, CT y TT.
- Estas variantes afectan la actividad de la glicoproteína P, alterando la absorción del tacrolimus.
Efecto de cada variante en la absorción del tacrolimus:
- Variante C (CC):
Mayor actividad del transportador > Se expulsa mas tacrolimus fuera de la celula.
Menor absorción del farmaco en el torrente sanguíneo. - Variante T (TT):
Menor actividad del transportador > Se expulsa menos tacrolimus.
Mayor absorción del farmaco. - Variante heterocigota (CT):
Actividad transportadora intermedia y absorción variable.
Importancia clínica: Dependiendo del genotipo del paciente, la eficacia y seguridad del tacrolimus
pueden variar, por lo que es relevante en la medicina personalizada para ajustar dosis y evitar
toxicidad o falta de efecto.