Dispensazione di alimenti speciali, presidi per diabete e stomizzati
Documento da Università su dispensazione alimentazione speciale, presidi per il diabete, dispositivi per incontinenti e stomizzati. Il Pdf esplora aspetti normativi e logistici di tali prodotti, con riferimenti a decreti legislativi e regolamenti europei, utile per lo studio universitario.
Mostra di più15 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Dispensazione di Prodotti Differenti dai Farmaci
Dispensazione alimentazione speciale, presidi per il diabete, dispositivi per incontinenti e stomizzati Parliamo oggi quindi di dispensazione di prodotti differenti dai farmaci.
Nel decreto legislativo 219 del 2006 ci sono 13 capitoli e ognuno va a parlare di qualcosa del farmaco e lo norma in maniera attenta.
La definizione giuridica di medicinale è ben espressa in questo decreto, il quale è stato emanato in attuazione alla direttiva europea 83 del 2001 e successive direttive di modifica, relativa ad un codice comunitario concernente i medicinali per uso umano.
Il testo si divide in 160 articoli suddivisi in XIII capitoli, oltre ai due allegati. Ogni sezione o titolo è relativa ad uno specifico argomento: titolo III immissione in commercio, IV produzione/ importazione, V etichettatura e foglio illustrativo, VI classificazione die medicinali ai fini della fornitura, VII distribuzione all'ingrosso dei medicinali, VIII pubblicità, IX farmacovigilanza, X disposizioni speciali sui medicinali derivati dal sangue o dal plasma fi umani e suoi medicinali immunologici, XI vigilanza e sanzioni, XII ulteriori disposizioni, XIII disposizioni finali.
Sulla voce distribuzione all'ingrosso dei medicinali si va a parlare di quella che è la logistica del farmaco, cioe l'insieme delle attività organizzative, gestionali e strategiche che governano nell'azienda i flussi di materiali e delle relative informazioni dalle origini presso i fornitori fino alla consegna dei prodotti finiti ai clienti e al servizio post-vendita. (AILOG: associazione italiana della logistica). Ovviamente in ognuna di queste fasi c'è anche di mezzo il farmacista.
Negli anni è stata pienamente riconosciuta l'importanza di questa funzione aziendale tanto da essere ad oggi considerata fra le maggiori leve strategiche per il conseguimento di alti livelli prestazionali e di performance economica.
Logistica del Farmaco e Ruolo del Farmacista
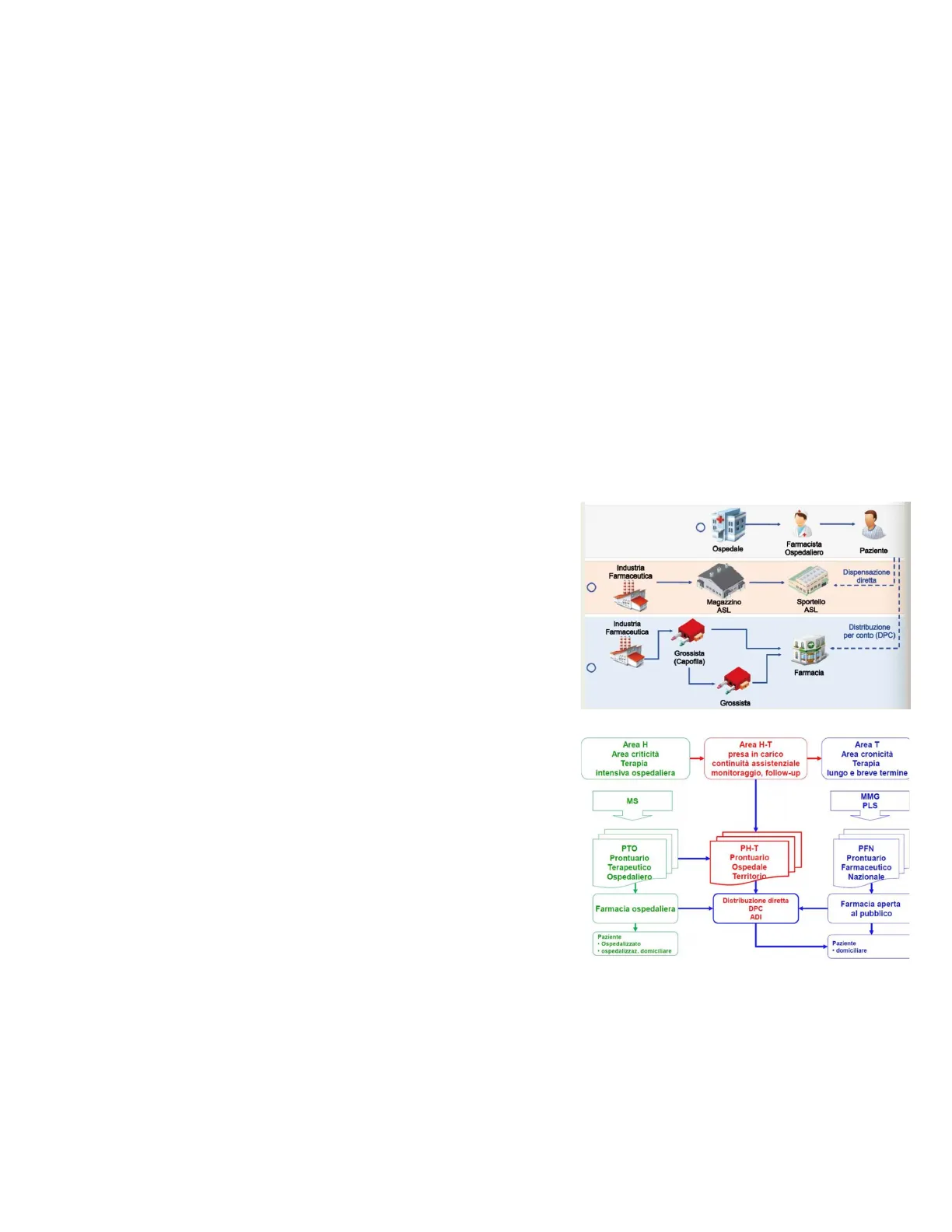
Ospedale Farmacista Ospedaliero Paziente Industria Farmaceutica Dispensazione | diretta O Magazzino ASL Sportello ASL Industria Farmaceutica Distribuzione per conto (DPC) Grossista (Capofila) O Farmacia Grossista Area H Area criticità Terapia intensiva ospedaliera Area H-T presa in carico continuità assistenziale monitoraggio, follow-up Area T Area cronicità Terapia lungo e breve termine MS MMG PLS PTO Prontuario Terapeutico Ospedaliero PH-T Prontuario Ospedale Territorio PFN Prontuario Farmaceutico Nazionale 1 1 Distribuzione diretta DPC ADI Farmacia aperta al pubblico Paziente · domiciliare Farmacia ospedaliera Paziente · Ospedalizzato · ospedalizzaz. domiciliare
Dispositivi Medici: Definizione e Normativa
I dispostivi medici secondo il decreto legislativo 46 del 97 emendato con il decreto legislativo 37 del 2010 e la direttiva europea 93/42 emendata nel 2007, sono qualunque strumento, apparecchio, impianto, software, sostanza o altro prodotto, utilizzato da solo o in combinazione, compresi gli accessori, tra cui il software informatico per il corretto funzionamento, destinato dal fabbricante ad essere impiegato nell'uomo a scopo di:
- Diagnosi, prevenzione, controllo, trattamento o attenuazione di una malattia, di una ferita o di un handicap
- Studio o sostituzione o modifica dell'anatomia o di un processo fisiologico - Intervento sul concepimento
Il dispositivo medico non esercita l'azione principale, nel o sul corpo umano, con mezzi farmacologici o immunologici o mediante processo metabolico, ma la sua funzione pu essere coadiuvata da tali mezzi.
Quindi vediamo proprio che la storia del farmaco parte nello stabilimento produttivo, poi si hanno i vari depositi e si parla in questo caso di trasporto dei farmaci primario, poi si hanno le piattaforme e transit point, distributori (grossisti, ospedali e farmacie) e infine il paziente finale e in questo caso si parla di trasporto secondario. Sia i farmaci che i vari prodotti di cui parleremo oggi sono entrati nella DPC
Distribuzione per Conto (DPC)
La distribuzione per conto (DPC), in forte crescita negli ultimi anni, consiste nella gestione di farmaci realizzata dal farmacista per conto del SSN, la cui normativa di riferimento è il Decreto legislativo 405 del 2001 e che prevedono: accordi specifici tra Regione e le Farmacie territoriali e limitatamente ai medicinali che richiedono il controllo continuo del paziente presso le strutture del SSN, secondo il prontuario P-HT e/o specifichi elenchi definiti dalla Regione.
I medicinali oggetto degli accordi sono di proprietà delle aziende sanitarie del SSR e il prezzo di rimborso è uguale a quelle dell'onorario di dispensazione.
Il cittadino nella continuità assistenziale puo attingere da HT tramite DPC o ADI, cioe assistenza domiciliare.
Classificazione Nazionale dei Dispositivi Medici (CND)
Abbiamo varie classificazioni di dispositivi medici: quella nazionale dei dispositivi medici o CND è una delle principali, è stata definita nella prima versione con il Decreto Ministeriale del 22 settembre 2005, è la classificazione italiana che raggruppa i dispositivi medici (DM) in categorie omogenee di prodotti destinati ad effettuare un intervento diagnostico terapeutico.
La prima versione della CND non prevedeva al suo interno i dispositivi medico diagnostici in vitro, i quali vennero introdotti successivamente con il Decreto Ministeriale del 20 febbraio 2007. Nel corso degli anni si sono susseguite una serie di revisioni della CND, fino ad arrivare alla più recente del 13 marzo 2018
In particolare questa classificazione divide i dispositivi medici in base alla categoria diagnostica terapeutica e poi la divisione in classe di rischio, da quella a minor rischio a quella a maggior rischio.
Dipende dalla destinazione d'uso indicata dal fabbricante e va attribuita sulla base delle regole di classificazione dell'Allegato IX del DLgs 24 febbraio 1997, n 44. Le classi sono divise in: classe I, Is, Isa, IIb e III.
Nuovi Regolamenti Europei sui Dispositivi Medici
Poi si hanno i nuovi regolamenti europei: Regolamento (UE) 2017/745 del Parlamento europeo e del Consiglio, del 5 aprile 2017, relativo ai dispositivi medici, che modifica la direttiva 2001/83/CE, il Regolamento (CE) N. 178/2002 e il Regolamento (CE) N. 1223/2009 e che abroga le direttive 90/385/CEE e 93/42/CEE del Consiglio.
Regolamento (UE) 2017/746 del Parlamento europeo e del Consiglio, del 5 aprile 2017, relative ai dispositivi medico-diagnostici in vitro e che abroga la direttiva 98/79/CE e la decisione 2010/227/UE della Commissione.
Il regolamento europeo viene applicato da subito in europa e si danno 3 anni per far si che tutti i paesi membri si adeguano.
Quindi in particolare questi due regolamenti parlano proprio di dispositivo medico e di dispositivo medico diagnostico in vitro e hanno portato a molte modifiche, di codici ecc. e si crea anche una banca dati europea, per migliore la tracciabilità.
Elementi Chiave dei Regolamenti Europei
Vedendo quindi gli elementi principali di questi regolamenti abbiamo: maggiore chiarezza nello scopo della legislazione europea, maggior controllo degli Organismi Notificati da parte delle Autorità competenti e dell'Unione europea, rafforzamento del ruolo e delle attività degli Organismi Notificati, maggiore chiarezza delle responsabilità di fabbricanti, rappresentanti autorizzati (mandatari), importatori, distributori, banca dati europea contenente informazioni sui dispositivi medici presenti nel mercato europeo, migliore tracciabilità dei dispositivi medici (UDI: Unique Device Identification system), maggiore dettaglio dei requisiti per la valutazione clinica, adattamento delle regole al progresso scientifico e tecnologico, migliore coordinamento fra Autorità competenti in materia di sorveglianza e vigilanza del mercato e allineamento delle legislazione europea alle linee guida internazionali per favorire l'integrazione dei mercati.
Nuova Definizione di Dispositivo Medico
In particolare con questo regolamento varia anche la definizione di dispositivo medico: qualunque strumento, apparecchio, apparecchiatura, software, impianto, reagente, materiale o altro articolo, destinato dal fabbricante a essere impiegato sull'uomo, da solo o in combinazione, per una o più delle seguenti destinazioni d'uso mediche specifiche:
- diagnosi, prevenzione, monitoraggio, previsione, prognosi, trattamento o attenuazione di malattie,
- diagnosi, monitoraggio, trattamento, attenuazione o compensazione di una lesione o di una disabilità,
- studio, sostituzione o modifica dell'anatomia oppure di un processo o stato fisiologico o patologico,
- fornire informazioni attraverso l'esame in vitro di campioni provenienti dal corpo umano, inclusi sangue e tessuti donati, e che non esercita nel o sul corpo umano l'azione principale cui è destinato mediante mezzi farmacologici, immunologici o metabolici, ma la cui funzione pu essere coadiuvata da tali mezzi. Si considerano dispositivi medici anche i seguenti prodotti:
- dispositivi per il controllo del concepimento o il supporto al concepimento,
- i prodotti specificamente destinati alla pulizia, disinfezione o sterilizzazione dei dispositivi di cui all'articolo 1, paragrafo 4, e di quelli di cui al primo comma del presente punto
Livelli Essenziali di Assistenza (LEA)
Noi farmacisti eroghiamo questi dispositivi, prodotti grazie al decreto del 2017 che ha aggiornato i LEA.
I Livelli essenziali di assistenza (LEA) individuano le prestazioni e i servizi che il Servizio Sanitario Nazionale (SSN) è tenuto a fornire a tutti i cittadini, gratuitamente o dietro pagamento di una quota di compartecipazione (ticket), attraverso le risorse pubbliche raccolte mediante la fiscalità generale (tasse); essi sono approvati con Decreto del Presidente del Consiglio dei Ministri (DPCM).
I Livelli essenziali di assistenza(LEA): definiscono le attività, i servizi e le prestazioni garantite ai cittadini con le risorse pubbliche messe a disposizione del Servizio sanitario nazionale; descrivono in maniera dettagliata le prestazioni e le attività già precedentemente incluse e quindi conformate come livelli essenziali di assistenza; ridefiniscono e aggiornano gli elenchi delle malattie rare e delle malattie croniche e invalidanti che dannodiritto all'esenzione dal ticket; aggiornano i nomenclatori della specialistica ambulatoriale e dell'assistenza protesica, introducendo prestazioni tecnologicamente avanzate ed escludendo eventuali prestazioni obsolete.
L'Articolo 1 del decreto si occupa proprio di questo ma è molto ampio come decreto, parla sia di salute della collettività sanitaria pubblica, assistenza distrettuale (articolo 8) e quella ospedaliera (articolo 9).
Fanno parte dei LEA anche gli allegati in cui si elencano i prodotti erogabili con limiti massimi e le modalità di erogazione.
Assistenza Integrativa e Nomenclatore Tariffario
Dei LEA ci interessa l'articolo 10 sull'assistenza integrativa in cui rientra l'erogazione a carico del Sistema sanitario dispostitivi medici (cateteri, sacche, cannule, pannolini, siringhe e medicazioni, presidi per diabetici) e alimenti speciali (prodotti senza glutine, latti artificiali, prodotti proteici ecc) per specifiche categorie di pazienti
Il Nomenclatore tariffario è il documento emanato e periodicamente aggiornato dal Ministero della Salute che stabilisce la tipologia e le modalità di fornitura di protesi e ausili a carico del Servizio Sanitario Nazionale.
Secondo l'articolo 10 nell'ambito dell'assistenza integrativa il SSN garantisce prestazioni che comportano l'erogazione dei dispositivi medici monouso, dei presidi per diabetici e dei prodotti destinati ad un alimentazione particolare nei limiti e con le modalità degli articoli successivi
Attraverso l'assistenza integrativa è possibile acquisire a carico del Sistema Sanitario regionale ausili e presidi medici con varie finalità: Presidi per incontinenza, Ausili per autodeterminazione glicemia per diabetici e microinfusori, Prodotti dietetici per celiachia, Prodotti dietetici per assistiti nefropatici, con intolleranze alimentari, latte per bambini nati da madri sieropositive per HIV, Prodotti dietetici per assistiti affetti da malattie metaboliche congenite, Presidi per stomizzati, Prodotti dietetici per nutrizione artificiale domiciliare e Ossigenoterapia domiciliare.
Ruolo del Farmacista e Presidi per Incontinenza e Stomizzati
Il farmacista ha sempre maneggiato questi prodotti ma con l'avvento della farmacia di servizi avremo un incremento di ingresso di questi prodotti in farmacia e quindi dobbiamo conoscerli attentamente sia per informare il paziente, sia per il modo di erogazione di SSN e sia per le informazioni sul prodotto stesso, modalità uso ecc. Il paziente fa affidamento sul farmacista come primo riferimento. Dialoga sempre di piu anche con professionisti che circondano la farmacia dei servizi e quindi il medico di medicina generale, specialista e infermiere.
Ci concentriamo soprattutto sui presidi per l'incontinenza e stomizzati.
Nell'allegato 2 del cPCM del 2017 è prevista l'erogazione di dispositivi medici monouso dal SSN: tracheostomizzati e laringectomizzati (cannule tracheali), ileostomizzati, colostomizzati e urostomizzati (sacche per stomia,paste e pomate protettive, ecc.), che necessitano permanentemente di cateterismo (cateteri e sacche di raccolta, ecc.), affetti da grave incontinenza urinaria o fecale cronica e agli assistiti affetti da patologia cronica grave che obbliga all'allettamento (ausili assorbenti e ausili per incontinenza, medicazioni per lesioni da pressione o di altra natura).
Per l'erogazione dei dispositivi è necessaria e sufficiente (non è necessario il riconoscimento di invalidità) la certificazione del medico specialista e la prescrizione medica; i dispositivi sono acquistati e forniti agli assistiti, nelle quantità indicate dal medico entro il limite massimo fissato dall'allegato 2, direttamente dalla Asl o per il tramite di altri servizi territoriali (farmacie, sanitarie, ecc.)
Incontinenza: Cause e Soluzioni
In questo allegato si parla di inconentenza, cioe impossibilità di trattenere urine e feci per disfunzioni anatomiche e funzionali degli sfinteri della vescica o del retto; anche piccole fughe di urina possono infatti dare disagio sociale e un problema igienico (irritazioni cutanee e infezioni) e quindi compromettere la qualità di vita. Ovviamente nel caso in cui ci sia insuccesso della terapia farmacologica o chimica, l'ausilio per l'incontinenza è l'unica via in cui possiamo andare incontro.
Se c'è qualche disfunzione a livello renale si parla di incontinenza e quindi di disturbi della minzione.
Fughe d'urina, anche piccole, costituiscono un problema igienico e una causa di disagio sociale che può compromettere in misura rilevante la qualità della vita. L'incontinenza urinaria colpisce più frequentemente il sesso femminile (tra il 10 e il 30 %), ma si calcola che una percentuale variabile tra il 2 e il 10% della popolazione maschile presenti delle perdite di urina. Fortunatamente esistono delle soluzioni, che si diversificano in relazione alle cause che sottostanno alla incontinenza stessa.
L'incontinenza, vera e propria sindrome geriatrica, presenta tra i fattori di rischio le modifiche fisiologiche legate all'età, le comorbilità, i farmaci assunti e soprattutto le alterazioni funzionali. In particolare l'incontinenza fecale è causata da importanti problemi in sede rettale, o da patologie del sistema nervoso, come paraplegia o demenza.
Quando la vescica deve essere svuotata, i nervi di questo organo inviano un segnale al cervello e noi avvertiamo l'urgenza di urinare. Una volta raggiunto il luogo preposto, il nostro cervello invia un messaggio al grosso muscolo della vescica, il detrusore, spingendolo a contrarsi per espellere l'urina dalla vescica. Allo stesso tempo, il cervello ordina al muscolo sfintere che mantiene chiusa la vescica e ai muscoli del pavimento pelvico