Gli equilibri chimici: reazioni e grado di avanzamento in Chimica
Slide sugli equilibri chimici. La Presentazione esplora come le reazioni raggiungono l'equilibrio, introducendo la costante di equilibrio e il quoziente di reazione. Questo documento di Chimica, adatto per l'Università, illustra anche il grado di avanzamento e il verso di svolgimento delle reazioni.
Mostra di più32 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Gli equilibri chimici
Le reazioni chimiche non vanno a completamento ma si arrestano quando la composizione della miscela di reazione corrisponde all'energia libera minima. Tale composizione è descritta dalla costante di equilibrio, caratteristica della reazione e dipendente solo dalla temperatura. La ragione per la quale dobbiamo conoscere la composizione della miscela di reazione all'equilibrio è che essa ci dice quanto prodotto possiamo ricavare dal processo. Per controllare il rendimento di una reazione dobbiamo comprendere il fondamento termodinamico dell'equilibrio chimico e l'influenza esercitata da condizioni quali la pressione e la temperatura sulla posizione dell'equilibrio.
- Reazioni che proseguono fino a completezza Entro i limiti imposti dal reagente limitante nel corso della reazione i reagenti si trasformano completamente nei prodotti. A + 2 B -> 2 C + D B C concentrazioni D A 0 tempo
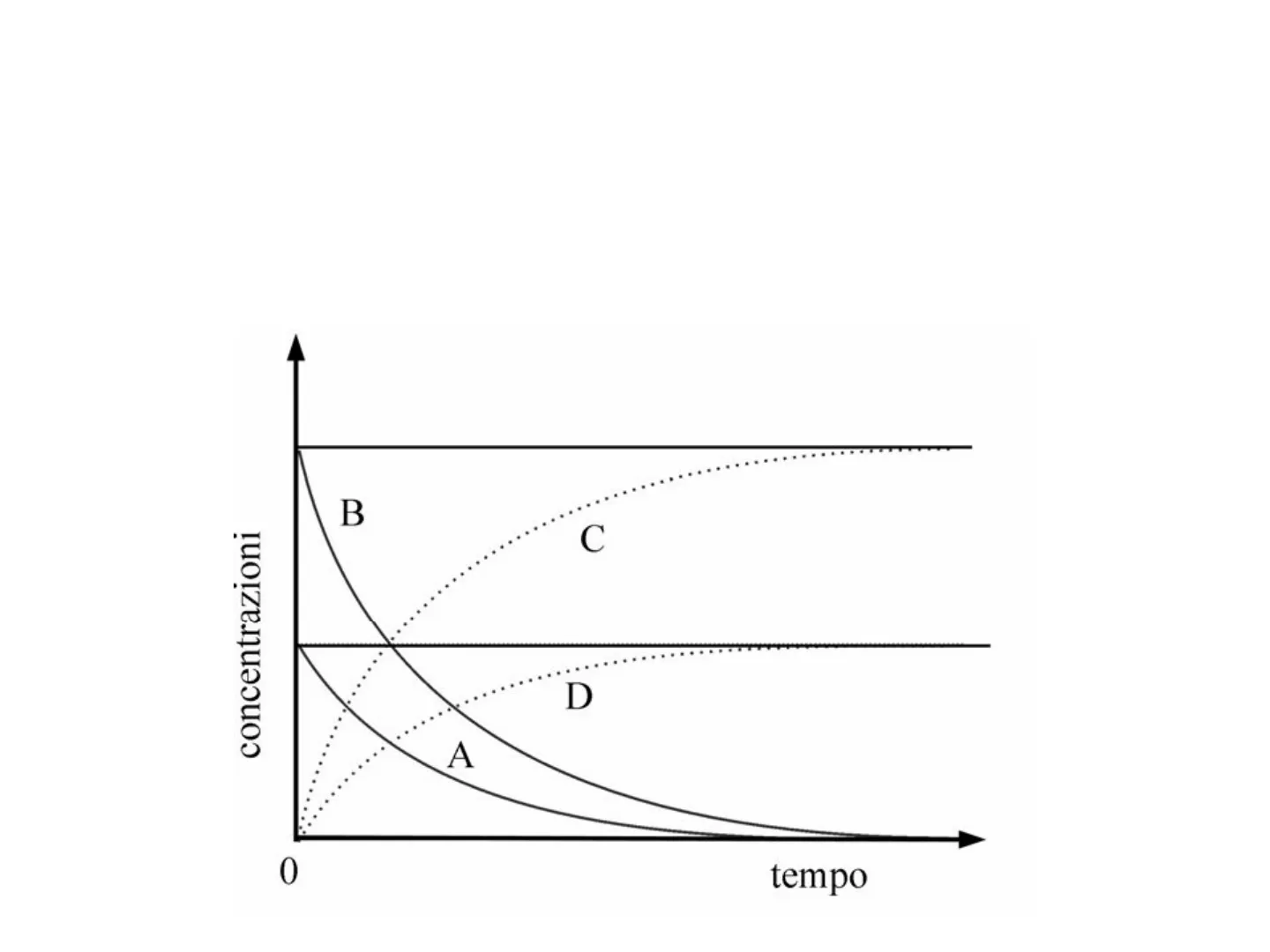
- Reazioni che proseguono fino a raggiungimento dell'equilibrio La trasformazione dei reagenti nei prodotti è parziale e prosegue solo fino al raggiungimento di una condizione di equilibrio chimico. B concentrazioni C A D 0 tempo All'equilibrio le concentrazioni dei reagenti e dei prodotti rimangono indefinitamente costanti nel tempo.
Equilibrio dinamico
La reazione è reversibile in quanto procede sia in senso diretto A + 2 B -> 2 C + D sia in senso inverso 2 C + D -> A + 2 B Alla condizione di equilibrio il numero di moli di ciascun reagente che scompare nel decorso della reazione diretta (dai reagenti ai prodotti) è uguale a quello delle moli dello stesso reagente che si riforma nel medesimo tempo in seguito al decorrere della reazione inversa (dai prodotti ai reagenti). Quello che si instaura è, dunque, un equilibrio chimico dinamico e viene indicato nel seguente modo: reazione diretta A + 2 B reazione inversa 2 C + D
N2 (g) + 3H2 (g) 2NH3 (g) Concentrazione molare -> H2 (reagente) NH3 (prodotto) N2 (prodotto) N2 (reagente) NH3 (reagente) (a) Tempo (b) Tempo Sintesi Concentrazione molare -> H2 (prodotto) Decomposizione
Legge di azione di massa
Lo stato di equilibrio è caratteristico di ogni reazione di equilibrio ed è regolato da una relazione nota come legge d'azione di massa, o legge dell'equilibrio chimico o legge di Guldberg e Waage (1864). 2SO2 (g) + O2 (g) 2SO3 (g) Essi prepararono 5 miscele di composizione iniziale differente dei 3 gas e determinarono la pressione parziale dei gas una volta raggiunto l'equilibrio a 1000 K. K = (PS03/Pº)2 (PS02/Pº)2(PO2/Pº) = costante Pj = pressione parziale del componente j Pº = 1 bar, pressione standard A temperatura e mezzo di reazione costanti, il rapporto tra il prodotto delle pressioni parziali all'equilibrio delle sostanze prodotte nella reazione, elevate ai rispettivi coefficienti stechiometrici e il prodotto delle pressioni parziali all'equilibrio dei reagenti elevate ai rispettivi coefficienti stechiometrici è costante. aA(g) + bB(g) cC(g) + dD(g) (Pc)"(PD)ª K = (PA)ª(PB)b Ogni Pj (pressione parziale del componente j-esimo) va inteso come Pj/Pº Nota: le concentrazioni che compaiono nella relazione sopra sono quelle all'equilibrio. Va precisato che per una data reazione l'equilibrio viene raggiunto a partire da qualsiasi composizione della miscela iniziale.
Equilibri eterogenei
Quando sono presenti reagenti e/o prodotti in fasi condensate (liquidi o solidi) come nel caso seguente: CaCO3(s) 4 CaO(s) + CO 2(g) K = P / Pº CO2 Si è constatato sperimentalmente e giustificato termodinamicamente che i liquidi e i solidi puri non devono figurare in K. Queste regole empiriche possono essere riassunte introducendo il concetto di attività a, della sostanza j. Le attività (a) sono delle concentrazioni (o pressioni) effettive riferite ad una concentrazione (o pressione) standard. Le costanti di equilibrio termodinamiche sono adimensionali.
Sistemi ideali
Per sistemi ideali (gas a bassa pressione e soluzioni diluite) possiamo ignorare le interazione tra le molecole purchè ricordiamo che le nostre relazioni sono solo approssimate. Valgono le seguenti relazioni: Gas ideale a = p/pº Solidi e liquidi puri a = 1 Soluzioni Solvente ag = 1 Soluti in soluzioni diluite a. = [j]/C° = [j] Co= 1 M
Costanti di equilibrio termodinamiche
Costante di equilibrio definita in funzione delle attività. aA + bB ~> CC + dD acaD a .. b a AUB cd K = Per un gas reale a = Y;(P /Pº) Per una soluzione reale a = Y (C/Cº) Le attività servono per tenere conto dei gas reali e delle soluzioni reali, laddove hanno importanza le interazioni intermolecolari.
Origine termodinamica della costante di equilibrio
aA + bB + cC + dD L'energia libera di reazione di un particolare momento della trasformazione è data differenza tra l'energia libera molare dei prodotti e quella dei reagenti alla pressione parziale o alla concentrazione che essi assumono in quel punto, ponderata dai coefficienti stechiometrici intesi come numero di moli AG, = > nGm (prodotti) - > mGm(reagenti) AGT = (cGm(C) + dGm(D) - aGm(A) - bGm(B) L'energia libera molare parziale di una sostanza J è definita dalla relazione: Gm(J) = Gm(J) + RTIn aj AG,=(cGm(C)+dG_(D) - aG_(A) - bG __ (B) + RT In (ac)"(ap)d (aA)ª(aB)b (ac)"(ap)d AGT = AGO + RT In (aA)ª(aB)b
Variazione energia libera di reazione con la composizione
AG reaz = AGO reaz + RT In m a a MUN ... 1 a b a aB ... m quoziente di reazione n Q = a aa a a MY N b AB Si può prevedere in quale direzione la reazione è spontanea (reazione diretta o reazione inversa), o se si trova in condizioni di equilibrio, a temperatura e pressione costanti tre casi AG reaz <0 AG reaz .. >0 AG reaz =0
Equilibrio
Energia libera di Gibbs, G AGO AG<0 AG=0 AG>0 Reagenti puri Prodotti puri Avanzamento della reazione
ΔΕ = 0 reazioni all'equilibrio -AG 0 reaz = RT In Qequilibrio = RT In KO equilibrio -AGO = RT In Ku reaz equilibrio ¥0 AGO T reaz Kº equilibrio = exp RT
Grado di avanzamento della reazione
Reagenti Prodotti K=10-3 K=1 K=103 K < 10-3 : l'equilibrio favorisce i reagenti 10-3 < K < 103 : l'equilibrio non favorisce fortemente né i reagenti né i prodotti K > 103 : l'equilibrio favorisce i prodotti
Verso di svolgimento della reazione
Supponiamo che la miscela di reazione contenga concentrazioni arbitrarie. Come facciamo a stabilire se essa tende a formare altro prodotto oppure a decomporre questo nei reagenti? [C]C[D]ª Q = [A]ª[B]b Le concentrazioni non sono quelle di equilibrio ma di un momento qualunque della reazione Per stabilire se una particolare miscela di reazione e prodotti tende a fornire questi ultimi o meno, confrontiamo Q con K
I prodotti tendono a decomporsi nei reagenti I reagenti tendono a formare i prodotti Q Q K Q Reazione all'equilibrio
- Se Q > K, le concentrazioni o le pressioni parziali dei prodotti sono troppo grandi ( o quelle dei reagenti troppo piccoli) perché sussista l'equilibrio.
- Se Q < K, la reazione tende a formare i prodotti.
- Se Q = K la miscela possiede la composizione di equilibrio e non ha tendenza a modificarsi in un verso o nell'altro.
Costante di equilibrio in funzione della concentrazione molare dei gas
a A + b B + ... m M + n N+ ... K = (PM / Pº)™ (Py / Pº)" (P& / Pº)ª (PR / Pº)b pm pn Pº = 1 bar K = C (CM /c°)™(CN /Cº)" C 1 C M- N pª pb A- B C m n MUN = [M][N]" co = 1 M (cA/C°)ª(CB / cº)b a b C AB Le costanti K, e K sono legate tra loro da relazioni che possono essere ricavate ricordando la legge generale dei gas PV = n RT ; p = [i] RTm PMPN ... K = a PAPB .. . b [M] (RT)"[N]" (RT)" [A](RT)ª[B] (RT)" ... (m+n ... )-(a+b ... ) - [A][B]B ... K = K . (RT) m+n)-(a+b) 4v Δν = η prodotti - n reagenti . .. (RT)
Utilizzazione delle costanti di equilibrio
Esempio: Calcolo concentrazioni all'equilibrio
Esempio: Calcolare la concentrazione all'equilibrio di A e di B quando si sciolgono 0.60 mol di A in 1 L di soluzione. A B Kc = 0.80 A B Inizio 0.60 0 variazione -x +X equilibrio 0.60-x X K = C [A] [B] =0.80 = x 0.48-0.80 . x = x 1.80 · x = 0.48 0.60- x x = 0.27
Esempio: Calcolo Kc
Esempio: Calcolare la Kc per l'equilibrio B A sapendo che le [A] e [B] all'equilibrio di A e di B sono: [A ] = 0.33 M e [B] = 0.27 M K = [B] [A] 0.33 0.27 =1.2
Esempio: Calcolo Kp e Kc
Esempio:In un reattore del volume di 6.0 L e alla temperature di 600℃ vengono introdotte 3.96 mol di CO e 1.98 mol di H2O. CO + H2O CO2 + H2 Raggiunto l'equilibrio nel reattore sono presenti 1.20 mol di H2. Calcolare Kp e Kc della reazione a 600℃. Kp = P pCO2 . pH2 pCO . pH2O Kc= C [CO2] .[H2] [CO] .[H2O] Kp = Kc(RT)Av e poiché Av = O Kp = Kc All'equilibrio avremo: CO2 + H2 CO + H2O Inizio 3.96 1.98 0 0 variazione -1.20 -1.20 +1.20 +1.20 equilibrio 2.76 0.78 1.20 1.20 [H2]=[CO2]= 1.20 (mol) 6.0 (L) [CO]= 2.76 (mol) 6.0 (L) [H20]= 0.78 (mol) 6.0 (L) Kc = (1.2/6.0)2 (2.76/6.0) (0.78/6.0) = 0.67 Kp = Kc = 0.67
Risposta dell'equilibrio alla variazione delle condizioni esterne
Principio di Le Chatelier (o dell'equilibrio mobile) Un sistema chimico all'equilibrio, se soggetto a variazioni dall'esterno, tende a reagire spostando l'equilibrio in modo da opporsi alla variazione esterna a A + b B c C+d D con Kc= [C][D]/[A][B]b
Aggiunta di reagenti
1) Aggiunta di reagenti: Aggiungiamo, p.es. [A] Q = [C][D]/[A] + [A]ag)[B] < Kc Se Q < Kc, la reazione tenderà a spostarsi verso destra, in modo da consumare parte di [A], e formare un po' più di [C] e [D], fintanto che, con altri valori di concentrazione, Q = Kc .
Aggiunta di prodotti
2) Aggiunta di prodotti: Aggiungiamo, p.es. [C] Q = [C]+ [C]ag)[D]/[A][B] > Kc Se Q > Kc, la reazione tenderà a spostarsi verso sinistra, in modo da consumare parte di [C], e formare un po' più di [A] e [B], fintanto che, con altri valori di concentrazione, Q = Kc .
Rimozione di prodotti e reagenti
3) Rimozione di prodotti: Q < Kc, reazione verso destra 4) Rimozione di reagenti: Q > Kc, reazione verso sinista
Compressione della miscela di reazione
Un equilibrio in fase gassosa è in grado di rispondere alla compressione, cioè alla diminuzione del volume del contenitore. Secondo il principio di Le Chatelier la composizione tenderà a mutare nel senso che rende minimo il conseguente rialzo di pressione. Ad esempio: I2(g) = 2I(g)
- La reazione diretta fa aumentare il numero di particelle gassose e quindi la pressione
- Quella inversa fa diminuire il numero di particelle gassose e quindi la pressione
- Se comprimiamo il volume l'equilibrio si sposta verso sinistra cercando di far diminuire la pressione