Metabolismo delle proteine: catabolismo e ricambio proteico
Slide da Università su Metabolismo delle Proteine. Il Pdf, una presentazione, esplora il metabolismo delle proteine, il loro catabolismo e il continuo ricambio proteico, con schemi visivi per facilitare la comprensione. Questo materiale di Biologia è utile per lo studio autonomo.
Mostra di più32 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
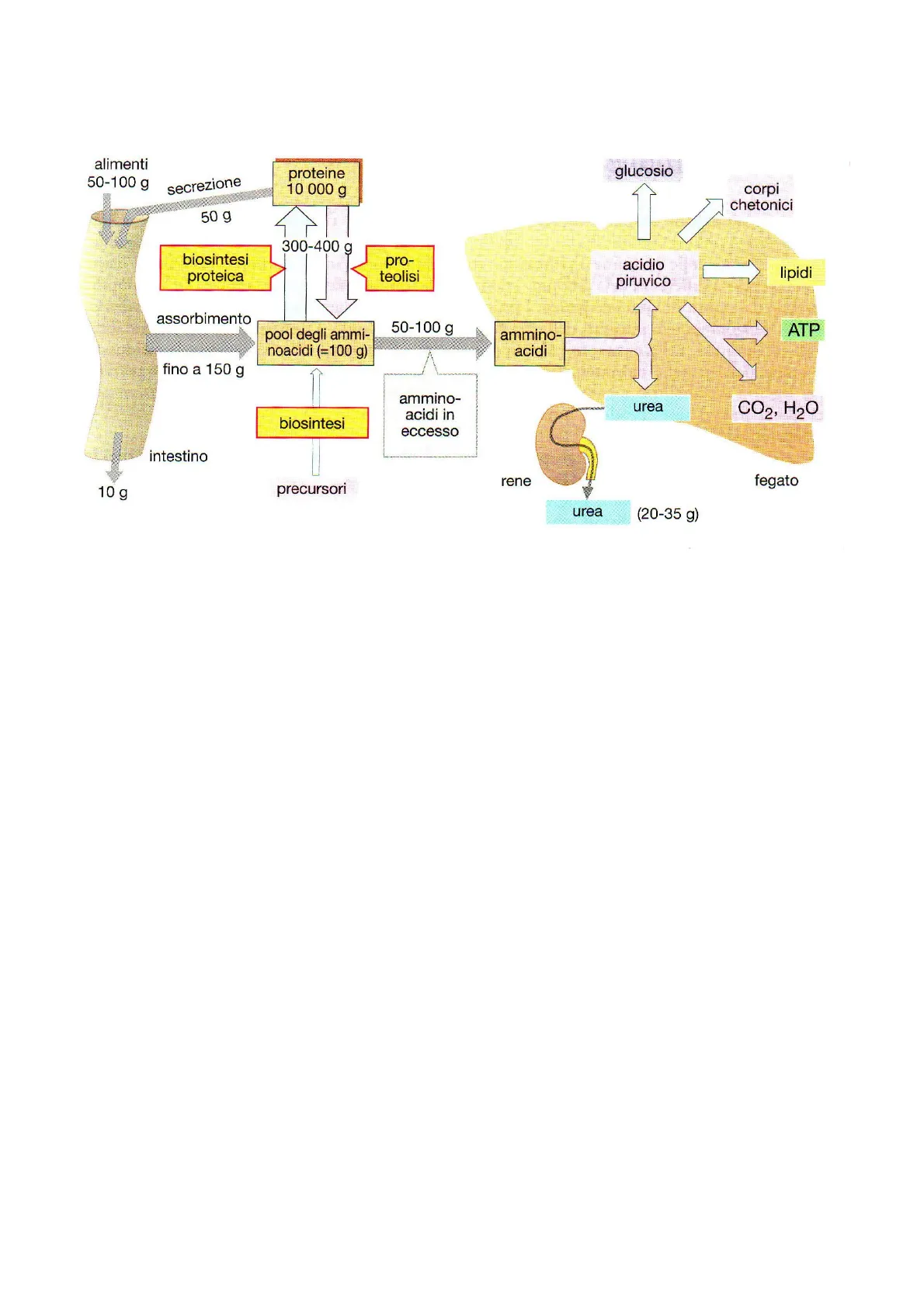
Metabolismo delle proteine
alimenti 50-100 g glucosio secrezione proteine 10 000 g corpi chetonici 50 g 300-400 g biosintesi proteica pro- teolisi acidio piruvico lipidi C ATP pool degli ammi- noacidi (=100 g) ammino- acidi fino a 150 g N biosintesi ammino- acidi in eccesso urea CO2, H2O intestino rene fegato 10 g precursori urea (20-35 g) assorbimento 50-100 g
Catabolismo delle Proteine
- Componenti degli alimenti
- Digerite nello stomaco e poi nel duodeno a dipeptidi e amminoacidi
- Lo scopo della digestione delle proteine è l'idrolisi dei legami peptidici per generare amminoacidi liberi
- Digestione delle proteine non avviene nella bocca
- AA sono assorbiti attraverso un sistema trasporto: simporto attivo con il sodio
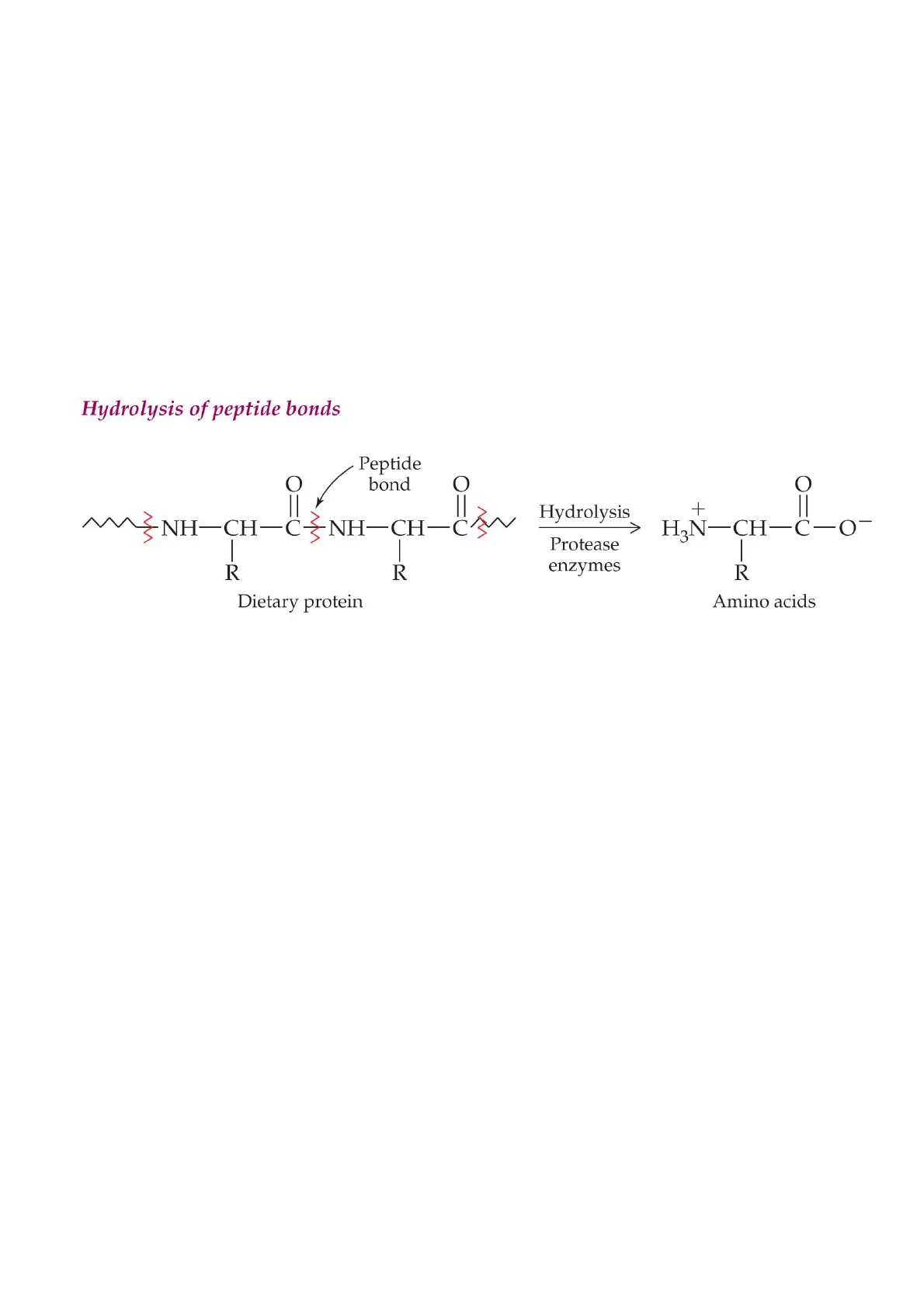
Idrolisi dei legami peptidici
Hydrolysis of peptide bonds Peptide bond O o + A NH-CH-CNH-CH-C' - Protease enzymes 1 R R R Dietary protein Amino acids II Hydrolysis H3N-CH-C-O-
Proteolisi (digestiva extracellulare)
- Idrolisi del legame peptidico
- Nell'intestino dell'uomo sono presenti diverse proteasi secrete da diversi organi digestivi:
- Dallo stomaco: pepsina
- Dal pancreas: chimotripsina, tripsina, carbossipeptidasi
- Dall'intestino tenue: peptidasi intestinali, aminopeptidasi
Con l'eccezione della lipasi linguale e dell'amilasi salivare tutti gli enzimi digestivi vengono secreti in forma di zimogeni Perché cosi tanti enzimi per la stessa funzione?
- Massimizzare il processo di digestione
- Non è mai completo
Digestione e assorbimento delle proteine
lume intestinale spazio luminale enterocita capillare polipeptidi orletto a spazzola denaturazione 1 pepsina aminoacidi aminoacidi Na+ & Na+ ATP Na+/ K+ ATPasi Na+ ADP 3 H+ 5 tripsina, chimotripsina, elastasi, carbossipeptidasi E co-trasportatore H+-dipendente aminoacidi 2 oligopeptidi endopeptidasi aminopeptidasi dipeptidasi dipeptidasi tripeptidasi 6 fase: gastrica pancreatica intestinale assorbimento 4
Digestione delle proteine: 6 fasi
- Idrolisi gastrica del legame peptidico;
- Digestione da parte delle proteasi pancreatiche nel lume dell'intestino tenue;
- Idrolisi degli oligopeptidi da parte di peptidasi dell'orletto a spazzola degli enterociti;
- Ulteriore digestione dei di- e tri-peptidi da peptidasi citoplasmatiche nell'enterocita;
- Metabolismo degli AA negli enterociti;
- Trasporto degli AA attraverso la membrana basolaterale e invio al sangue portale e quindi al fegato
H+ dipeptidasi tripeptidasi
Digestione delle proteine
L'assorbimento di molecole proteiche intatte avviene raramente nell'adulto ma è più frequente nel neonato. Gli anticorpi materni arrivano intatti grazie anche alla presenza nel latte di inibitori di peptidasi e vengono assorbiti. Questo spiega i fenomeni allergici a cui vanno incontro i neonati non nutriti con latte materno e il meccanismo di trasferimento delle difese anticorpali dalle nutrici al neonato.
(a) Gastric glands in stomach lining Parietal cells (secrete HCI) Chief cells (secrete pepsinogen) Stomach Gastric mucosa (secretes gastrin) Pancreas Pepsinogen - pepsin Pancreatic duct (b) Exocrine cells of pancreas Rough ER pH 7 Zymogen granules Zymogens -> active proteases Collecting duct (c) Villi of small intestine - Villus Small intestine Intestinal mucosa (absorbs amino acids) Low pH
Digestione delle proteine
Le cellule parietali e adelomorfe/principali secernono i loro prodotti (HCl e Pepsinogeno) in risposta all'ormone gastrina HCI nello stomaco (pH 1-2) denatura le proteine Pepsinogeno, è attivato dal pH acido e produce la pepsina Pepsina è stabile a pH 1-2, idrolizza alcuni legami peptidici Il polipeptide passa nell'intestino tenue, dove il pH è circa 7-8. Proteasi come (tripsina, chimotripsina e carbossipeptidasi) completano la digestione
Ghiandole gastriche e cellule esocrine
(a) Ghiandole gastriche sulla superficie dello stomaco - Cellule parietali (secernono HCI) Cellule adelomorfe (secernono pepsinogeno) Mucosa gastrica (secerne gastrina) pH acido Stomaco - ormone Pepsinogeno-pepsina (b) Cellule esocrine del pancreas Pancreas Reticolo endoplasmatico ruvido pH 7 Dotto collettore Granuli di zimogeno Zimogeni - proteasi attive (c) Villi dell'intestino tenue Dotto pancreatico Intestino tenue Villo - Mucosa intestinale (assorbe gli amminoacidi)
Fase gastrica
- Succo gastrico :
- pH 1-3 (HCI 0,2-0,5%)
- 97-99% acqua
- Mucina
- Sali inorganici
- Enzimi (pepsina, rennina) dalle cellule principali
La secrezione di H+ è un processo attivo mediato dalla H+,K+,ATPasi (cellule parietali) PEPSINA (8 isoforme) prodotte dalle cellule gastriche, sotto forma di zimogeno. Autoattivazine pH acido . RENNINA importante nei bambini poiché essendo coinvolta nella coagulazione del latte (fa precipitare la caseina in presenza di Ca++) ne rallenta il passaggio nell'intestino. -> È assente nell'adulto
Trasporto dei protoni nello stomaco
Cellula della mucosa gastricą Stomaco: Trasporto netto: VCISO l'esterno FIGURA 9.52 La H+,K+-ATPasi delle cellule della mucosa gastrica media il trasporto dei protoni nello stomaco. Gli ioni potassio vengono riciclati tramite un sistema di cotrasporto associato K+/CI -. L'azione di queste due pompe risulta in un trasporto netto di H+ e Cl- nello stomaco.
Fase pancreatica e intestinale: zimogeni
Aminoacidi nel duodeno Cellule endocrine del duodeno Colecistochinina intestino crasso (colon) Enterociti intestino tenue Enteropeptidasi Tripsinogeno Tripsina Proelastasi Elastasi Procarbossi- peptidasi Carbossi- peptidasi Chimotripsinogeno Chimotripsina Prolipasi Lipasi OKLS
Enzimi digestivi: origine, attivazione e prodotti
Origine Zimogeno/ Enzima Attivazione Substrato Prodotto finale Stomaco Pepsinogeno/pepsina pH 1-2, autoattivazione Proteine Peptidi Pancreas Tripsinogeno/tripsina Enteropeptidasi (membrana enterociti duodeno) Proteine, peptidi Peptidi, dipeptidi Chimotripsinogeno/ chimotripsina Tripsina Proteine, peptidi Peptidi, dipeptidi Pro-elastasi/elastasi Tripsina Proteine, peptidi Peptidi, dipeptidi Pro-carbossipeptidasi Tripsina Estremità C- terminale polipeptidi Peptidi, aminoacidi Intestino tenue (membrana e citoplasma) Amminopeptidasi Assente Estremità N- terminale di oligopeptidi Peptidi, aminoacidi
Le proteasi a serina
Tripsina, Chimotripsina, Elastasi
Enzima Fonte Specificità Commenti R __ 1 0 = R. 0 -NH-CH-C -- NH-CH-C- Legame peptidico suscettibile Tripsina Pancreas bovino Rn-1 = residui con carica positiva: Arg, Lys; Rn #Pro Altamente specifica Chimotripsina Pancreas bovino Rn-1 = residui idrofobici voluminosi: Phe, Trp, Tyr; Rn#Pro Occasionalmente rompe Rn-1 = Asn, His, Met, Leu Elastasi Pancreas bovino Rn-1 = piccoli residui neutri: Ala, Gly, Ser, Val; Rn Pro
Specificità delle proteasi a serina
Specificità Tripsina Il residuo 189 è un Asp (nella chimotripsina è una Ser), le catene laterali preferite (Arg, Lys) sono cationiche possono formare un appaiamento ionico Chimotripsina La grossa catena laterale idrofobica (Phe, Trp, Tyr) che fornisce il gruppo carbonilico del legame peptidico si adatta in una tasca idrofobica localizzata nelle vicinanze dei gruppi catalitici Elastasi Idrolizza la proteina elastina ricca in Ala, Gly, Val. La tasca del legame è occupata dalle catene laterali di Val e Thr (2 Gly negli altri due enzimi) perciò rompe legami dopo residui non polari e con catene laterali piccole. In particolare dopo Ala
Confronto strutturale delle proteasi
Tripsina Chimotripsina Elastasi Asp189 Legame scissile Legame scissile Phe Lys Gly 216 Gly 216 + Gly 226 Gly 226 Ser 189 Chimotripsina Asp 189 Tripsina Legame scissile Ala Thr 216 Val 226 Elastasi
Assorbimento delle proteine
Proteine Pepsina e proteasi pancreatiche Dipeptidi Tripeptidi Oligopeptidi Aminoacidi liberi Trasportatore H+ dipendente Peptidasi microvillari Trasportatore Na" dipendente Dipeptidi Tripeptidi Peptidasi citoplasmatiche (in piccoli quantitativi) Aminoacidi Aminoacidi ASSORBIMENTO ·l'assorbimento inizia nel duodeno ed è incompleta (75-80% nei primi 50cm) ·Gli AA vengono assorbiti in quantità proporzionale alla loro concentrazione ·Trasporto mediato (Na+, H+)
Contenuto proteico nell'uomo adulto
Contenuto in proteine di un UOMO ADULTO: circa 12 kg/70 kg peso actina, miosina, collagene ed emoglobina costituiscono circa la metà di tutte le proteine 40% nel muscolo: possono diventare fonte di amminoacidi in condizioni di stress, si perdono però proteine funzionali 10% tessuti viscerali (fegato, intestino): scarsamente mobilizzate in condizioni di stress 30% nella pelle e nel sangue: diventano fonte di amminoacidi in deficit di proteine alimentari
Ricambio giornaliero delle proteine
ORGANISMO Ricambio giornaliero 1-2% proteine totali Amminoacidi 70-80% riutilizzati 20-30% metabolizzati Proteine dalla dieta Proteine metabolizzate 70 grammi/giorno 250 grammi/giorno
Continuo ricambio proteico
Serve energia sia per la sintesi che per la degradazione: 15-20 % del bilancio energetico La continua demolizione e sintesi è fondamentale per V degradare e rimpiazzare proteine danneggiate v modificare la quantità relativa di differenti proteine in base alle necessità nutrizionali e fisiologiche v rapido adattamento metabolico
Regolazione del turnover proteico
La regolazione del turnover proteico è influenzata da: V stato nutrizionale (energetico e proteico) V da alcuni ormoni (insulina, glucocorticoidi, ormoni tiroidei, ormone della crescita, citochine)
Turnover Proteico
- Tutte le proteine sono soggette al turnover
- È eterogeneo (avviene a velocità diverse per le diverse proteine)
- È intracellulare (sia sintesi, sia demolizione)
- È regolato (sia nella sintesi, sia nella demolizione)
- Ha velocità variabile tra le diverse specie animali (dipende dalla taglia: >nell'animale piccolo)
- Dipende dall'età (>negli infanti)
- Varia per diversi organi e tessuti (veloce in fegato e intestino, più lento nel muscolo)
- Richiede energia (20% dell'energia spesa per il metabolismo basale)
Andamento del ricambio proteico
>Andamento progressivamente decrescente con l'età % ricambio muscolo 30-50% fegato 25% leucociti emoglobina diversa emivita pochi minuti: proteine regolatorie 300 giorni: collageno Quantitativamente corrisponde a 3-4 volte le proteine ingerite ed è pari a 3-4 g proteine/kg/die
Regolazione
Regolazione della sintesi proteica
-Regolazione della sintesi proteica: Avviene nella tappa di inizio della traduzione e dipende dalla disponibilità degli amminoacidi, dei tRNA e della concentrazione dei ribosomi (regolata dagli ormoni insulina, glucagone, ormoni tiroidei, ormoni di accrescimento, glucocorticoidi)
Regolazione della degradazione proteica
-Regolazione della degradazione: Diversi sistemi proteolitici (alcuni digestivi - altri regolatori)