Metodologia della sperimentazione clinica: fasi e requisiti
Documento di Università sulla Metodologia della Sperimentazione Clinica. Il Pdf esplora le fasi pre-clinica e clinica dello sviluppo di un farmaco, i tipi di studi clinici e i requisiti metodologici per garantire rigore scientifico, utile per lo studio universitario.
Mostra di più47 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
METODOLOGIA DELLA SPERIMENTAZIONE CLINICA
Ricerca farmacologica è standardizzata a livello internazionale in 2 fasi:
- Fase pre-clinica: test in vitro, in vivo e sperimentazione su animali
- Fase clinica: sviluppo del farmaco che si svolge con il coinvolgimento del soggetto umano
All'interno della fase clinica, i primi tre step riguardano lo sviluppo clinico del farmaco vero e proprio, che si completa poi con uno studio clinico in cui il medicinale viene autorizzato ad essere commercializzato, seppur sempre controllandone sicurezza ed efficacia. Per questo, la fase 4 è sempre integrata nella fase clinica della ricerca, seppure il farmaco venga già prodotto.
Anno 0 1 2 3 4 5 6 7 8 9 10 11 12 Fase Pre-Clinica Fase Clinica Ricerca e sviluppo Ricerca iniziale e identificazione del target Scoperta del farmaco e sviluppo preclinico Produzione su larga scala Fase 1 Fase 2 Fase 3 Fase 4 Nº di sostanze > 10.000 100 10 2-3 1 1 1 1
Ciò che è importante è che l'ingranaggio si deve avvalere di un team multidisciplinare, in quanto sviluppare un medicinale presuppone diverse competenze, clinici, farmacologici, ingegneri, chimici, statistici. Inoltre, è fondamentale associare agli obbiettivi dei tempi precisi: la pianificazione avviene fin dall'inizio. Ogni fase è legata ad un tempo pianificato di inizio e conclusione. Questa poi deve essere attuata e rispettata.
Ogni fase di sviluppo del farmaco è rappresentata da una sperimentazione clinica, cioè uno studio clinico. Con studio clinico si intende un'indagine su soggetti umani intesa a scoprire effetti clinici, farmacologici di un prodotto di investigazione, con l'obiettivo di accertare la sua sicurezza ed efficacia (GCP). Clinical trial e clinical study sono sinonimi secondo la GCP.
- Esplorativo Farmacologico
- Esplorativo Terapeutico
- Confermatorio Terapeutico
- Confermatorio nella routine clinica
All'interno delle fasi il termine generale è studio clinico, ma è corretto parlare di sperimentazione clinica, intesa come studio clinico che deve soddisfare una di queste indicazioni:
- L'assegnazione del soggetto ad una strategia terapeutica è decisa in anticipo e non rientra nella normale pratica clinica dello stato membro
- La decisione di prescrivere i medicinali e di includere il soggetto nello studio sono prese nello stesso momento
- Sono applicate ai soggetti procedure diagnostiche o di monitoraggio aggiuntive rispetto alla normale pratica clinica
Ogni studio clinico deve seguire una metodologia che permetta di garantire:
- Rigorosità scientifica
- Validità e affidabilità dei risultati: validi significa che i dati devono dare evidenza di ciò che si vuole studiare, che siano misurabili e riproducibili in condizioni simili
- Riproducibilità
- Riduzione del bias e di tutto ciò che può influenzare i risultatiLezione 1_22/11/2024
- Interpretazione dei risultati
- Trasparenza e comunicazione
- Etica: ogni ricerca clinica ha il paziente al centro, soggetto e oggetto della ricerca. La metodologia permette di garantire che siano rispettate tutte le linee guida riguardo ai diritti del paziente.
> Produrre una conoscenza affidabile e applicabile nella pratica clinica, fungendo da ponte tra ricerca di base e pratica clinica.
Questi aspetti sono poi funzionali a garantire tempi, risorse e facilities: in sintesi, permette di eseguire una progettazione in termini di costi.
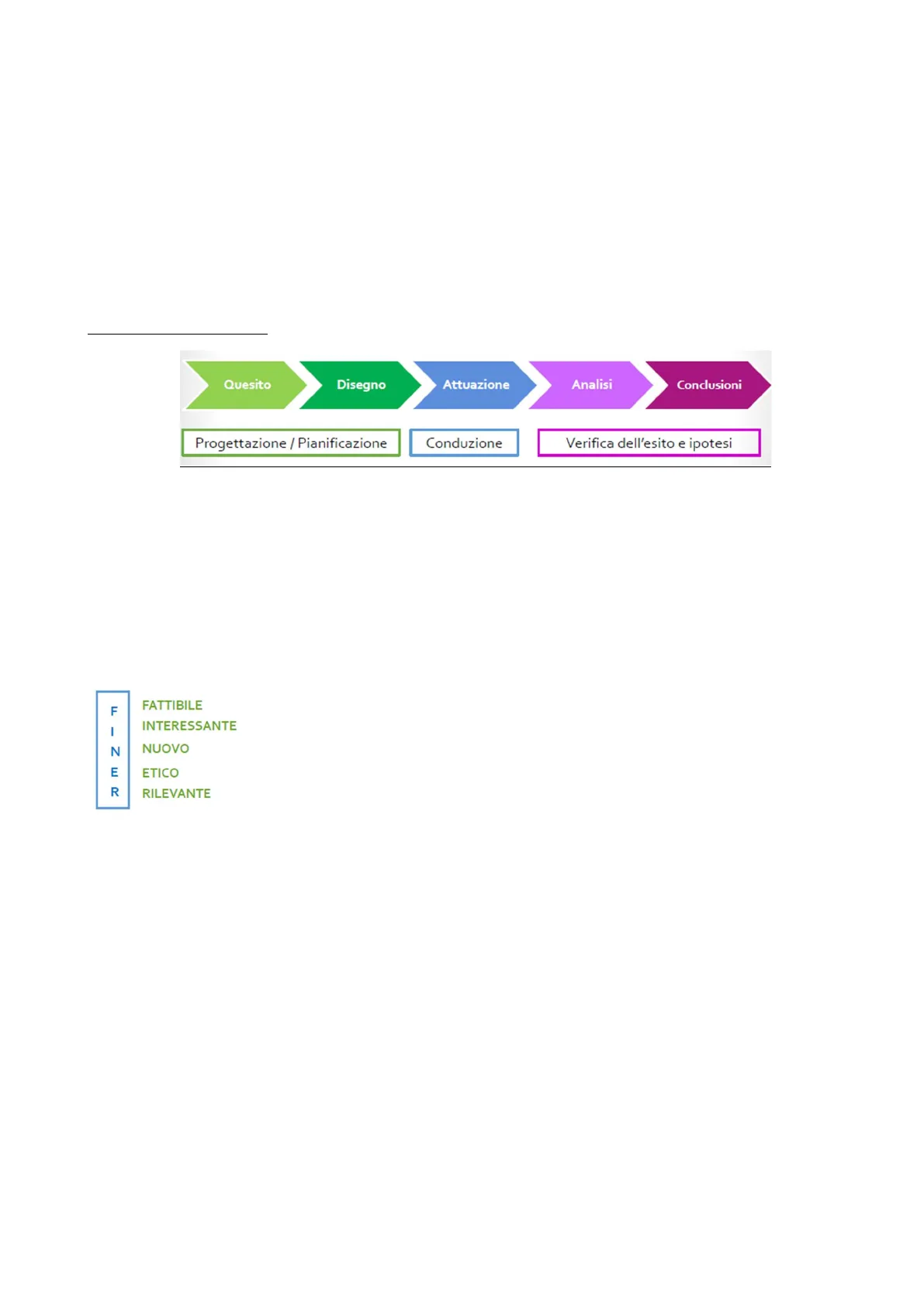
Metodologia come flusso
Quesito Disegno Attuazione Analisi Conclusioni Progettazione / Pianificazione Conduzione Verifica dell'esito e ipotesi
La metodologia si applica sia a studi profit che no profit: negli studi profit, le aziende farmaceutiche sviluppano un medicinale per una finalità commerciale. Nella ricerca no profit, gli studi vengono eseguiti senza scopo di lucro. Inoltre, la ricerca si applica sia per studi interventistici che non-interventistici, od osservazionali.
I ruoli coinvolti diventano: sponsor, o promotore (azienda farmaceutica, IRCCS, ecc), medico sperimentatore e comitato etico. Questi ruoli sono coinvolti, in modi e tempi diversi nella metodologia della ricerca clinica.
1. QUESITO
F 1 FATTIBILE Le diverse tipologie di quesito sono associate ad eziologia e rischio, diagnosi, prognosi e terapia, trattamento e intervento. La vera sfida è costruire un quesito di ricerca che INTERESSANTE sia chiaro, specifico e a cui si possa dare una risposta per mezzo di uno studio. N NUOVO E ETICO I quesiti possono quindi essere distinti in conoscitivi e ipotesi di soluzioni: se non si R RILEVANTE conosce il problema, il quesito è di tipo conoscitivo. Conoscere il problema significa avere due informazioni, la sua incidenza e i fattori predittivi positivi e negativi.
Il quesito di ricerca contiene diversi elementi da mettere in relazione (PICO):
- Popolazione di riferimento (chi è coinvolto? una determinata popolazione soggetta ad una patologia)
- Intervento: come intendo intervenire. Il medicinale sperimentale è un intervento che manipolo per ottenere un esito
- Confronto: valutare se c'è un'alternativa, magari già riconosciuta, dalla pratica clinica.
- Esito: cosa intendo ottenere, l'outcome.
Quando si parla di quesito bisogna partire dalla revisione della letteratura scientifica, per definire il razionale e motivare la scelta di un determinato quesito. Inoltre, vanno valutate le variabili pertinenti:
- Variabili indipendenti (esposizione): quella che viene manipolata, di cui ci interessa valutare il rapporto di causa con l'outcome (test diagnostico, intervento terapeutico).
- Variabili dipendenti (risultati): devono o essere misurabili, oggettive, e con probabilità che si verifichi nel periodo di osservazione.
A questo punto si può formulare l'ipotesi di ricerca, l'affermazione che predice la relazione o la differenza tra due o più variabili in termini di risultati attesi.Lezione 1_22/11/2024
I bambini con età dai 5 ai 10 anni a cui sono fornite informazioni pre -operatorie sulla tonsillectomia, sperimentano minore ansia post- operatoria rispetto ai bambini della stessa età che non ricevono queste informazioni.
Variabile indipendente
L'ansia postoperatoria Il fornire informazioni preoperatorie sulla tonsillectomia, in questo caso, è la variabile indipendente ed è considerata il trattamento (manipolazione) utilizzato per scoprire i suoi effetti sull'ansia post-operatoria
2. DISEGNO
Nella pianificazione è importante stabilire la popolazione, la tipologia di studio più appropriata per poter rispondere nel modo più semplice al quesito, le risorse, il tempo a disposizione e la gestione dei risultati, ovvero chiarire in che modo analizzare i risultati e come condividerli.
Popolazione target
a. devono essere chiari i criteri di inclusione/esclusione, ovvero i criteri di eleggibilità. Lo studio e l'identificazione dei soggetti da arruolare deve riflettere la popolazione generale. Diventa quindi importante non selezionare una popolazione non troppo diversa da quella che si incontra nella pratica quotidiana, perché i risultati dello studio siano applicabili. b. Fondamentale è anche definire la dimensione del campione, ovvero il numero di soggetti da includere. La potenza di un test statistico è la capacità del test di individuare un effetto, se quell'effetto esiste realmente. Valutare la dimensione del campione permette di capire il numero di centri da coinvolgere, il numero di pazienti per ogni centro e il costo della sperimentazione. In questo frangente è diverso il concetto di arruolato rispetto a randomizzato (il paziente arruolato è quello che accetta di partecipare allo studio, randomizzato invece è il paziente che assume il farmaco: non tutti i pazienti arruolati poi andranno per forza ad assumere il farmaco).
Esistono diversi tipi di studio, classificati in base a randomizzazione, blinding, e superiorità/inferiorità.
Blinding Randomizzazione consapevolezza delle parti coinvolte del tipo di trattamento assegnato Studi clinici di superiorità o di non inferiorità metodo utilizzato per assegnare i pazienti al trattamento o al controllo entità della differenza tra gruppi di trattamento e di controllo attesa Disegno
Inoltre, per assicurare che gli esiti dello studio siano dovuti solo al trattamento, i soggetti sono divisi in gruppo sperimentale e controllo, che riceve un placebo, o la miglior terapia già disponibile. L'utilizzo del placebo è considerato etico nel momento in cui non c'è un trattamento alternativo.
La randomizzazione è l'unico metodo che consente di distribuire i pazienti in gruppi non sbilanciati per fattori prognostici, garantendo a tutti la stessa probabilità di essere associati ad uno dei due gruppi. Essa prevede: la generazione di una sequenza casuale e l'implementazione di tale sequenza, in modo che i partecipanti non siano a conoscenza della sequenza. Di fatto, come verranno analizzati i dati da cui si traggono le conclusioni viene deciso in questo momento, la pianificazione coinvolge tutti gli aspetti del disegno di studio.Lezione 1_22/11/2024
Per quanto riguarda il blinding, si può parlare di single blind, double blind e triple blind, in cui sia gli sperimentatori che i soggetti partecipanti, che altri investigatori non sanno quale trattamento è somministrato a ciascun soggetto: questo è utile quando le variabili cliniche esaminate possono essere interpretate in modi differenti.
Ci sono diversi tipi di disegni di studio, come studio parallelo, studio crossover, umbrella trial, basket trial.
Ci sono poi anche studi osservazionali, che sono legati ad avere maggiore conoscenza, osservando dati che vengono raccolti da una pratica clinica. Gli esiti di uno studio osservazionale possono essere utilizzati da un'azienda farmaceutica per valutare un eventuale sviluppo ulteriore di un farmaco sperimentale. Negli studi osservazionali descrittivi, non è presente un gruppo di controllo, in quelli analitici è presente il controllo.
Studi sull'eziologia
Studi sull'eziologia utili per determinare se un agente eziologico è responsabile di una malattia.
CASO-CONTROLLO COORTE PROSPETTICA ESPOSTI OUTCOME + ESPOSTI NON ESPOSTI OUTCOME - SOGGETTI DELLO STUDIO ESPOSTI CONTROLLI NON ESPOSTI NON ESPOSTI OUTCOME - DIREZIONE DELL'OSSERVAZIONE Retrospettivo Prospettico
Tipologia di studio
SPERIMENTAZIONI CLINICHE
Disegno FASE I SCOPO Fornire una prima valutazione della sicurezza e tollerabilità del nuovo principio attivo sull'uomo DURATA Breve (da pochi mesi ad un anno) POPOLAZIONE Piccoli gruppi di soggetti: volontari sani oppure pazienti selezionati (20 - 100) Valutazioni di · farmacocinetica (assorbimento, distribuzione, metabolismo, escrezione) · farmacodinamica (meccanismo d'azione) · tollerabilità preliminare (massima dose tollerata) DOVE Strutture specializzate ed autorizzate (determina AIFA 809/2015) Se il farmaco dimostra di avere un livello di tossicità accettabile rispetto al beneficio previsto, può passare alle successive fasi della sperimentazione.
CARATTERISTICHE
Durata breve e piccolo gruppo di soggetti sono le cosiddette 'azioni e mitigazioni', ovvero modalità per mettere a rischio un minor numero di soggetti possibili, considerando che i farmaci che stiamo testando sono appena usciti dalla sperimentazione pre-clinica. Inoltre, il dosaggio iniziale è più basso del dosaggio considerato ottimale nella fase pre-clinica. Tramite una dose-escalation si arriva poi al dosaggio massimo tollerato, valutando gli esiti in termini di sicurezza. Gli studi di fase I sono gli unici in Italia che devono essere svolti in strutture specializzate e autorizzate.
CASI OUTCOME +