Le proteine: caratteristiche, struttura e importanza biologica
Slide sulle Proteine che descrive le caratteristiche principali e i diversi livelli di organizzazione strutturale. Il Pdf, utile per lo studio della Biologia a livello universitario, illustra la composizione delle proteine e la loro importanza biologica, con diagrammi esplicativi.
Mostra di più17 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
LE PROTEINE
Caratteristiche: sono catene (polimeri) di amminoacidi sono il più abbondante materiale biologico negli organismi animali sono essenziali per la struttura e le funzioni degli esseri viventi Le informazioni per la costruzione delle proteine sono contenute nei geni, cioè nelle sequenze di DNA.
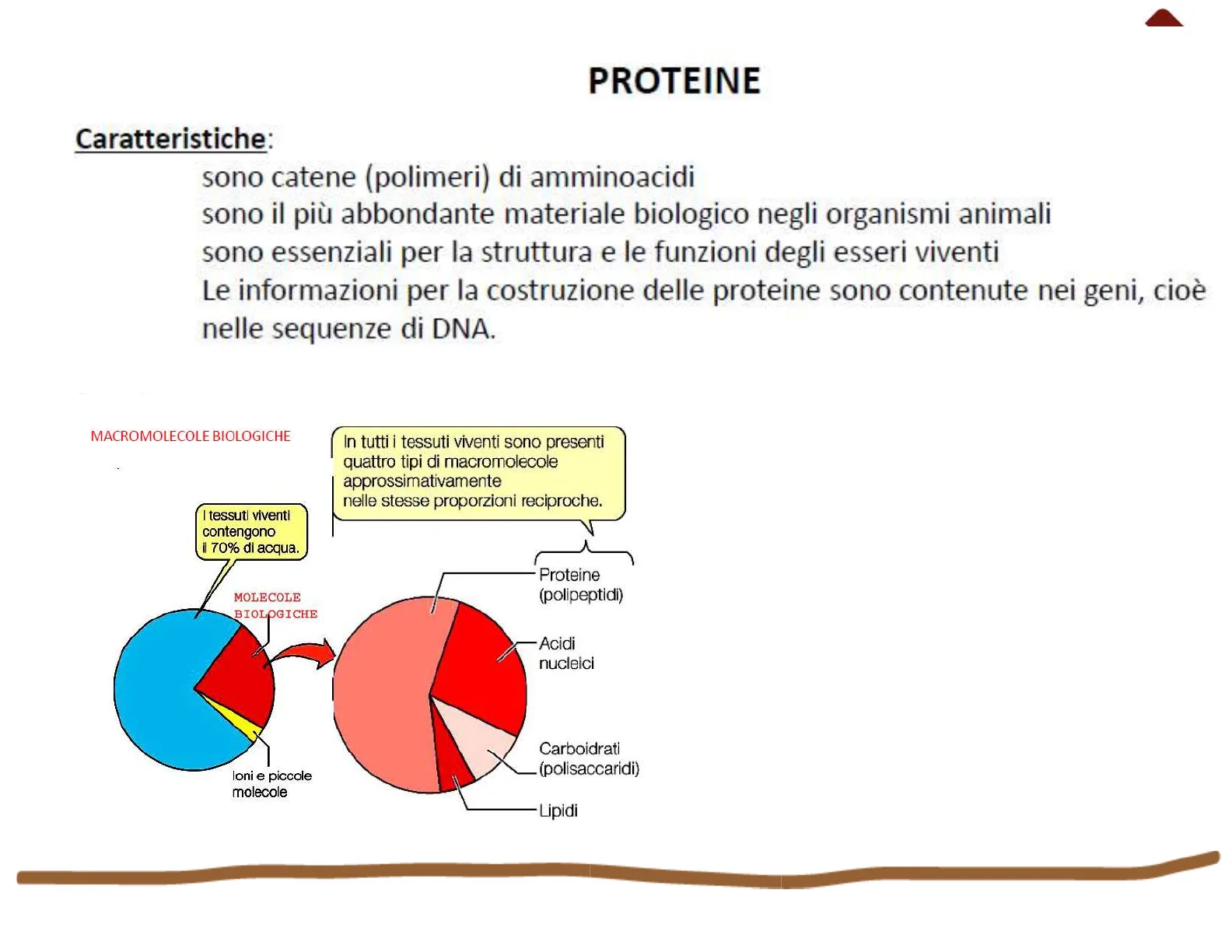
MACROMOLECOLE BIOLOGICHE
In tutti i tessuti viventi sono presenti quattro tipi di macromolecole approssimativamente nelle stesse proporzioni reciproche. I tessuti viventi contengono il 70% di acqua.
MOLECOLE BIOLOGICHE
Proteine (polipeptidi) Acidi nucleici loni e piccole molecole Carboidrati (polisaccaridi) LipidiProteine: molecole «tuttofare»! Tutte le proteine sono polimeri di composti chiamati amminoacidi. Esistono 20 amminoacidi diversi, che combinati fra loro formano milioni di tipi diversi di proteine ...
Phe Gly Glu Asn Gin Ala Arg Pro Tyr Ser Trp Met Asp lle Leu Ly's Cys Val HIR alpha helix beta sheet
RUOLI BIOLOGICI DELLE PROTEINE
CLASSE FUNZIONALE E RUOLO
| CLASSE FUNZIONALE | RUOLO | ESEMPI |
|---|---|---|
| Proteine strutturali | Formazione di strutture biologiche | collagene, cheratine proteoglicani |
| Enzimi | Catalizzatori | ossidoriduttasi, trasferasi, idrolasi, liasi, isomerasi, ligasi |
| Proteine di trasporto | trasporto molecole a distanza, trasporto transmembrana | emoglobina, albumina di siero trasportatore glucosio, canali ionici |
| Proteine contrattili/motili | contrazione e movimento | impalcatura cellulare motori cellulari, muscoli |
| Proteine di riserva | riserve di nutrienti, metalli | ovalbumina ferritina |
| Proteine protettive | sistema immunitario coagulazione | immunoglobuline trombina/fibrinogeno |
| Recettori/regolatori | ormoni, recettori di membrana, repressori/attivatori | insulina, recettori cellule T repressore lac |
| Altre | funzioni esoteriche | proteine antigelo |
Biochimica
FUNZIONE STRUTTURALE
Capelli, unghie, piume, corna, cartilagine, tendini.
FUNZIONE PROTETTIVA
Proteine che aiutano a sconfiggere i microrganismi (come gli anticorpi) o permettono la coagulazione del sangue (come il reticolo di fibrina).
FUNZIONE REGOLATORIA
Controllano le funzioni delle cellule e formano alcuni ormomi (come i cristalli di ormone della crescita nell'immagine).
FUNZIONE CONTRATTILE
Permettono ai muscoli di contrarsi, al cuore di pompare sangue e agli spermatozoi di muoversi.
FUNZIONE DI TRASPORTO
Trasportano molecole, come per esempio l'ossigeno o il ferro, attraverso il corpo.Le proteine sono polimeri di amminoacidi. Svolgono molteplici funzioni e ognuna di esse ha una forma specifica indispensabile per il lavoro che deve svolgere.
Amminoacidi: Struttura Generale
Tutti gli amminoacidi hanno una struttura comune: un atomo di carbonio legato a quattro gruppi ...
- un atomo di idrogeno
- un gruppo amminico
- un gruppo carbossilico (acido)
- un gruppo "R" diverso per ciascuno dei 20 amminoacidi.
H L H O H N C c H RH O H N-C C OH H H H.N-C-COOH 2 R HAmminoacido Amminoacido
Amminoacidi e Gruppi R
COO" COO- COO I + H3N-C-H H3N -C-H 1 H3N-C-H + 1 CH3 CH / Glicina CH3 CH3 COO- Alanina Valina I H3N-C-H + - COO COO- CH2 I H3N-C-H + + H3N-C-H CH - CH2 H-C-CH3 - CH2 CH2 COO - H C. + H2N CH2 I Metionina Isoleucina I H2C-CH2 Prolina COO COO )- H3N-C-H I H3N-C-H I CH2OH Serina COO- Cisteina COO- - COO- H3N-C-H + I H3N-C-H - CH2 I I I H-C -OH C C I CH3 H2N H2N Glutammina COO- coo- COO- I - + H3N-C-H H3N-C-H H3N-C-H I I CH2 CH2 CH2 NH OH Fenilalanina Tirosina Triptofano Gruppi R a carico negativo COO- COO- - - + H3N-C-H 1 CH2 COO- - CH2 COO Aspartato Glutammato Polari, Gruppi R non caricati Non polari, Gruppi aromatici + I + H3N-C-H I CH2 I CH2 Treonina Asparagina I + I + H3N-C-H H3N-C-H H3N-C-H Gruppi R a carico positivo CH2 - 1 CH2 - CH2 - C-NH+ CH2 - CH2 CH2 - CH2 I CH C -NH+ CH2 I 1 +NH3 C =NH2 1 NH2 Lisina Arginina Istidina Non polari, Gruppi R alifatici COO I I H COO- COO- I + S I CH CH3 H3N-C-H 1 CH2 I NH I /. CH3 CH3 Leucina CH2 I SH + +COME SI CREA IL POLIMERO?
Formazione del Polimero Proteico
R H R H I I HO-C-C-N-H + HO-C-C-N-H 1 - O H O H R H R H 1 1 1 HO-C-C-N-C-C-N-H = o H ) H + H20LEGAME PEPTIDICO: HHO H - N - C - C -OH 1 R HHO H - N - C - C -OH İ R' H2O HHO | | | H - N - C - C -OH 1 HHO H - N -C -C -OH 1 1 R R 1 HHOHHO - = - = H - N - C -C - N -C -C -OH 1 1 R R G. MerlinoPROTEINE
Struttura delle Proteine
ala Catena di amminoacidi gly leu leu gly gly val val lys lys his lys lys lys gly ala his Catena di amminoacidi Struttura primaria Struttura secondaria Struttura terziaria Struttura quaternaria La sequenza di amminoacidi che forma la struttura primaria determina, in conseguenza dei legami idrogeno che si formano tra di loro, dei ripiegamenti caratteristici che ne condizionano la struttura secondaria. A causa delle interazioni tra i gruppi R dei diversi amminoacidi, la struttura secondaria può ancora ripiegarsi a costituire la struttura terziaria di alcune proteine. Infine, molte proteine sono formate da più catene di amminoacidi legate tra loro, che nel loro insieme rappresentano la struttura quaternaria.
Livelli di Struttura delle Proteine
Primary structure Amino acids Becondary structure 6 B-pleated those Terti 30 Livelli di struttura delle proteinelegame peptidico monomeri (amminoacidi) 0 0 0 H H H H R R C C N C C N C N c C N c C R R H H H H 0 0 legame a idrogeno & elica La struttura primaria di una proteina è la sequenza degli amminoacidi nella catena polipeptidica. La struttura secondaria è il ripiegamento dovuto ai legami a idrogeno tra le parti costanti degli amminoacidi.loop foglietto B legame a idrogeno ponte disolfuro ox elica subunità 1 subunità 2 subunità 3 subunità 4 La struttura terziaria è la conformazione finale della molecola causata dalle interazioni tra i gruppi R. Alcune proteine hanno una struttura quaternaria, cioè sono formate da più catene rilegate. Immunoglobulina (4 catene polipeptidiche)
Gli Enzimi nelle Reazioni Cellulari
13. Gli enzimi nelle reazioni cellulari substrato sito attivo lattosio
- Ciascun enzima ha un sito attivo che riconosce il substrato della reazione.
lattasi
- In seguito al legame con l'enzima, il lattosio causa una modifica nella conformazione della lattasi: ora substrato ed enzima si incastrano perfettamente e la reazione può essere avviata.
glucosio galattosio
- Il legame tra i due zuccheri semplici che compongono il lattosio viene rotto e i due zuccheri semplici vengono liberati.
Gli enzimi sono catalizzatori, cioè accelerano le reazioni chimiche. Sono proteine globulari che hanno un sito attivo specifico e interagiscono con le molecole substrato, facilitando la rottura o la formazione di legami chimici.Un enzima NON fa parte dei reagenti o dei prodotti della reazione chimica che catalizza.
Esempi di Enzimi e Loro Funzioni
amilasi amido glucosio ATP sintasi ADP + P ATP glicogeno sintasi glucosio glicogeno DNA polimerasi nucleotidi DNA substrati (=reagenti) prodotti enzimiDenaturazione
Denaturazione Proteica
Proteina normale Proteina denaturata La rinaturazione può essere impossibile! Una proteina può in certe condizioni essere denaturata in modo irreversibile, per esempio dal calore.