Politrauma e marcatori biologici: terapia antitumorale e resistenza ai farmaci
Slide su politrauma e marcatori biologici, esplorando la terapia antitumorale, la crescita dei tumori e la resistenza ai farmaci. Il Pdf, adatto per lo studio universitario in Biologia, descrive i meccanismi d'azione dei farmaci e le cause di resistenza, con grafici e schemi esplicativi.
Mostra di più17 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Terapia Antitumorale: Meccanismi e Resistenza
10/12/2024 Il processo di metastatizzazione tende a selezionare cellule capaci di sopravvivere anche in assenza di ossigeno, quindi quelle più glicolitiche e resistenti all'apoptosi indotta da ipossia e da acidità. La terapia antitumorale si fonda sulle caratteristiche cinetiche di crescita dei tumori e su una serie di modelli della ricerca preclinica. Una massa tumorale è molto eterogenea in quanto composta da cellule in diverse fasi del ciclo cellulare e con diverso potenziale di crescita. Lo scopo della terapia antitumorale è quello di colpire il maggior numero di cellule nelle diverse fasi di divisione cellulare minimizzando la probabilità di insorgenza e di resistenza alla terapia impiegata. Per studiare l'azione di un farmaco antitumorale dobbiamo analizzare dapprima la velocità di crescita di un tumore.
100 50 Growth fraction 0 100 Percent of maximum 50 Growth rate 0
- La vicinanza dei vasi sanguigni
- La disponibilità d'ossigeno
Terapia Antitumorale: Tipologie di Farmaci
Si tratta di farmaci di diversa natura e che si basano su meccanismi di azione ben distinti:
- Chemioterapici antineoplastici
- Farmaci che stimolano il sistema immunitario (immunoterapia)
- Farmaci a bersaglio molecolare diretti contro proteine di segnale (target therapy)
- Farmaci che vanno ad agire sul fuso mitotico
- Farmaci che agiscono direttamente sul DNA
Number of cancer cells 1012 Detectable cancer > Death 1010 Palliation Non-detectable 108 cancer D 106 104 Resistance or toxicity 102 B C Cure Cure Surgery Radiation
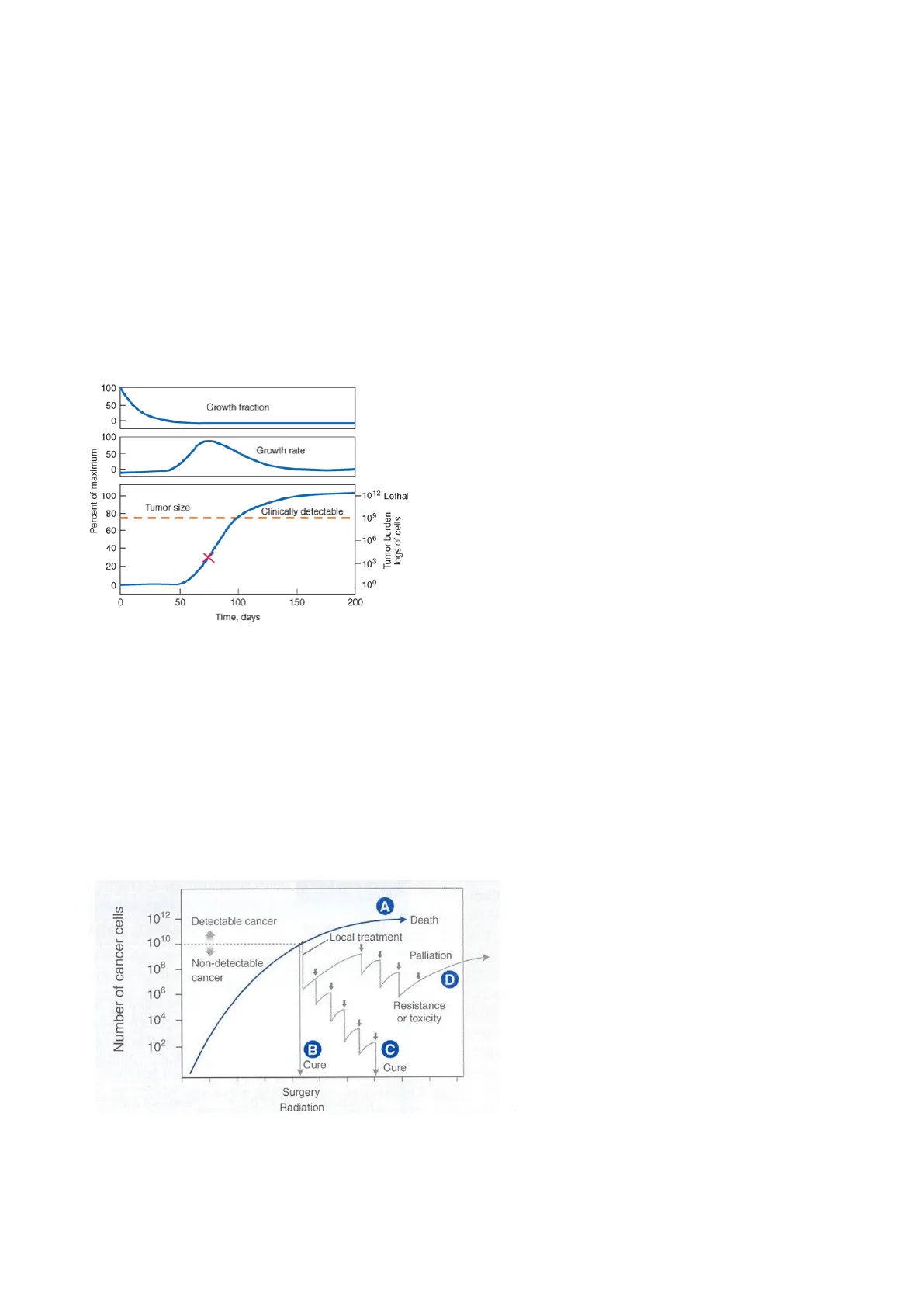
Ipotesi di Uccisione Logaritmica e Crescita Tumorale
IPOTESI DI UCCISIONE LOGARITMICA I farmaci uccidono una frazione costante, non un numero costante, di cellule. All'interno dell'immagine vengono raffigurate 4 curve che rappresentano:
- La curva A raffigura la crescita del tumore nel corso del tempo
- La curva B raffigura l'effetto della chemioterapia dopo l'intervento
- La curva C raffigura il trattamento anche locale del tumore
- La curva D raffigura il trattamento locale derivante da un processo di chemioterapia sistemica
Pagina 1 di 17 80 109 60 -106 40 103 20 Tumor burden logs of cells 0 100 - 0 50 100 150 200 Time, days In figura ci viene rappresentata la curva di Gompertz e ci indica la crescita tumorale. I principali fattori che determinano un aumento della crescita tumorale sono:
100 -1012 Lethal Tumor size Clinically detectable A Local treatmentI risultati del trattamento dipendono da:
- Dose di farmaco somministrata
- Numero e frequenze di ripetizione dei trattamenti
- Dimensioni del tumore all'inizio del trattamento
Citotossicità e Vulnerabilità Cellulare
La citotossicità è proporzionale all'esposizione totale al farmaco. Le cellule possono manifestare diversa vulnerabilità ai farmaci citotossici a seconda della fase del ciclo cellulare:
- Agenti non ciclo-specifici: farmaci sono tossici sia per le cellule che si dividono che per quelle quiescenti (fase G0). Esempio: agenti alchilanti (melfalan e nitrosouree)
- Agenti ciclo-specifici, fase-aspecifici: Questi farmaci distruggono le cellule che si dividono, a prescindere dalla fase del ciclo cellulare. Esempi: antracicline, mitoxantrone, derivati del platino.
- Agenti ciclo-specifici, fase-specifici: Questi farmaci distruggono le cellule che si dividono, in fasi particolari del ciclo cellulare. Esempi: antimetaboliti (fase S), alcaloidi della vinca (fase M), bleomicina (fase S-G2).
Numero di cellule Log dosaggio agenti alchilanti irradiazione - antimetaboliti Nella figura accanto viene raffigurata la letalità di un farmaco ciclo-specifico rispetto un farmaco non ciclo-dipendente. Entrambi i farmaci partano con lo stesso numero di cellule ma all'aumentare del dosaggio i farmaci alchilanti e d'irradiazione tendono a determinare la diminuzione della crescita cellulare, a differenza degli antimetaboliti che avranno all'inizio una diminuzione della crescita cellulare fino poi ad arrivare ad una fase di plateau che corrisponde al completo blocco della crescita.
Caratteristiche dei Farmaci Chemioterapici
L'attività dei farmaci chemioterapici si caratterizza per essere:
- Sistemico perchè questi farmaci riescono a raggiungere tutte le zone del corpo
- Poco selettivo perchè non sempre risparmia la cellula normale
- Sinergica fra i diversi agenti perché a volte questi farmaci sono accoppiati con la radioterapia
- Istotipo specifica perché i tumori nello stesso organo possono essere trattati con farmaci diversi a seconda dell'istotipo
- Organo aspecifica perché alcuni farmaci possono essere usati in tumori diversi
- Estremamente eterogenea
Interazioni nel Trattamento Oncologico
OSPITE-TUMORE-FARMACO Pagina 2 di 17OSPITE INTERAZIONI OSPITE-TUMORE IMMUNORISPOSTA INTERAZIONI FARMACO-OSPITE MALATTIA FARMACOCINETICA TERAPIA TUMORE FARMACO CHEMIORESISTENZA INTERAZIONI FARMACO-TUMORE L'interazione tra organismo ospite e tumore è molto difficile da studiare infatti all'interno della slide vengono trattate queste tipo d'interazioni e come esse vengano modulate dal sistema immunitario nella sua risposta.
Classificazione dei Farmaci Antitumorali
A seconda del loro meccanismi d'azione, dell'origine e/o della chimica si dividono in:
- Alchilanti: formano legami covalenti con i gruppi nucleofilici della catena del DNA
- Antimetaboliti: antagonizzano l'azione dei metaboliti normali a livello del sito effettore
- Antibiotici: producono tagli nel DNA mediante produzione di radicali liberi e interazione con la topoisomerasi II; alterano la sintesi dell'RNA; alcuni interagiscono con le strutture di membrana
- Antimicotici: formano legano con la tubulina interferendo con la formazione del fuso mitotico
- Ormoni e antagonisti ormonali: impiego di sostanza che modulano la crescita tumorale attraverso un'azione di tipo endocrinologico
- Gruppo miscellaneo: non classificato contenente citoprotettori e derivati dell'urea
Impiego dei Chemioterapici Antineoplastici
PERCHE' E QUANDO VENGONO IMPIEGATI? Il prof legge la slide
Stadi Precoci e Avanzati
Stadi precoci Stadi localmente avanzati Stadi avanzati I chemioterapici antineoplastici causano morte cellulare attraverso un danno citotossico e un'interferenza con i processi replicativi. chemioterapia neoadiuvante o primaria chemioterapia della malattia metastatica +/- chemioterapia adiuvante chirurgia radioterapia chirurgia AGENTI ALCHILANTI guarigione prolungamento della sopravvivenza operabilità guarigione prolungamento della sopravvivenza guarigione prolungamento della sopravvivenza palliazione Pagina 3 di 17 chirurgia TOSSICITA'
Agenti Alchilanti: Meccanismo d'Azione
Temozolomide HON H2N. HON. O N. CH3 CH N N=N spontanea NH2 N @ ·CH3 Nucleus O MTIC Temozolomide MTIC N2 + H+ Z HN OCH 3 H2N N N DNA guanina Apoptosis H2N N DNA Gli agenti alchilanti sono quei composti che vanno ad in inibire la replicazione del DNA. Vengono definiti alchilanti perché vanno ad inserire dei gruppi alchilici nelle basi azotate determinando la formazione di alcuni legami crociati meglio noti come cross-link. Sono degli agenti non ciclo specifici, ma più efficaci nelle cellule in rapida proliferazione (fasi G1 e S). Da un punto di vista farmacologico facciamo riferimento alla tenozolamide che viene usato contro il glioma nei pazienti pediatrici e va generalmente a svolgere un'azione citotossica andando ad intercalare questi gruppi alchilici nel doppio filamento.
Agenti Antimetaboliti: Funzione e Applicazioni
AGENTI ANTIMETABOLITI MTX RFT/PCFT RFT/PCFT MTX-PG MTX FPGS GCP + Nucleus Drug target Liposome MTX Gli agenti antimetaboliti hanno il compito di agire su specifiche componenti delle basi azotate del DNA (formazione dell'anello pirimidinico o di quello purinico). A differenza degli alchilanti, maggiore è il tempo di esposizione, maggiore sarà il numero di molecole che reagiranno. Da un punto di vista farmacologico consideriamo il fluorobracile che viene utilizzato nel carcinoma mammario o in quello gastrico e generalmente viene associato ad altri farmaci. I primi studi vennero effettuati sugli agonisti dell'acido folico che andava ad interagire con una proteina ubiquitaria fondamentale per la sintesi del DNA, Successivamente venne sintetizzato il metrotrexato, usato nelle leucemie, molto simile all'acido folico perché va ad agire come un'antimetabolita perché penetra nelle cellule che hanno un trasporto attivo ovvero trasportato dai folati. Nella cellula vengono inseriti dei residui di acido butalico e va a ridurre la capacità di diffusione all'esterno, quindi andando a competere con l'acido folico blocca una serie di cofattori untili nella sintesi delle purine e pirimidine.
Pagina 4 di 17 + -NH N -NH N DNA breaks Cytosol N DNA Methylation H
Antibiotici con Ruolo Antineoplastico
Possono avere anche un ruolo antineoplastico, come ad esempio la Mitomicina, un tempo molto usato con tale funzione. Meccanismo d'azione:
- Alchilazione del DNA ed inibizione della sintesi dello stesso (molto simile agli agenti alchilanti);
- Inibizione dei ribosomi e quindi della sintesi proteica;
- Stress ossidativo da radicali liberi del perossido ad alte dosi, determinando la rottura del flamenco di DNA;
- Non ciclo o fase-specifi.
Mitomycin C G1 M S · DNA Alkylation . Ribosomal RNA Inhibition · Weakens Antioxidant Defense G2 Anche in questo caso, gli effetti del farmaco sono potenziati se le cellule sono in fase attiva del loro ciclo cellulare (ovvero fase G tardiva e fase S), rispetto alle fasi di riposo. La scelta ovviamente è dettata dalla sensibilità, più o meno variabile, dei vari tumori all'azione specifica della molecola e dalla sede (esempio: mitomicine non superano la barriera ematoencefalica per cui l'uso in tal senso può essere limitato). Alcuni antibiotici, tuttavia, agiscono con meccanismi molecolari differenti, ma in generale la loro azione principale è quella di formare legami covalenti con gli acidi nucleici, interferendo con la sintesi del DNA.
Antimitotici: Inibizione della Divisione Cellulare
ANTIMITOTICI Queste molecole determinano l'inibizione della divisione cariocinetica o mitotica della cellula. Tra le molecole che rientrano in questa categoria troviamo la colchicina e i taxani.
Colchicina
Colchicina: - Prima ad essere utilizzata; - è un alcaloide; - agisce inibendo la polimerizzazione dei microtubuli e quindi la formazione del fuso mitotico.
Taxani
Taxani: - alcaloidi estratti dalle conifere; - Azione opposta alla colchicina, in quanto determinano una stabilizzazione/ congelamento del fuso impedendo così il movimento e il rinnovamento. - Uno dei primi ad essere studiato fu il paclitaxel e successivamente il docetaxel. Docetaxel agisce legandosi in maniera reversibile e con elevata affinità ai microtubuli della cellula. Questo causa l' aggregazione della tubulina e la conseguente stabilizzazione dei microtubuli, impedendone così la fisiologica depolimerizzazione. Quindi l'effetto finale è sempre quello di inibizione della divisione cellulare ma con meccanismi completamente opposti, la colchicina inibisce la formazione del fuso, i taxani la dissoluzione. Vengono pertanto definiti citostatici (inibizione della replicazione cellulare).
G Interphase Cell cycle M S Prophase Microtubules Treatment Stabilization Depolymerization Tubulin dimer @ 3 Taxanes Anaphase ( Mitotic checkpoint Telophase Cell death Cytokinesis Metaphase 5 di 17