Effetti biologici delle radiazioni ionizzanti e implicazioni in oncologia
Documento da Corso di Laurea in Medicina e Chirurgia su Effetti biologici delle radiazioni ionizzanti: implicazioni in ambito oncologico. Il Pdf esplora l'interazione tra radiazioni ionizzanti e sistemi biologici, con focus su radiosensibilità, danni molecolari e strategie di frazionamento della dose in radioterapia, utile per Biologia a livello universitario.
Mostra di più11 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Introduzione agli effetti biologici delle radiazioni ionizzanti
Se la scorsa lezione ci siamo soffermati sugli effetti dannosi delle radiazioni ionizzanti, oggi vedremo com'è possibile sfruttarli in modo selettivo a scopo anti tumorale: trattandosi di conoscenze basilari per qualsiasi medico, utili per esempio per capire e distinguere una reazione acuta da una tardiva, è un argomento importante non solo per oncologi e radioterapisti.
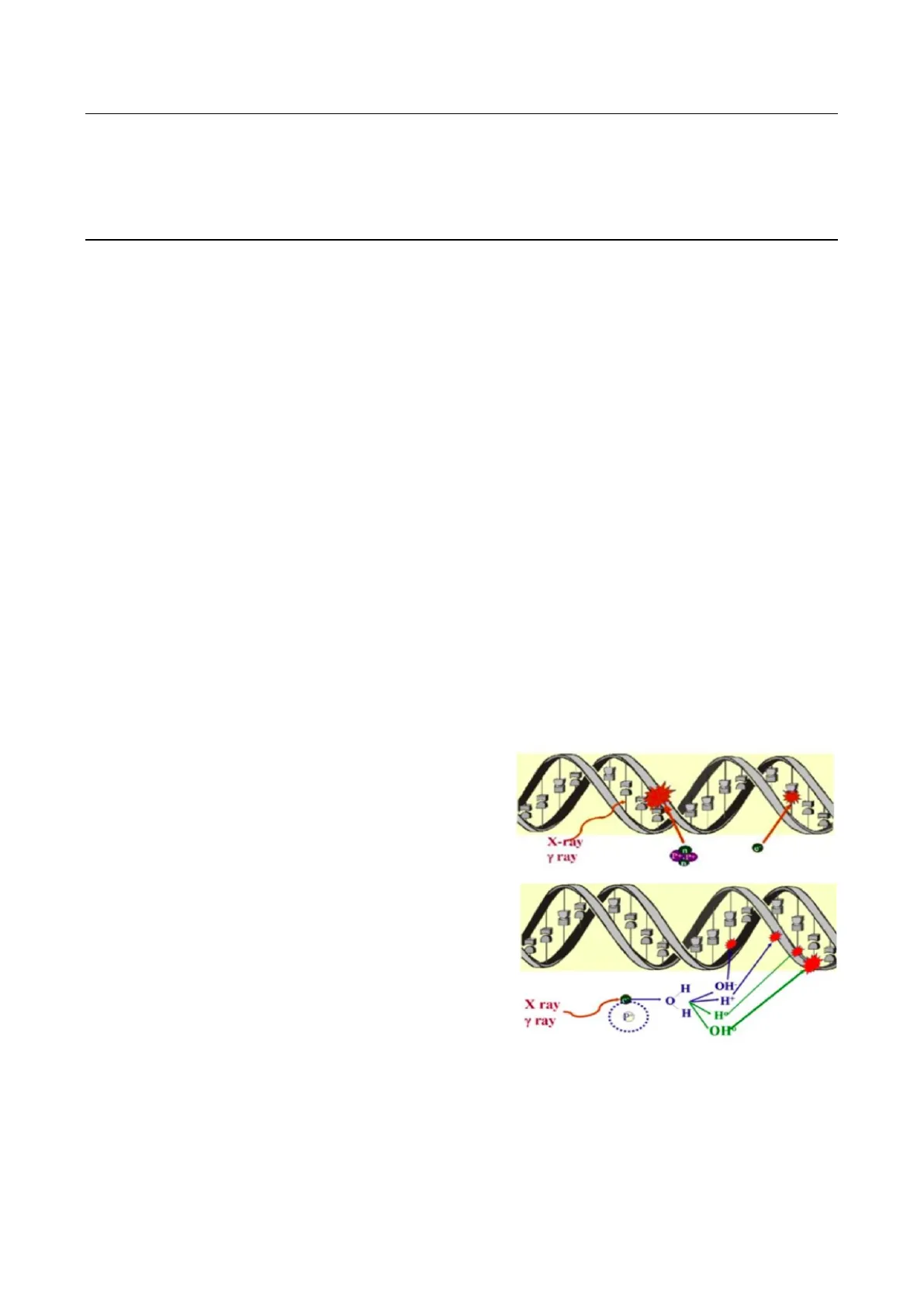
L'interazione tra radiazioni ionizzanti e sistemi biologici può avvenire in modo diretto o indiretto, tramite la formazione di specie radicaliche reattive dell'ossigeno. L'acqua, che rappresenta circa il 60% del peso di un individuo adulto, è la molecola con cui le radiazioni ionizzanti interagiscono costantemente: ad avvenire è una reazione enzimatica detta "radiolisi ionizzativa", che provoca la liberazione di radicali liberi dell'ossigeno (perossido di idrogeno e idroperossido). L'ossigeno ha infatti la capacità di sottrarre elettroni alle biomolecole ossidandole, generando perossidi organici che hanno elevata tossicità. Questi sono gli effettori del danno replicativo a livello del DNA, molecola target delle radiazioni ionizzanti. Questo fenomeno ha delle importanti implicazioni cliniche: la presenza di ossigeno in concentrazioni sufficienti nel tessuto irradiato è un elemento radiosensibilizzante naturale; viceversa in condizioni di ipossia o anossia tissutale, la risposta alle radiazioni ionizzanti sarà inferiore; l'anossia determina quindi una condizione di radioprotezione.
Quando ci si trova di fronte a delle grandi masse tumorali bisogna aspettarsi una radioresistenza, poiché il centro delle stesse rappresenta un core necrotico colliquativo ed ipossico fortemente radioresistente, che costituisce un ostacolo importante al trattamento con radiazioni indirettamente ionizzanti. Nel processo di accrescimento di un tumore, infatti, si assiste parallelamente ad un processo di neoangiogenesi (sviluppo di una fitta rete capillare) e anossia, in quanto la prima è sempre insufficiente rispetto all'entità di crescita delle cellule tumorali, che avviene con un ritmo proliferativo molto elevato ed anarchico. La distanza tra molte cellule neoplastiche e la parete capillare è così elevata da rendere insufficiente l'apporto di ossigeno per diffusione. Nel caso invece delle radiazioni direttamente ionizzanti le condizioni di ossigenazione tissutale sono relativamente meno importanti, perché queste non hanno bisogno di un mediatore per effettuare il danno a livello del DNA; ciò ha un'implicazione clinica: se si deve irradiare una grossa massa tumorale con area centrale ipossica, se X-ray Y ray possibile si sceglierà di utilizzare radiazioni direttamente ionizzanti, poiché l'utilizzo delle indirettamente ionizzanti sarebbe altamente inefficiente.
Sia nel caso delle radiazioni corpuscolari, che agiscono direttamente e per le quali le condizioni di ossigenazione tissutale sono relativamente meno importanti, sia nel caso di fotoni, che agiscono indirettamente, il danno si verifica sempre per lesioni a carico del DNA.
H OH X ray Y ray O -H+ PH H OHS
Danni molecolari e mortalità cellulare
Si possono verificare fondamentalmente due tipi di danno a livello cellulare:
- Danno non riparabile o danno letale, che porta alla morte della cellula;
- Danno riparabile o danno sub-letale, che di per sé non comporta morte cellulare e che si verifica esclusivamente in seguito all'accumulo di un certo numero di danni sub-letali, superando una soglia critica oltre la quale il danno non può più essere riparato.
Ne deriva che esistono due tipi di mortalità cellulare in seguito ad una dose di radiazioni:2 di 11
Corso di Laurea in Medicina e Chirurgia - Radioterapia #13 - Prof. Arcangeli - Effetti biologici delle radiazioni ionizzanti: implicazioni in ambito oncologico
- da colpo singolo (danno letale);
- da colpi multipli (più danni sub-letali che, sommati, oltrepassano la soglia critica).
Fattori determinanti gli effetti biologici delle radiazioni
Gli effetti delle radiazioni sulle cellule dipendono da diversi fattori: la qualità delle radiazioni (basso o alto LET), la suscettibilità tissutale intrinseca, le condizioni ambientali (ossigenazione, temperatura) e l'utilizzo di alcuni farmaci che possono aumentare o meno la suscettibilità tissutale. In ogni caso, la risposta delle cellule alle radiazioni ionizzanti è espressa mediante la curva dose-risposta, che indica la percentuale di cellule sopravviventi a diverse dosi di radiazioni ionizzanti; utilizzando questa curva si misura la capacità clonogenica.
Questa curva dose-risposta è la medesima per cellule tumorali e sane; in particolare troviamo sull'asse delle ascisse la dose di radiazione e sull'asse delle ordinate la frazione di cellule sopravvissute ad essa.
I parametri che influenzano tale curva, come già accennato, sono:
- Tipo di radiazione utilizzata
- Popolazione cellulare
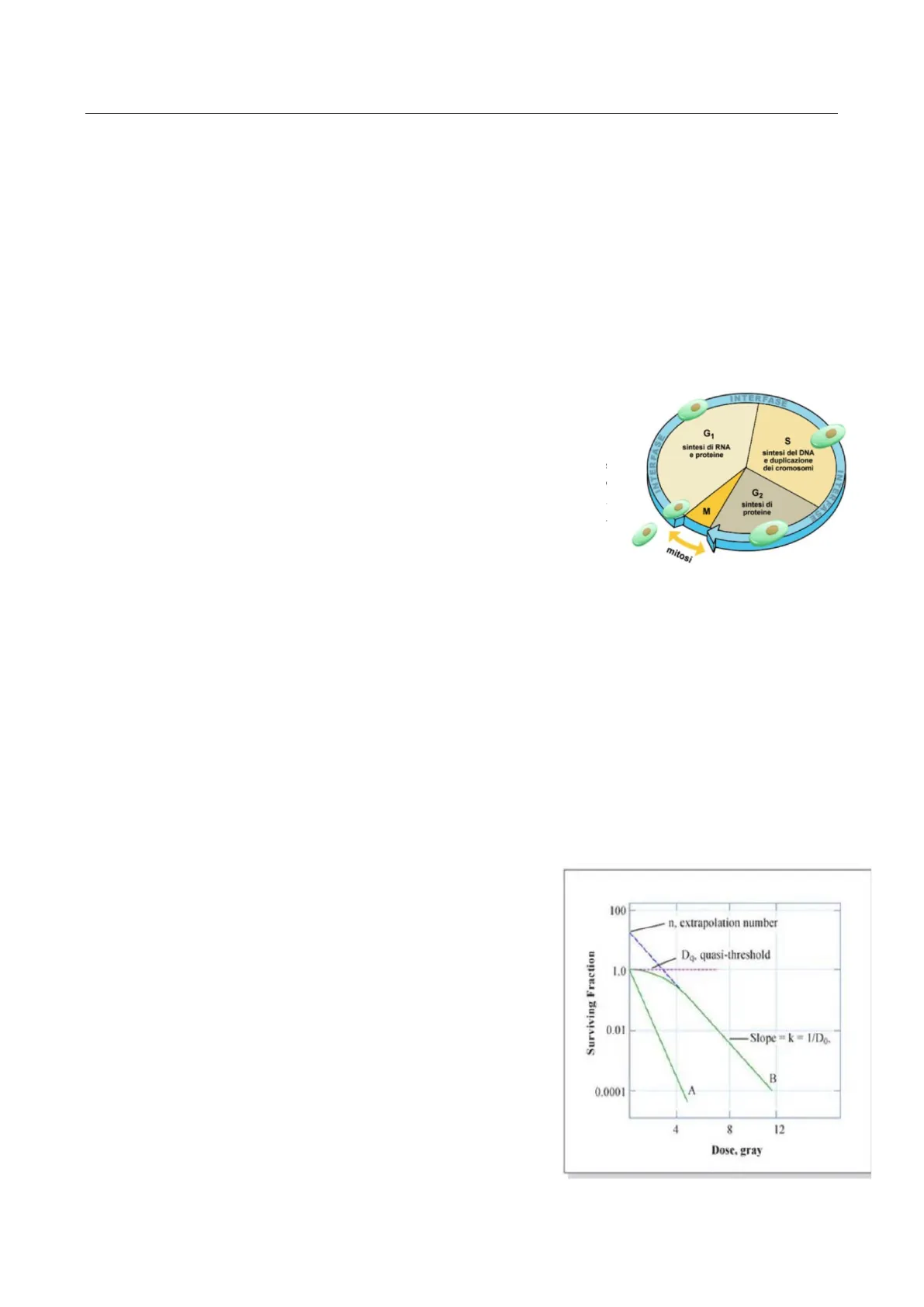
- Radiosensibilità intrinseca, che ha a che vedere con la probabilità che le cellule del tessuto irradiato si trovino in una determinata fase del ciclo cellulare; si ricordi che la fase G2 e la fase M sono quelle in cui le cellule sono più radiosensibili, poiché durante la mitosi il DNA è più esposto; ne consegue che tutti i tessuti (compresi quelli tumorali) con ritmo proliferativo molto elevato hanno più probabilità che le cellule che li costituiscono si trovino in fase di replicazione, in cui il DNA è più vulnerabile, più esposto e più suscettibile al danno;
- Condizioni ambientali di temperatura e di ossigeno
- LET, ovvero l'energia trasferita per unità di misura.
INTERFASE G. S sintesi di RNA e proteine sintesi del DNA e duplicazione dei cromosomi INTE M G2 sintesi di proteine ERFASE mitosi
LET e efficacia biologica relativa
In base al LET (ovvero l'energia trasferita per unità di misura nella traiettoria percorsa dalle radiazioni) si distinguono radiazioni ad alto LET che sono radiazioni direttamente ionizzanti, corpuscolate (al trasporto di energia si associa il trasporto di materia) e radiazioni a basso LET, ovvero i fotoni, raggi X e gamma, che sono quelli impiegati più spesso nella pratica clinica (90% delle radiazioni utilizzate).
Da questo parametro deriva il concetto di efficacia biologica relativa (EBR), poiché a parità di dose assorbita l'efficacia biologica relativa dipende dal LET: le radiazioni a basso LET distribuiscono le ionizzazioni in forma sparsa, quelle ad alto LET, ovvero ad alta densità di ionizzazione, concentrano le ionizzazioni nello spazio e quindi, sono capaci di provocare un danno più efficiente. Dunque le radiazioni ad alto LET hanno una maggiore EBR a parità di dose assorbita. Le prime sono radiazioni indirettamente ionizzanti, ovvero più penetranti ma in grado di causare un danno più spesso riparabile, mentre le seconde sono 100 radiazioni direttamente ionizzanti, poco penetranti, ma in grado di n, extrapolation number concentrare molto gli eventi ionizzanti nella traiettoria del volume Dq. quasi-threshold che attraversano: l'iperconcentrazione di questi ultimi nello spazio 1.0 determina quasi sempre inevitabilmente un danno letale.
L'efficacia biologica relativa è pertanto il rapporto tra la dose della radiazione di riferimento (in radioterapia è sempre considerata la radiazione fotonica a basso LET) e la dose della radiazione oggetto di studio: per esempio, l'efficacia biologica relativa di una particella corpuscolare è superiore a quella di un fotone, quindi è una radiazione qualitativamente più efficiente.
Surviving Fraction 0.01 -Slope = k= 1/Do. B 0.0001 A 4 8 12 Dose, gray3 di 11
Corso di Laurea in Medicina e Chirurgia - Radioterapia #13 - Prof. Arcangeli - Effetti biologici delle radiazioni ionizzanti: implicazioni in ambito oncologico
Quindi 1 Gy è uguale a 1 Sievert se si utilizzano radiazioni elettromagnetiche, mentre 1 Gy è uguale a 20 Sv per una radiazione per esempio a, che ha un'elevata EBR. In base al LET la curva dose-risposta si modifica, come già anticipato.
Effetto delle RI in funzione del LET 1 Surviving Fraction 10-1 10-2 Low-LET 10-3 High-LET 10-4 Dose FIG. 6-17. Cell survival curves for the same cell line irradiated with both low- and high-LET radiation. For low-LET radiation a "shoulder" to the curve at lower doses indicates the cell's abil- ity to repair some damage at low doses. High-LET radiation typ- ically has no shoulder, indicating that little or no repair takes place UNIVERSITA' BICOCCA
La curva dose-risposta delle radiazioni ionizzanti
Quando si irradiano cellule eucariotiche con radiazioni ionizzanti a basso LET, la mortalità cellulare rappresentata graficamente è espressa da una curva esponenziale che presenta un tratto iniziale a minor pendenza, la cosiddetta "spalla". Essa rappresenta una minor mortalità per le basse dosi, ovvero la fase in cui si stanno accumulando i danni sub-letali; quando si supera la soglia critica, la mortalità è tutta per letalità da colpo singolo. L'entità della "spalla" dipende dalla capacità di riparare il danno sub-letale: tanto più ampia è questa fase iniziale, tanto più i tessuti sono in grado di riparare il danno sub-letale. La curvatura nella zona corrispondente alle dosi più basse, quindi, indica una minore efficienza degli effetti delle radiazioni ionizzanti a basse dosi. La linea retta del grafico o 'pendenza esponenziale' invece, indica che progressivi livelli di dose inducono una progressiva riduzione della CURVA DOSE-RISPOSTA capacità di riparare danni cellulari e quindi n Do: dose efficace media progressivo danno cellulare.
Osservando la morfologia della curva dose-risposta si è in grado di stabilire il tipo di radiazioni utilizzate: la spalla è caratteristica delle radiazioni indirettamente ionizzanti, a basso LET; invece per le radiazioni ad alto LET, direttamente ionizzanti e in grado di indurre un danno letale senza possibilità di riparazione, l'effetto è descritto da una retta priva della tipica curvatura iniziale, indice del fatto che la capacità di riparazione del danno letale è pressoché nulla e la relazione dose-risposta è unicamente lineare.
D. q spalla n: numero di estrapolazione (numero di bersagli presenti nella cellula) Da: dose quasi soglia 0,1 1/e 0,01 Regione esponenziale finale pendenza = 1/Do D 0,001 DOSE -
Architettura tissutale e tolleranza dei tessuti alle radiazioni
L'effetto delle radiazioni ionizzanti dipende anche dall'architettura tissutale, ovvero dall'organizzazione delle subunità funzionali, diversa tra tessuto e tessuto. In base all'architettura tissutale dunque si distinguono due categorie di tessuti:
- I tessuti late-responders, anche chiamati tessuti seriali: da un punto di vista radiologico si comportano come una catena, dunque il danno in un punto determina sempre una perdita di funzione.
- I tessuti early-responders, in cui prevale una componente parallela: da un punto di vista radiologico si comportano come una fune: anche se viene persa una piccola parte può esservi mantenimento della funzione.
I tessuti seriali o late-responders sono implicati nella patogenesi della tossicità tardiva, mentre tessuti a risposta rapida sono implicati nella patogenesi della tossicità acuta. Dunque il pattern di comparsa delle reazioni, acute o tardive, dipende dal tipo di tessuto che viene incontrato; ciò ha delle implicazioni cliniche, perché non è detto DEGLI STUDI DI MILANO 1