Farmacologia clinica: trattamento del diabete di tipo II e metformina
Documento di Rossi, Rossi, Sciscio, Silvestrin su Farmacologia clinica (Pea). Il Pdf esplora il trattamento del diabete di tipo II, le classi di farmaci antidiabetici e il loro meccanismo d'azione, con un focus sull'uso della metformina e le sue controindicazioni, utile per studenti universitari di Biologia.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
DIABETE DI TIPO II
Il trattamento del diabete di tipo II è più complesso. Come già detto, le prime due classi di farmaci, di cui si ha avuto disponibilità a partire dagli anni 50', sono state le sulfaniluree e i biguanidi. A quest'ultima famiglia appartiene la Metformina, l'unica ancora usata oggi mentre tra le sulfaniluree sono citate la Clorpropamide e la Tolbutamide. Oggi giorno sono stati soppiantati da una serie di sulfaniluree di seconda generazione (in particolare Gliclazide) e più recentemente dagli inibitori dell'a- glicosidasi (Acarbose), dagli inibitori DPP4 (Sitagliptin, Saxagliptin), dagli agonisti GLP-1 (Exanatide, liraglutide) e dagli inibitori di SGLT2 (Canagliflozin, Dapagliflozin, Empagliflozin). In questo scenario molto vasto bisogna cercare di capire pregi e difetti di ciascuna di queste classi di farmaci al fine di capire qual è la logica, da un punto di vista clinico, per cui questi farmaci vengano utilizzati all'interno di un piano terapeutico di un paziente diabetico.
I farmaci possono avere due tipi di influenza sull'azione dell'insulina:
- influenza a livello pancreatico, nel senso che viene promossa la secrezione di insulina;
- sensibilizzazione dei recettori periferici nei confronti dell'insulina;
Qual è la via più sicura tra le due? La via più sicura risulta essere la sensibilizzazione all'insulina perché presenta un minore rischio di ipoglicemia; infatti, i farmaci insulino-secretagoghi hanno il rischio di causare picchi ipoglicemici, cosa che non avviene con farmaci insulino-sensibilizzanti. Se si pensa infatti alla storia della farmacologia del paziente diabetico, i farmaci più utilizzati per 40 anni sono stati la metformina (insulino-sensibilizzante) e le sulfaniluree (insulino-secretagoni) appunto perché per mantenere un controllo della glicemia adeguato è necessario combinare più farmaci; parliamo infatti di terapie complesse che tuttavia al giorno d'oggi, grazie alle diverse classi di farmaci di cui disponiamo, portano ad una risposta più concreta e sicura.
Si procede quindi con la descrizione dei Biguanidi.
METFORMINA
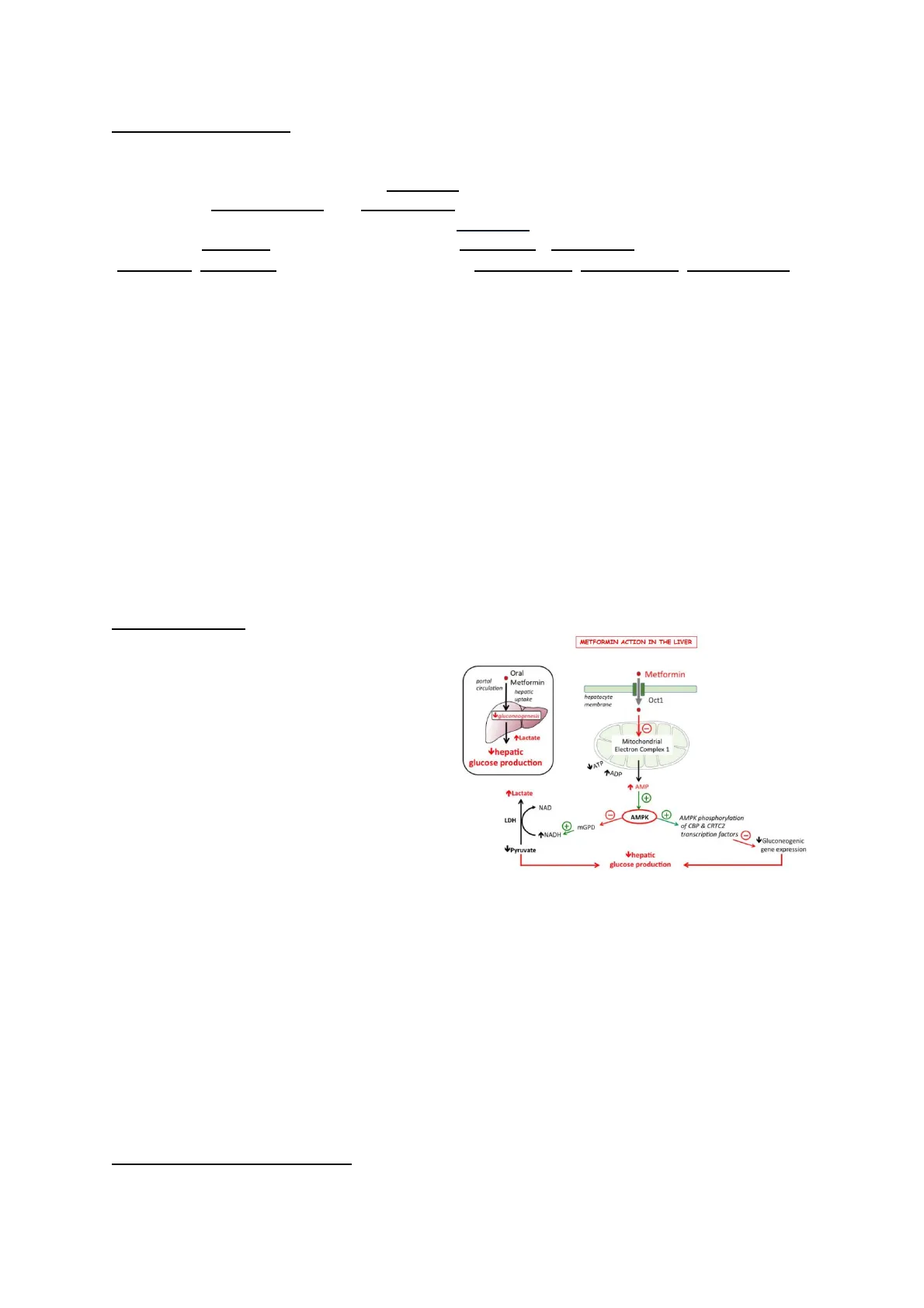
La metformina è un farmaco che migliora la sensibilità insulinica. In che modo? In realtà, anche se viene utilizzata in terapia da ormai 70 anni, non si è ancora riusciti bene a capire in che modo riesca a migliorare la sensibilità all'insulina; tuttavia, l'ipotesi più accreditata è quella riportata nell'immagine qui a dx. La metformina, infatti, viene captata a livello epatico (sia per diffusione passiva, sia ad opera di trasportatori specifici) ed all'interno dell'epatocita è in grado di inibire la produzione di ATP a livello mitocondriale, causando una maggiore disponibilità di cAMP.
METFORMIN ACTION IN THE LIVER
Il cAMP stimola delle chinasi specifiche ad espletare la loro duplice funzione:
- ridurre l'espressività dei geni responsabili della gluconeogenesi;
- promuove la conversione del NADH nella sua forma ossidata: in questo modo riducono la produzione di piruvato e facilitano la produzione di lattato;
Congiuntamente questi due meccanismi hanno l'effetto di ridurre la produzione di glucosio a livello epatico. In sintesi, possiamo dire che nei pazienti in cui viene usata la metformina si viene a creare una riduzione della produzione di glucosio a livello epatico, ma il rovescio della medaglia a cui dovremo prestare attenzione sarà il fatto che questo meccanismo induce un aumento nella produzione dei lattati. Con questo schema in mente ci rendiamo conto che la metformina è un farmaco prezioso, insulino- sensibilizzante, dal costo irrisorio, ma che ha un rischio di iperlattacidemia che è una condizione incompatibile con la vita.
Caratteristiche della metformina
La metformina è un farmaco che utilizziamo per via orale, ha una buona biodisponibilità, ha il limite di avere un'emivita relativamente breve intorno a 6 ore, quindi nella sua formulazione standard, che è stata per lungo tempo l'unica disponibile, viene data praticamente ogni 8 ore (in realtà ci sono anche delle formulazioni che consentono un po' di superare questo limite). L'aspetto che ci interessa è il fatto che questo farmaco viene eliminato per via renale: questo ci porta a pensare che, dato il rischio legato all'iperlattacidemia, nei pazienti che hanno insufficienza renale la dose di metformina dovrà essere ridotta, e se l'insufficienza renale è grave, la metformina non va usata. Questo concetto naturalmente può essere esteso anche ad altri fattori di rischio come l'insufficienza epatica o lo scompenso cardiaco ed inoltre ci dà modo di introdurre un argomento importante che affronteremo probabilmente nelle ultime lezioni del corso, che è l'uso degli antibiotici per la terapia della sepsi.
Digressione sulla SEPSI
La sepsi è una sindrome clinica, non è una patologia d'organo specifica, che ha come caratteristica principale quella di indurre sulla base di uno stimolo infettivo, spesso di natura batterica, una tempesta citochinica cioè vengono liberate molte citochine proinfiammatorie che hanno un'effetto devastante nella funzionalità dell'organo, e possono portare a una MOF (Multiple Organ Failure); quindi si potranno verificare un'insufficienza epatica, un'insufficienza renale, uno scompenso cardiaco, un danno a livello cerebrale, ecc. Questa condizione è grave dal punto di vista clinico, ma tornando al concetto della gestione della metformina, è una condizione che può promuovere un'acidosi lattica. Quindi se un paziente, che è in terapia con metformina, sviluppa una sepsi, la terapia con metformina va sospesa, poiché altrimenti ci sarebbe un rischio molto importante di acidosi lattica.
Utilizzo di metformina in condizione di insufficienza renale cronica
In questo studio si è fatta una valutazione del rischio di acidosi lattica in relazione ai pazienti che utilizzavano la metformina in presenza di una comorbidità come l'insufficienza renale cronica. Quindi quello che è stato fatto è che si è andati a vedere quale fosse il rischio, in relazione a quelle che erano la le varie fasce d'età, di insorgenza di acidosi in pazienti in trattamento con metformina. I risultati di questo studio constatavano un rischio aumentato di acidosi lattica nei pazienti che avevano insufficienza renale grave (dove per insufficienza renale grave si intende una funzione renale inferiore a 30 ml/min/1.73m2). Ecco il motivo per il quale questo valore viene indicato come il limite di funzionalità renale per controindicare l'uso della metformina in ambito di terapia antidiabetica. In altre parole, in quei soggetti che hanno l'insufficienza renale con valori di creatinina inferiori a 30 non si può, anche da un punto di vista medico-legale, utilizzare la metformina. Questo indica che chi mette un paziente in terapia con metformina deve prima avere l'accortezza di valutare la funzionalità renale del paziente.
JAMA Internal Medicine | Original Investigation
Association of Metformin Use With Risk of Lactic Acidosis Across the Range of Kidney Function A Community-Based Cohort Study Benjamin Lazarus, MBBS, MPH: Aozhou Wu. MHS: Jung-Im Shin, MD, PHD; Yingying Sang, MS. G. Caleb Alexander, MD, MS; Alex Secora, MPH: Lesley A. Inker, MD, MS: Josef Coresh, MD, PhD); Alex. R. Chang, MD, MS: Morgan E. Grams, MD, PHD JAMA Intern Med. 2018;178(7):903-910. Published online June 4, 2018. DESIGN, SETTING, AND PARTICIPANTS Community-based cohort of 75 413 patients with diabetes in Geisinger Health System, with time-dependent assessment of eGFR stage from January 2004 until January 2017. Results were replicated in 67578 new metformin users and 14 439 new sulfonylurea users from 2010 to 2015, sourced from 350 private US health systems. RESULTS In the primary cohort (n = 75 413), mean (SD) patient age was 60.4 (15.5) years, and 51% (n = 38 480) of the participants were female. There were 2335 hospitalizations with acidosis over a median follow-up of 5.7 years (interquartile range, 2.5-9.9 years). Compared with alternative diabetes management, time-dependent metformin use was not associated with incident acidosis overall (adjusted hazard ratio [HR], 0.98; 95% CI, 0.89-1.08) or in patients with eGFR 45 to 59 ml/min/1.73 m2 (adjusted HR, 1.16: 95% CI, 0.95-1.41) and eGFR 30 to 44 ml/min/1.73 m2 (adjusted HR. 1.09: 95% CI, 0.83-1.44). On the other hand. metformin use was associated with an increased risk of acidosis at eGFR less than 30 mL/min/1.73 m2 (adjusted HR, 2.07, 95% CI, 1.33-3.22). Results were consistent when new metformin users were compared with new sulfonylurea users (adjusted HR for eGFR 30-44 mL/min/1.73 m2, 0.77: 95% CI. 0.29-2.05), in a propensity-matched cohort (adjusted HR for eGFR 30-44 mL/min/1.73 m2, 0.71; 95% CI, 0.45-1,12), when baseline insulin users were excluded (adjusted HR for eGFR 30-44 mL/min/1.73 m2, 1.16: 95% CI, 0.87-1.57), and in the replication cohort (adjusted HR for eGFR 30-44 ml/min/1.73 m2, 0.86; 95% CI, 0.37-2.01). CONCLUSIONS AND RELEVANCE In 2 real-world clinical settings, metformin use was associated with acidosis only at eGFR less than 30 ml/min/1.73 m2. Our results support cautious use of metformin in patients with type 2 diabetes and eGFR of at least 30 ml/min/1.73 m2.
Conseguenze dell'acidosi lattica
Quali possono essere le conseguenze? Questa è una osservazione fatta in Italia con uno studio retrospettivo, che analizza circa 6 anni di utilizzo della metformina in alcune realtà del Nord-Ovest italiano (Piemonte e Valle D'Aosta), relativo a un campione di oltre 140.000 soggetti. L'incidenza di acidosi lattica grave riportando i pazienti in terapia intensiva (quindi situazioni Blood Pul. 2017:44(3):18-205. doi: 10.1159/000471917. Epub 2017 Jul 1. Metformin-Associated Lactic Acidosis Undergoing Renal Replacement Therapy in Intensive Care Units: A Five-Million Population-Based Study in the North-West of Italy. Mariano E1. Pozzato M, Inguaggiato P. Guarena C, Turello E. Manes M. David P. Berutti S. Consiglio V. Amore A. Campo A. Marino A. Berto M. Carpani P. Calabrese G. Gherzi M. Stramignoni.E. Martina G. Serra.A. Comune.L. Roscini.E. Marciello.A. Todini V. Vio.P. Eiliberti Q. Boero B. Cantaluppi.V. @ Author information Abstract BACKGROUND: Metformin-associated lactic acidosis (MALA) is a severe complication of drug administration with significant morbidity and mortality. So far no study in large population areas have examined the incidence, clinical profile and outcome of acute kidney injury (AKI)- MALA patients admitted in intensive care units (ICUs) and treated by renal replacement therapy (MALA-RRT). METHODS: Retrospective analysis over a 6-year period (2010-2015) in Piedmont and Aosta Valley regions (5,305,940 inhabitants, 141,174 diabetics treated with metformin) of all MALA-RRT cases. RESULTS: One hundred and seventeen cases of AKI-MALA-RRT were observed (12.04/100,000 metformin treated diabetics, 1.45% of all RRT-ICU patients). Survival rate was 78.3%. The average duration of RRT was 4.0 days at mean dialysis effluent of 977 mL/kg/day. At admission most patients were dehydrated, and experienced shock and oliguria CONCLUSION: Our data showed that MALA-RRT is a common complication, needing more prevention. Adopted policy of early, extended, continuous and high efficiency dialysis could contribute to an observed high survival rate. Video Journal Club "Cappuccino with Claudio Ronco" at http://www.karger.com/?doi=471917. · 2017 S. Karger AG, Basel.