Completamento di ematologia del Dr. Lorenzo Iovino: patologie del sangue
Documento del Dr. Lorenzo Iovino su completamento di ematologia. Il Pdf, adatto a studenti universitari di Biologia, descrive patologie del sangue come neoplasie linfoidi, mieloma multiplo, leucemie acute e sindromi mielodisplastiche, con diagnosi e terapie.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Indice delle Neoplasie Ematologiche
- Neoplasie linfoidi e mieloma multiplo
- Linfomi
- Tumori della cellula staminale emopoietica
- Leucemie acute
Esistono due esami diagnosti invasivi largamente utilizzati:
- Biopsia osteomidollare (BOM) consiste nel prelievo di un frustolo di osso spugnoso contenente quindi il midollo ematopoietico (carotaggio). Generalmente viene effettuato nella cresta iliaca postero superiore. Il cilindro viene sottoposto quindi a esame istologico. Consente di vedere tutte le cellule, l'organizzazione architettonica, lo stroma e le trabecole ossee.
- Mieloaspirato: prelievo del sangue midollare. È un esame citologico. Le cellule sono in sospensione, per cui non si hanno informazioni architetturali ma essendo le cellule più separate tra loro possono essere viste nella loro singola citologia.
Sono due esami complementari.
Neoplasie Linfoidi
Sono neoplasie che nascono dai linfociti:
- Maturi (linfocita T/B o plasmacellula)-> malattie linfoidi o linfoproliferative o generalmente linfomi o mielomi
- Staminale ematopoietica, ovvero precursore ematopoietico che risiede nel midollo osseo.
Il linfoma è un tumore del linfocita non del linfonodo, benchè la presentazione più frequente sia di masse linfonodali. Non tutti i linfomi però hanno necessariamente il coinvolgimento dei linfonodi come nel caso dei linfomi cerebrali, linfomi cutanei, linfoma MALT gastrico (nasce nello spessore della parete gastrica da formazioni linfoidi intercalate), linfoma di Burkitt nella forma endemica (si localizza nel ramo della mandibola), linfomi con localizzazione nel midollo osseo e linfomi leucemizzati.
Le neoplasie vengono distinte nella classificazione WHO in base alla COO ovvero cell of origin:
- Neoplasie che derivano dai linfociti B maturi tra cui troviamo le discrasie plasmacellulari
- Neoplasie che derivano dai linfociti T maturi
- Istiocitosi
- Malattie linfoproliferative del post-trapianto
- Linfoma di Hodgkin.
L'80% dei linfomi sono malattie linfoproliferative a cellule B.
Quando il linfocita B naive incontra l'antigene si attiva nei centri germinativi linfonodali differenziando poi in cellule B della memoria e plasmacellula.
A seconda dello stadio maturativo del linfocita B in cui insorge la mutazione genetica, ci sarà l'insorgenza di diversi linfomi. L'80% dei linfomi origina nel centro germinativo, altri originano pre o post centro germinativo
Gammopatia Monoclonale di Incerto Significato (MGUS)
La MGUS caratterizzata da un picco nella regione gamma a banda stretta all'elettroforesi sierica. Questa deve essere sempre indagata per clonalità, infatti per avere la conferma di gammopatia mono o policlonale si esegue l'immunofissazione sierica e urinaria.
Le gammopatie monoclonali fanno parte dei tumori ematologici ma non tutte hanno significato certamente tumorale.
573 Document shared on https://www.docsity.com/it/materiale-per-la-preparazione-al-concorso-ssm/10411263/La MGUS di nuova scoperta deve essere indagata per escludere la presenza di un tumore ematologico sottostante.
- EO e ecografia delle stazioni linfonodali (alcune gammopatie sono di accompagnamento ai linfomi)
- Calcemia, creatininemia, emocromo, studio dello scheletro (RX, PET, RM, TC), dosaggio delle catene legge libere (free light chain FLC)
Criteri di sospetto: componente monoclonale che aumenta nel tempo o prossima a 3 g/dl >la MGUS è la presenza di una componente monoclonale confermata all'immunofiossazione sierica e/o urinaria in assenza di criteri diagnostici di linfoma (infiltrato plasmacellulare < 10% della popolazione cellulare midollare alla biopsia midollare), mieloma (criteri SLIM CRAB) e amiloidosi. È quindi un'alterazione laboratoristica.
Può essere transitoria come negli stati post infettivi, post-trapianto di organo solido, malattie autoimmuni.
Le MGUS hanno una tendenza non prevedibile all'evoluzione nel tempo. In alcuni casi sono forme precancerose di mieloma e linfoma
Le MGUS da IgG sono le più frequenti ed hanno prognosi migliore.
Se la componente monoclonale è di IgA, il rischio di progressione a mieloma multiplo è maggiore.
Il discorso è a parte in caso di componente monoclonale IgM.
Il rischio di MGUS di progressione a mieloma multiplo è dell'1% annuo per i primi 10 anni e poi 0,5% per i successivi anni. Inoltre è possibile la comparsa di linfomi.
L'MGUS non richiede alcun trattamento, solo il follow-up ogni 6 mesi
Se la componente monoclonale aumenta oppure compaiono altre alterazioni di laboratorio, il paziente deve essere rivalutato da capo con le indagini.
Essendo una patologia dell'anziano generalmente nella pratica clinica I'MGUS non viene sottoposto a biopsia midollare
Esiste anche un criterio istologico alla biopsia osteomidollare che consente di distinguere la MGUS dal mieloma multiplo: I'MGUS è caratterizzata da un riscontro di plasmacellule < 10%.
Mieloma Multiplo
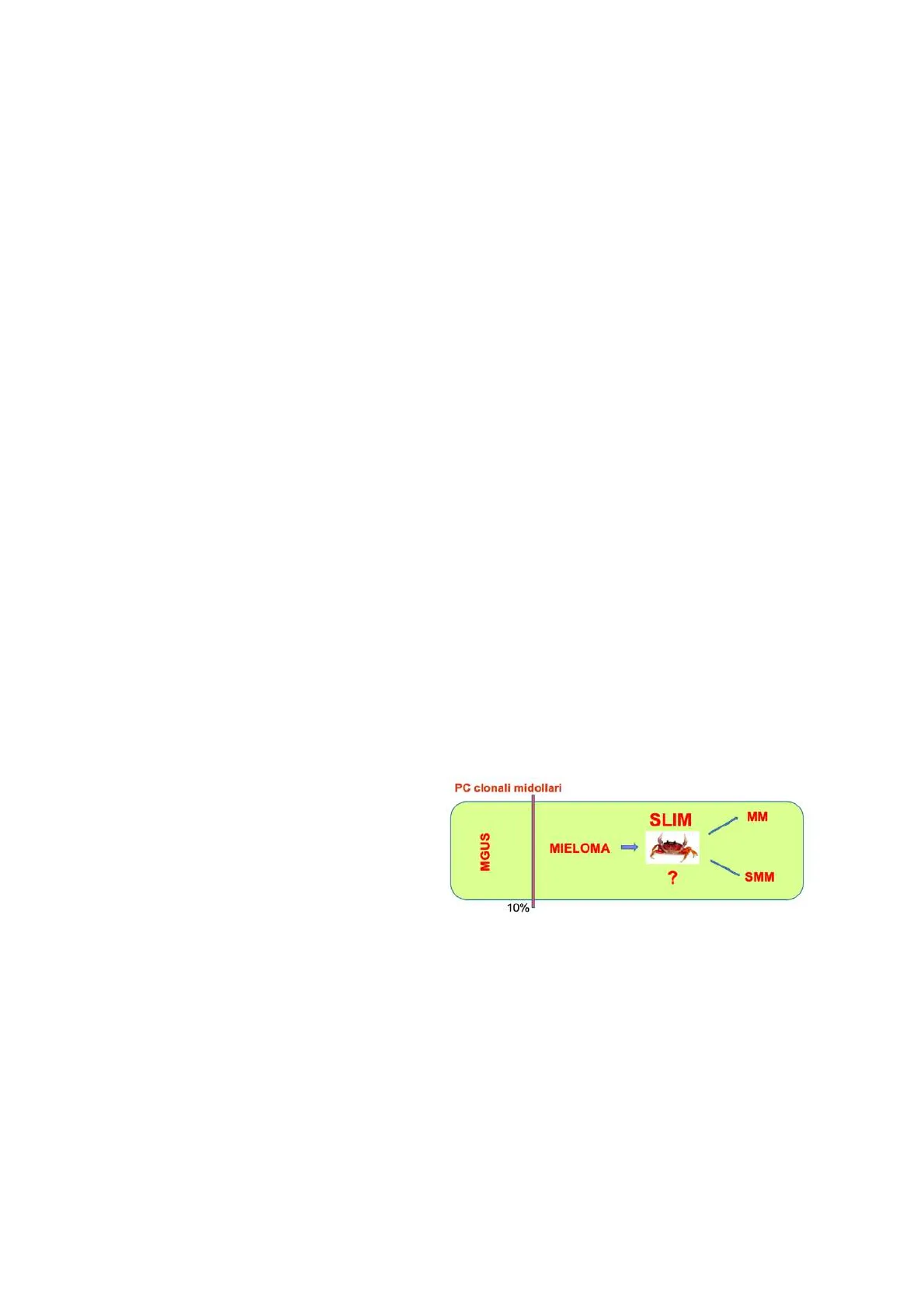
Il mieloma multiplo (MM) è un a proliferazione di plasmacellule maligne che costituiscono > 10% della cellularità midollare alla biopsia osteomidollare. Si associa ad una componente monoclonale in circolo: intera (catena pesante + catena leggera), a catene eleggere (MM PC clonali midollari SLIM MM MGUS MIELOMA ? SMM 10% micromolecolare), a catene pesanti (raro) o non secernente.
Il MM può essere asintomatico oppure sintomatico quando è presente almeno uno degli indicatori di danno d'organo chiamati "criteri SLIM CRAB".
SLIM: sixty (>60% plasmacellule midollari), Light Chain (FLC: il rapporto tra una catena e l'altra deve essere >100 o <0,1), IMaging (ad un'indagine radiologica dello scheletro di II livello quindi PET, RM e TC il soggetto deve avere più di 2 lesioni osteolitiche).
CRAB ipercalcemia, insufficienza renale, anemia e lesioni ossee.
Il MM asintomatico o SMM (smoldering mieloma multiplo) è quindi definito dall'assenza dei criteri SLIM CRAB. Il 25% di questi evolve in mieloma sintomatico
Nel MM non secernente è presente l'infiltrato midollare, le alterazioni ematiche e le caratteristiche lesioni osteolitiche, ma non è presente il picco monoclonale.
574 Document shared on https://www.docsity.com/it/materiale-per-la-preparazione-al-concorso-ssm/10411263/Talvolta nel MM può essere presente l'ipogammaglobulinemia perché la produzione di anticorpi irregolari ruba la produzione di anticorpi sani: tanta componente monoclonale ma poche Ig sane.
Nel MM micromolecolare si riscontra ipogammaglobulinemia perché le catene leggere passano il filtro glomerulare e la componente monoclonale sarà nelle urine con alto dosaggio di proteinuria visto che le Ig sono proteine.
Le lesioni osteolitiche sono destruenti, prive dell'orletto reattivo a differenza delle metastasi da organo solido. Causano dolore e localizzazione multipla.
Il MM causa insufficienza renale perché il rene viene sovraccaricato dal filtraggio della componente monoclonale (soprattutto nella forma micromolecolare), sul rene insiste l'ipercalcemia (legata alla lisi ossea), l'accumulo di catene k e 2 nel rene si trasforma in proteina amiloide, portando negli anni ad amiloidosi renale
La diagnosi è con BOM e mieloaspirato che mostrano > 10% di plasmacellule. Il mieloaspirato è utile per fare fenotipo, biologia molecolare e cariotipo.
Nel midollo osseo ci sono tante plasmacellule e questo giustifica l'anemia
Di fronte ad una MGUS o di un'ipogammaglobulinemia deve essere fatto lo studio dello scheletro (RX, TC, RMN, PET) e emocromo, calcemia, creatininemia.
Plasmocitoma solitario: unica massa ossea ma senza un quadro midollare di mieloma multiplo o altri segni clinici di mieloma multiplo. "tutto il mieloma che trovo è solo in quella lesione". Il tasso di evoluzione a MM è del 25% annuo
Stadiazione del Mieloma Multiplo
Stadiazione di Durie e Salmon
Essa tiene conto di parametri laboratoristici come emoglobina, calcemia, componente monoclonale e numero di lesioni ossee. È correlato con la prognosi e sopravvivenza.
Basta un solo parametro per slittare di stadio.
Tabella 2. Stadiazione di Durie e Salmon
Stadio Parametri
- Emoglobina >10 g/dl Calcemia normale Unica lesione ossea lgG<5 g/dl; IgA< 3 g/dl; BJ <4 g/24 ore
- Criteri non soddisfatti negli stadi I e II Emoglobina <8,5 g/dl Calcemia >12 mg/dl Gravi lesioni ossee lgG>7 g/dl; lgA>5g g/dl; BJ >12 g/24 ore
Sistema di Stadiazione Internazionale (ISS)
L'ISS tiene conto della ß2microglobulina e dell'albumina. La ß2microglobulina è un marcatore di massa tumorale, l'albumina è una proteina normale che deve essere rappresentata.
Se la prima è ridotta e la seconda alta lo stadio è 1, nello stadio 3 avviene il contrario.
Criteri del sistema di stadiazione internazionale (ISS)
Stadio Criteri Definizione Sopravvivenza mediana (mesi)
- B2-M ridotta e albumina normale B2-M < 3,5 mg/l e albumina ≥ 3,5 g/dl 62
- Pazienti che non soddisfano i criteri per gli stadil o III B2-M < 3,5 mg/l e albumina < 3,5 g/dl o B2-M compresa fra 3,5 e <5,5 mg/l 44
- ₿2-M elevata B2-M ≥ 5,5 mg/l 29
575 Document shared on https://www.docsity.com/it/materiale-per-la-preparazione-al-concorso-ssm/10411263/Il MM ad alto rischio è definito dalla traslocazione (4;14) oppure delezione del cromosoma 17 p (chiesto dal ministero). Questo è indipendente dalla stadiazione.
Trattamento del Mieloma Multiplo
.il MM smoldering/asintomatico viene sottoposto a monitoraggio ogni 3 mesi .il MM sintomatico viene sottoposto a trattamento.
Nei soggetti < 70 anni e fit: associazione con inibitorori del proteasoma (bortezomib), immunomodulanti (talidomide o lenalidomide) e desametasone (VTD o VRD). Si utilizzano in 4-6 cicli e si cerca di ottenere una remissione almeno parziale con l'induzione, dopo di che viene fatto il trapianto singolo o doppio (due volte in successione) autologo.
Spesso ci sono recidive.
Nei soggetti > 70 anni o non fit: non possono essere sottoposti a trapianto autologo. Possono essere trattati con bortezomib, melfalan (chemioterapico) e prednisone con 16 cicli. In alternativa, terapia continuativa con lenalidomide e prednisone.
Nuovi Farmaci per il Mieloma Multiplo
Inibitori del proteasoma (carfizomib e ixazomib), nuovi immunomodulanti (pomalidomide), anticorpi monoclonali (daratumuma, elotuzumab che sono anti CD38. Si utilizzano nelle recidive o nel MM ad alto rischio o refrattario), terapia CART e anti BCMA
"Al ministero MGUS e mieloma piacciono"
Linfomi
I linfomi sono neoplasie dei linfociti che non riguardano la plasmacellula. Le mutazioni che riguardano le plasmacellule sono nell'ambito delle discrasie plasmacellulari.
In Occidente l'80% dei linfomi sono a cellule B. A questo gruppo appartiene anche il linfoma di Hodgkin.
Clinica dei Linfomi
- Linfoadenopatia superficiali e/o profonde. I linfonodi tendono ad essere tondeggianti, non dolenti e anecogeni. Viceversa i linfonodi reattivi sono allungati
- Splenomegalia
- Anemia normocitica e talvolta emolitica autoimmune come sindrome paraneoplastica
- Sintomi B: febbre (>38℃ in assenza di infezione), sudorazione profusa notturna, calo ponderale > 10% del peso corporeo in 3 mesi. Il prurito è spesso presente nel linfoma ma non identifica lo stadio B.
- Localizzazione midollare ossea: possibile piastrinopenia o leucemizzazione
- Possibile gammopatia di accompagnamento o ipogammopatia con infezioni opportunistiche.
La diagnosi dei linfomi localizzati è istologica con biopsia linfonodale escissionale.
In presenza di criteri di sospetto, linfonodo ingrossato da un mese non responsivo ad antibioticoterapia empirica, eseguire biopsia linfonodale (non agoaspirato).
La TC total body con mdc è utile per la stadiazione ma non per la diagnosi. Nei linfomi aggressivi alla diagnosi deve essere effettuata la TC o la RM encefalo per il sospetto di localizzazione cerebrale.
Nei soggetti con linfoma deve essere sempre effettuata BOM e mieloaspirato. Infatti fino a prova contraria i soggetti con linfoma hanno una localizzazione midollare.
Deve essere effettuato anche lo striscio di sangue periferico perché i linfomi leucemizzano e cioè mandano in circolo delle cellule atipiche che possono essere viste sul sangue periferico.
576 Document shared on https://www.docsity.com/it/materiale-per-la-preparazione-al-concorso-ssm/10411263/