Proteine: digestione, assorbimento e metabolismo nel corpo umano
Documento universitario sulle Proteine: digestione, assorbimento e metabolismo. Il Pdf, un set di appunti di Biologia per l'Università, esplora i processi biochimici e le molecole chiave come aminoacidi, creatina e carnitina, con dettagli su regolazione e implicazioni cliniche.
Mostra di più19 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
PROTEINE
Le proteine svolgono principalmente funzione strutturale, in secondo luogo funzione energetica, in quanto alcuni aminoacidi fanno da substrato per la gluconeogenesi. Fondamentale è anche la loro funzione bioregolatrice (molti neurotrasmettitori e ormoni sono di natura proteica).
DIGESTIONE E ASSORBIMENTO DELLE PROTEINE
DIGESTIONE
La digestione inizia a livello dello stomaco grazie al pH gastrico, che denatura le proteine (cambia la carica dei gruppi laterali, per cui la struttura si distende), rendendole facilmente attaccabili da enzimi, in questo caso la pepsina. A livello intestinale i polipeptidi sono scissi in oligopeptidi e aminoacidi da parte delle peptidasi pancreatiche, che vanno a formare aminoacidi liberi e di o tripeptidi (la catena della proteina non è completamente degradata). Si distinguono le endopeptidasi (tagliano all'interno della proteina, es. pepsina, tripsina, chimotripsina, elastasi) dalle esopeptidasi (tagliano a livello dell'estremità carbossilica o amminica, ec. carbossipeptidasi A e B).
ASSORBIMENTO
Gli aminoacidi non possono attraversare liberamente la membrana per via della carica (a pH neutro, che troviamo a livello dell'intestino, la porzione N terminale è tipicamente caricata positivamente, la C terminale è caricata negativamente; in più la catena laterale può non essere neutra). Gli aminoacidi penetrano nelle cellule dell'epitelio mediante meccanismi di trasporto attivo dipendenti o indipendenti dalla concentrazione di Na+. Il gradiente di sodio deve essere creato, ed è un meccanismo ATP-dipendente, per cui richiede energia; gli aminoacidi aromatici sono essenziali, motivo per cui l'assorbimento è indipendente dal sodio. I sistemi di trasporto sono specifici per: aminoacidi neutri; aminoacidi basici; aminoacidi bicarbossilici; glicina e prolina. Di e tripeptidi usano i sistemi di trasporto PEPT, che sfruttano il gradiente protonico - è un simporto con un protone. I protoni non possono accumularsi nell'enterocita, per cui poi dovranno essere eliminati. Nel neonato, per sopperire all'elevato fabbisogno proteico, dipeptidi e tripeptidi sono assorbiti per endocitosi. In alcuni casi sono assorbiti anche peptidi più grandi, e questo è alla base, ad esempio, dell'intolleranza al glutine.
REGOLAZIONE
A livello intestinale sono presenti dei recettori del gusto specifici per glucidi e aminoacidi (sapore umami, legato alla presenza di glutammato e ribonucleotidi come IMP), che servono ad attivare dei meccanismi per cui la digestione e l'assorbimento di questi nutrienti è favorito. Fanno questo:
- promuovendo il rilascio di colecistochinina > aumento della secrezione dei succhi gastrici > favorisce la digestione delle proteine;
- aumentando il senso della sazietà, in modo che non vengano ingeriti altri alimenti e si abbia il tempo di digerire e assorbire il pasto.
METABOLISMO DELLE PROTEINE
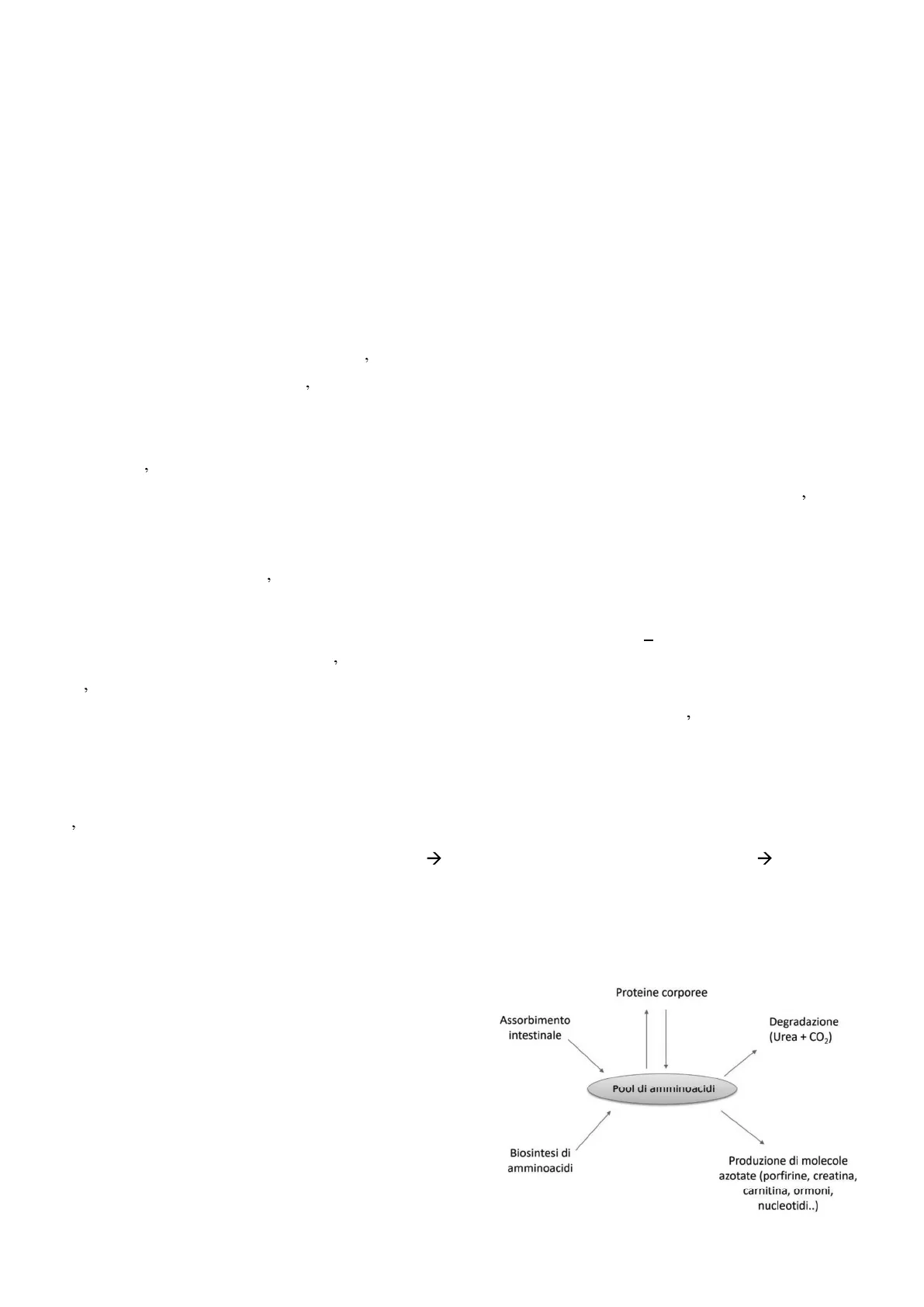
Le proteine assunte con la dieta non vengono immagazzinate ma vengono degradate a costituire il pool di aminoacidi liberi per la sintesi di altre proteine o composti azotati oppure vengono degradati a scopi energetici.
TURNOVER DELLE PROTEINE
Il turnover è un meccanismo costante, che riguarda tutte le molecole di natura proteica. La velocità di turnover dipende dalla funzione della proteina: si individuano infatti proteine a emivita breve, ovvero le proteine regolatrici (minuti-ore); 56proteine a emivita media (giorni-settimane); proteine a emivita lunga, ovvero le proteine strutturali (mesi-anni). Quindi, ad esempio, gli enzimi della gluconeogenesi avranno un turnover più veloce, in quanto devono essere degradati nel momento in cui l'effetto da loro prodotto non serve più, mentre il collagene ha un turnover molto più lento. L'organo che subisce meno turnover è il cuore; in un digiuno molto protratto il fegato può perdere il 50% delle proprie proteine, il muscolo il 30 % e il cuore il 3%. La degradazione proteica avviene principalmente a livello del fegato, in quanto questo organo deve regolare molti meccanismi in tempi anche brevi per garantire l'equilibrio metabolico dell'organismo. Il processo di turnover è finemente regolato dal sistema di ubiquitinizzazione, un segnale apposto alle proteine che devono essere degradate.
Reazioni a carico degli aminoacidi
Principalmente individuiamo: transaminazione, deaminazione e decarbossilazione.
TRANSAMINAZIONE
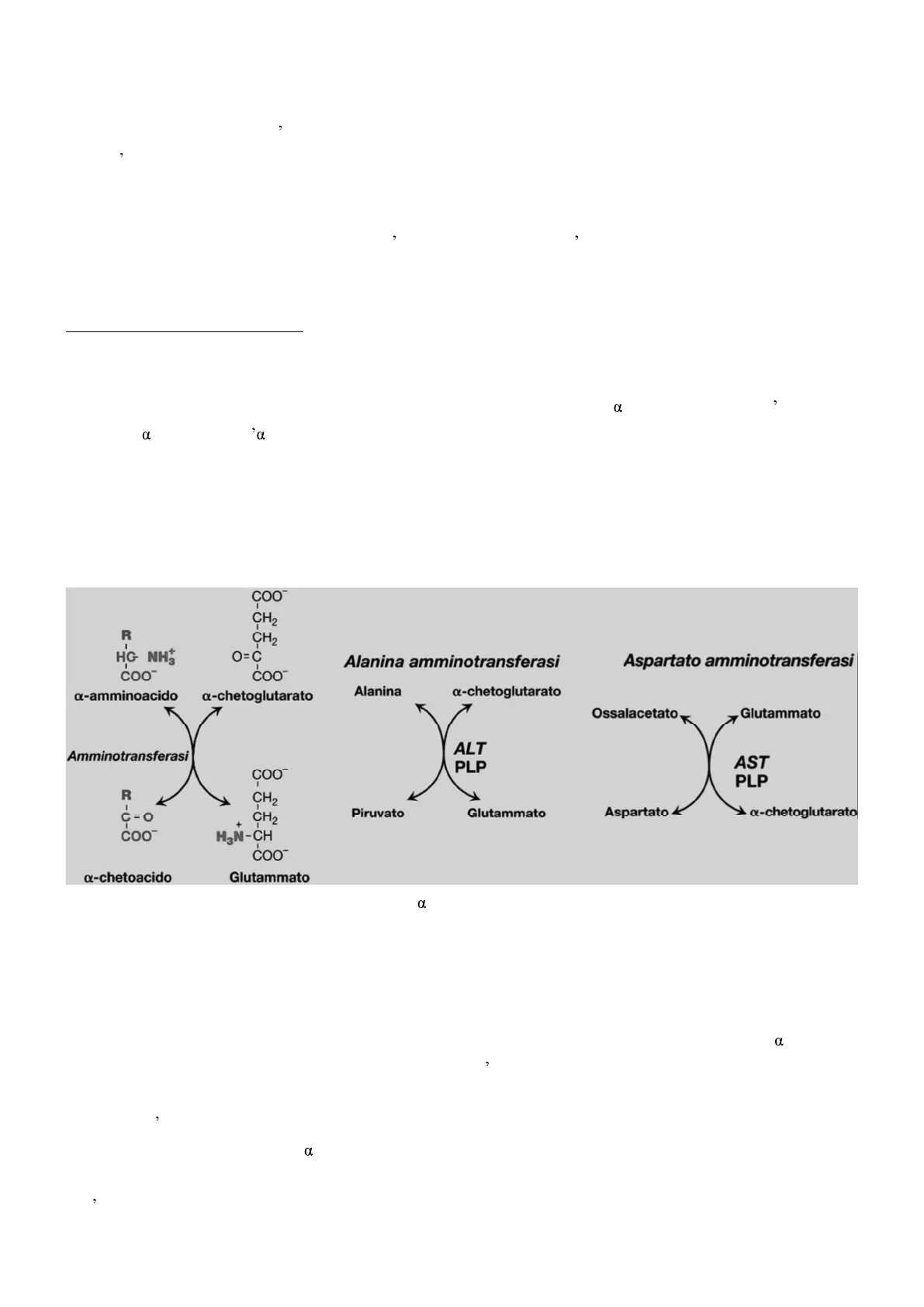
In questa reazione un gruppo amminico è trasferito da un aminoacido ad un a-chetoacido, per cui l'aminoacido diventa un a-chetoacido e l'a-chetoacido diventa un aminoacido. Si tratta di reazioni bidirezionali, il cui equilibrio è influenzato da vari fattori, e permettono di gestire il pool aminoacidico. Le transaminasi hanno infatti affinità molto bassa, il che significa che si attivano solo nel momento in cui si hanno elevati livelli di un determinato aminoacido. Le reazioni di transaminazione, quindi, permettono di ridistribuire il gruppo amminico fra gli aminoacidi ed è la stessa concentrazione di substrati e prodotti a direzionare la reazione. Diete ricche di proteine attivano la sintesi delle transaminasi a livello epatico ed intestinale.
Le transaminasi sono specifiche per ogni proteina e a-chetoacido, e le più conosciute solo la alanina aminotransferasi (GPT) e la aspartato aminotransferasi (GOT). Le transaminasi sono normalmente presenti in tracce a livello ematico; per questo, elevati livelli di GOT (AST) sono indice di lesione miocardica, mentre elevati livelli di GPT (ALT) sono indice di lesione epatica (le transaminasi si ritrovano nel sangue per rottura cellulare). Prolina, lisina, e treonina non sono suscettibili a reazioni di transaminazione. La transaminazione è spesso accoppiata alla deaminazione ossidativa: la presenza del gruppo NH2 in a impedisce agli aminoacidi di subire la degradazione ossidativa, per cui l'eliminazione del gruppo amminico è fondamentale.
DEAMINAZIONE OSSIDATIVA
Consiste nell'eliminazione di un gruppo amminico, che viene liberato sotto forma di ammoniaca. Riguarda in genere il glutammato, che è convertito ad a-chetoglutarato, il quale può essere impiegato nella reazione di transaminazione o può essere immesso nel ciclo di Krebs a scopo energetico. È, infatti, una reazione dipendente dai livelli energetici dell'organismo: GDP e ADP sono attivatori allosterici, mentre GTP e ATP sono inibitori. 57
Altri fattori che controllano la direzione della reazione sono il glutammato, NH3 e il rapporto [NAD+]/[NADH]. La glutammato-deidrogenasi (enzima che catalizza la conversione di glutammato ad a-chetoglutarato) è abbastanza ubiquitario, tranne alcune isoforme che sono più espresse in fegato e reni. Abbiamo detto che spesso la deaminazione è associata alla transaminazione, tanto che si parla di transdeaminazione.
DEAMINAZIONE NON OSSIDATIVA
In questo caso non avviene una redox ma idrolisi, e riguarda solo serina, treonina e cisteina. Questi tre aminoacidi sono prima trasformati in immine (C=NH2+) per disidratazione, e poi viene aggiunta nuovamente una molecola d'acqua, per cui viene eliminata ammoniaca. Si ottengono dei derivati che possono entrare in gluconeogenesi.
DECARBOSSILAZIONE
Questa rezaione può portare alla formazione di neurotrasmettitori o altri composti fondamentali per l'organismo. Ad esempio, dal glutammato si ottiene il GABA, neurotrasmettitore inibitorio, mentre dalla serina si ottiene l'etanolammina, che ritroviamo nella struttura dei fosfolipidi di membrana.
Destino metabolico dell'ammoniaca
TRASPORTO DELL'AMMONIACA A LIVELLO EPATICO
La gestione dell'ammoniaca è problematica in quanto tossica, per cui deve essere eliminata. Per essere eliminata deve prima essere trasportata, e per farlo viene nuovamente convertita ad aminoacido, e nello specifico in aminoacidi che: sono facilmente trasportabili; possano "caricare" più moli di ammoniaca possibili. Si ha:
- Trasformazione dell'a-chetoglutarato in glutammato (glutammato deidrogenasi) > 1NH3
- Ammidazione del glutammato in glutammina (muscoli, fegato, intestino, cervello) > 2NH3
La glutammina può così entrare in circolo ed arrivare a livello epatico, dove sarà ulteriormente metabolizzata: sono qui presenti le glutamminasi, che convertono la glutammina a glutammato, che viene deaminato a -chetoglutarato. Le molecole di ammoniaca a livello epatico possono essere convertite ad urea.
Un altro aminoacido che può essere usato per eliminare l'ammoniaca è l'alanina. Nel muscolo troviamo alanina aminotransferasi in grandi quantità, per cui dal piruvato si ottiene l'alanina, la quale può entrare nel torrente ematico e arrivare a livello epatico. 58