Microbiologia: farmaci antivirali e resistenza virale
Documento di Microbiologia – Lezione 9. Il Pdf, un set di appunti universitari di Biologia, esamina i meccanismi d'azione dei farmaci contro HIV, HBV e HCV, le strategie virali di resistenza, la barriera genetica e l'interazione virus-cellula.
Mostra di più19 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Farmaci Antivirali
MICROBIOLOGIA - LEZIONE 9
Farmaci antivirali
Sbobinatore 1: Miriam Santoro
Sbobinatore 2: Claudio Mattei
Data: 17/03/2023
Professoressa: Donatella Ferraro
Sommario
- Barriera Genetica e Fitness virale.
- Pressione farmacologica incongrua
- Virus Influenzali.
- Amantadina e Rimantadina.
- Inibitori della Neuraminidasi
- Baloxavir Marboxil
- Inibitori della sintesi degli acidi nucleici virali
- Analoghi dei Nucleosidi e dei Nucleotidi
- Analoghi non nucleosidici
- Herpesvirus
- Virus dell'HIV
- Virus dell'Epatite B
- Virus dell'Epatite C.
- Differenze tra HIV, HBV e HCV
- Interazione virus-cellula
Nella lezione precedente è stato introdotto il concetto dei farmaci antivirali. Così come i batteri
riescono a modificarsi per sfuggire all'azione del farmaco, allo stesso modo fanno i virus.
La resistenza antivirale è determinata in parte dalla capacità del virus di mutare, e in parte dall'utilizzo
del farmaco stesso.
I tre virus che dal punto di vista farmacologico sono stati più studiati sono HBV, HCV e HIV. Questi
virus hanno un'altissima attività replicativa, le loro polimerasi, quali RNA polimerasi RNA-
dipendenti per l'HVC, la trascrittasi inversa per l'HIV e per l'HBV, mancano della capacità di proof-
reading.
Dunque, il virus si replica, ma manca la correzione degli errori che fisiologicamente le polimerasi
fanno, e conseguentemente queste mutazioni si accumulano, fino a raggiungere le 10^11 mutazioni
puntiformi al giorno.
Queste mutazioni sono distribuite lungo il genoma virale in modo casuale, non ci sono siti privilegiati,
ma possono insistere sulle porzioni geniche su cui agisce il farmaco.
Barriera Genetica e Fitness Virale
Un virus diventa resistente ad un farmaco perché accumula mutazioni e questo concetto viene
chiamato Barriera Genetica: vuol dire che per un virus può essere sufficiente selezionare una
mutazione laddove agisce il
farmaco per
diventare
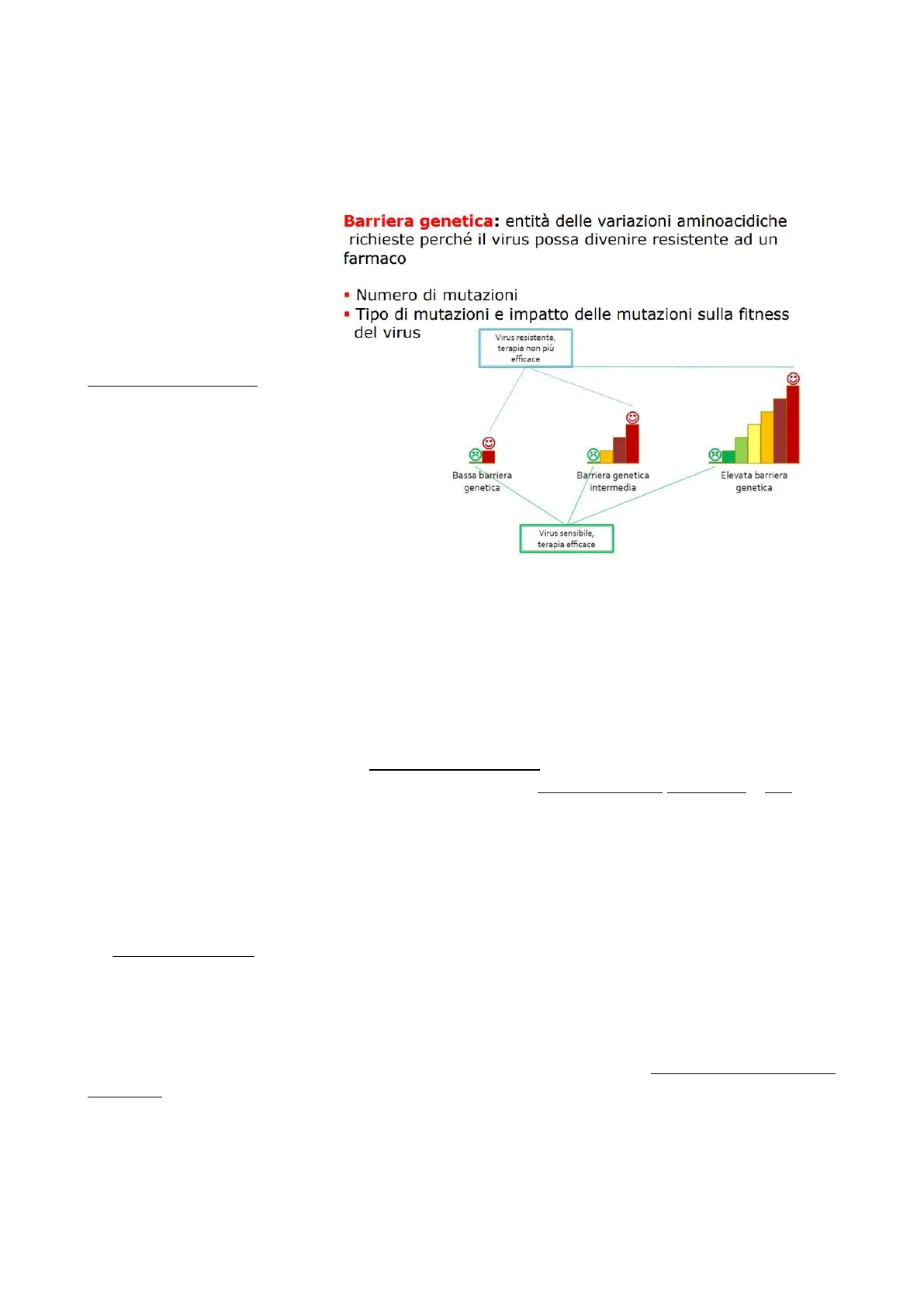
Barriera genetica: entità delle variazioni aminoacidiche
richieste perché il virus possa divenire resistente ad un
farmaco
resistente, rispetto ad un altro
virus a cui sarà necessario
selezionarne due o più di
• Numero di mutazioni
mutazioni.
La barriera genetica riguarda il
numero di mutazioni che il
singolo virus deve selezionare
rispetto al farmaco
in
questione, prendendo
in
considerazione il rapporto
virus-farmaco.
• Tipo di mutazioni e impatto delle mutazioni sulla fitness
del virus
Virus resistente,
terapia non più
efficace
Bassa barriera
genetica
Barriera genetica
intermedia
Elevata barriera
genetica
Un altro aspetto importante è il
Virus sensibile,
terapia efficace
tipo di mutazione, in quanto
una mutazione nucleotidica e una mutazione amminoacidica hanno un peso differente. Un altro
aspetto è come queste mutazioni incidano sulla fitness virale, ovvero la capacità e la forza replicativa
del virus.
Affinché si formi una mutazione, il farmaco crea sul virus una pressione selettiva e il virus seleziona
le mutazioni che ha già a monte. Il farmaco fa emergere una fisiologica mutazione che il virus aveva
acquisito a causa della mancata attività di proof-reading della sua polimerasi.
La barriera genetica corrisponde al numero di mutazioni che il virus deve selezionare per diventare
resistente. I farmaci posso avere una barriera genetica bassa, per cui è sufficiente una mutazione al
punto giusto per far diventare il virus resistente; oppure una barriera genetica intermedia o alta.
Le mutazioni avvantaggiano il virus rispetto al farmaco, però vanno ad influire sulla fitness virale: il
virus resiste al farmaco ma la sua capacità replicativa è stata alterata e ridotta.
È stato dimostrato che per recuperare la piena capacità replicativa, il virus tende a selezionare
mutazioni secondarie, che non hanno un peso sulla farmaco resistenza, ma servono al virus per
recuperare il fitness replicativo.
Le mutazioni primarie sono, invece, quelle strettamente correlate alla farmaco resistenza.
Pressione Farmacologica Incongrua
A causa di caratteristiche intrinseche del farmaco, o laddove il farmaco viene utilizzato in maniera
non corretta, utilizzato ad una concentrazione non ottimale, si crea una pressione farmacologica
incongrua.
Ogni farmaco è caratterizzato da una propria potenza, dove per potenza si intende la forza con la
quale un farmaco riesce a sopprimere la replicazione virale.
2Per quanto riguarda la concentrazione non ottimale, un esempio è il TENOFOVIR, utilizzato per
l'HIV e per l'epatite B. Questo farmaco ha una tossicità renale, per cui è stata creata una formulazione
a concentrazione dimezzata, di conseguenza però la sua pressione farmacologica si riduce.
Un altro aspetto che va ad inficiare sulla pressione farmacologica è la mancata somministrazione
del farmaco, ad esempio per una dimenticanza del paziente soprattutto in una terapia a lungo temine.
Nell'immagine è rappresentata la variazione della concentrazione ematica del farmaco durante la
terapia. In rosso è indicato il
virus resistente al farmaco, in
verde il virus sensibile.
Il paziente assume il farmaco,
la sua concentrazione ematica
arriva al picco e con il tempo
si va riducendo.
La linea tratteggiata indica la
concentrazione del farmaco al
di sotto della quale non si deve
scendere. Se il farmaco si
mantiene al di sopra della
concentrazione minima
è
capace di sopprimere la
replicazione virale.
Drug concentration
in blood
Changes of drug concentration
in blood during medication
Failed to take
medication
Time
Regular medication
HIV
Lower limit of effective
drug concentration in blood
Resistant HIV
Nel momento in cui il farmaco
non è più disponibile e la sua concentrazione scende sotto il valore minimo, le particelle virali iniziano
a replicarsi, in particolare quelle in rosso saranno avvantaggiate perché resistenti e perché quelle
sensibili (in verde) erano state precedentemente inibite dal farmaco.
Questo è quello che succede se c'è una pressione farmacologica non adeguata.
Le terapie hanno come obiettivo
sopprimere la replicazione virale in modo
da chiudere quello che viene definito
spazio replicativo.
Se il farmaco è potente e ben utilizzato, il
virus è talmente soppresso nella sua attività
replicativa che può mutare poco o nulla.
Se il farmaco è utilizzato a concentrazione
subottimale, lo spazio replicativo rimane
aperto, le particelle virali sensibili sono
inibite ma
le particelle resistenti
aumentano, determinando un fallimento
terapeutico.
Selezione di virus resistente sotto la
pressione farmacologica
Initiation of
suboptimal
drug therapy
O
Resistance to AZT
develops quickly
wild type virus
mutant virus
AZT
3TC
Initiation of
HAART
IDV
Functionally disabled virus
wild type virus
mutant virus
Resistance to
whole regimen
develops slowly
Questo è il motivo per cui si preferisce usare dei farmaci molto potenti e delle terapie di
combinazione, con più farmaci differenti che riescono a sopprimere il virus anche se resistente.
3Utilizzando una terapia multifarmaco vi è una minore probabilità che il virus riesca a resistere a tutti
i farmaci contemporaneamente. Questo è alla base della terapia per l'HIV chiamata terapia HAART.
A seguire sono trattati i principali farmaci disponibili per uso clinico, i quali agiscono sulle diverse
tappe del ciclo replicativo del virus. La maggior parte dei farmaci agiscono su questi virus, Virus
Influenzali, Herpesvirus, HIV, HBV e HCV, i quali sono una minoranza rispetto a quelli che circolano
nella popolazione umana.
Virus Influenzali
Il virus dell'influenza presenta come
antirecettore virale l'Emoagglutinina e
un'altra proteina chiamata Neuraminidasi.
L'antirecettore virale si lega al recettore
cellulare e questo virus, nonostante sia
inviluppato, non ha una proteina fusogena
immediatamente disponibile e quindi entra
per endocitosi.
Questo virus ha tra le proteine dell'envelope
la proteina canale M2, che si apre e chiude
a seconda delle condizioni di pH.
Virus dell'influenza
Complesso di trascrizione
& PB2
O PB
- PA
Emagglutinina
Neuraminidasi
M.
Proteina di matrice
M
Canale ionico
Scapsidazione
Nucleocapside
Gemmazione
Neuraminidase enables
the virus to bud from the
host cell
Newly
formed virus
Host cell
Influenza viruses infect host cells
turning them into "flu factories"
Hemagglutinin
Neuraminidase inhibition
Neuraminidase
La vescicola endocitica ha un pH acido, la proteina M2 si apre ed entrano gli ioni H+, si rompono i
ponti disolfuro, si attivano le proteasi e si crea una rottura dell'emoagglutinina, la parte superiore si
toglie facendo emergere la parte sottostante chiamata HA2. In questo modo il virus entra nella cellula.
Quando il virus deve uscire dalla cellula entra in gioco la seconda proteina dell'envelope chiamata
Neuraminidasi (sialidasi, enzima appartenente alla classe delle idrolasi) che rompe i legami con
l'acido sialico dell'emoagglutinina con il suo recettore.
Sulla membrana cellulare è presente acido sialico a cui si lega emoagglutinina, impedendo l'uscita
del virus. La neuraminidasi rompe questo legame permettendo l'uscita del virus dalla cellula.
Amantadina e Rimantadina
Esistono due categorie di molecole ammine tricicliche, Amantadina e Rimantadina, che hanno
un'affinità per la proteina canale M2. Si
Inibitori del denudamento del Virus Influenzale
legano ad essa e creano un ingombro sterico,
gli ioni H+ non riescono ad entrare e il virus
AMANTADINA e RIMANTADINA
non può penetrare all'interno della cellula.
Queste due molecole hanno effetti collaterali
di tipo neurologico e sono poco utilizzate.
Vengono principalmente utilizzati per la
profilassi dell'infezione nei pazienti
Proteina M2
Lipid
High pH form
(neutral)
Closed
Bilayer
M
Low pH form
(doubly ionized)
Open
R
4immunocompromessi, i quali non sono stati vaccinati e hanno un maggior rischio di infettarsi e di
non saper controllare l'infezione.
(Esistono tre tipi di virus influenzali: tipo A, tipo B e tipo C. I primi due sono i più attenzionati, in
quanto il tipo C circola molto poco.)
Le due molecole funzionano esclusivamente sul virus influenzale di tipo A, perché nel virus di tipo
B è presente una proteina canale differente per la quale Amantadina e Rimantadina non hanno affinità.
Inoltre, questi due farmaci devono essere somministrati entro 24 - 48 ore dall'insorgenza della
sintomatologia per poter bloccare la replicazione virale. Questo virus dà una sintomatologia come
risultato della replicazione e ha un periodo di incubazione breve, dopo di cui il virus tende ad
andarsene perché si induce un processo infiammatorio.
Da uno studio del 2005 è emerso che sebbene questi farmaci siano poco utilizzati, il virus ha
accumulato una serie di mutazioni di resistenza con una bassa barriera genetica, una mutazione che
corrisponde ad una resistenza. Nonostante ciò, il virus continua ad essere sensibile ad un'altra
categoria di farmaci, gli inibitori della Neuraminidasi.
Inibitori della Neuraminidasi
Questi farmaci funzionano sui virus influenzali sia di tipo A che di tipo B, che sono i più diffusi.
Queste molecole, Zanamivir e Oseltamivir, sono degli analoghi strutturali dell'acido sialico in quanto
la neuraminidasi agisce sull'acido sialico. In presenza di questi farmaci il virus non si lega all'acido
sialico della cellula bensì a
queste molecole, bloccando
l'azione della neuraminidasi.
Zanamivir e Oseltamivir sono
diversi tra di loro ma agiscono
entrambi sulla neuraminidasi,
ciò vuol dire che si possono
usare in combinazione
se
necessario.
Per quanto
riguarda
la
resistenza,
il
virus
ha
selezionato
un
serie
di
mutazioni ma allo stesso tempo
ha perso di fitness.
Analoghi strutturali di acido sialico
Virus influenzale A e B
Neuraminidase inhibition
SIALIC ACID
ZANAMIVIR
OSELTAMIVIR
Hydrophobic
Carboxylate
Carboxylate
Carboxylate group
Glycerol
Glycerol
Guanidine
Hydroxyl
Hydrophobic
pocket
Active site of
neuraminidase
Arg 371
Arg 118
Mutanti resistenti:
Arg 292
•ridotta fitness
Glu 119/
Głu 276
Asp 151
Ala 246
Arg 152
Arg 224
Trp 178
•ridotta infettività per gli animali
Anche in questo caso, questi
Tic 222
farmaci devono essere somministrati rapidamente rispetto all'inizio della sintomatologia.
La loro funzione è quella di ridurre la durata dei sintomi di 1 - 2 giorni. Sul singolo paziente potrebbe
sembrare un effetto di poco conto, ma guardando in maniera collettiva ha un peso rilevante.
Inoltre, ci sono pazienti fragili in cui queste infezioni possono causare delle complicanze fino alla
morte (circa 1000 ogni anno in Italia), e in questi casi è importante ridurre le complicanze ed eliminare
velocemente il virus.
Lo Zanamivir è il più utilizzato, può causare broncospasmo, ma se necessario si somministra.
5
Host cell