Soluzioni chimiche: definizione, classificazione e calcolo della concentrazione
Slide dall'Università sulle Soluzioni. Il Pdf illustra le soluzioni chimiche, distinguendo soluto e solvente, e le classifica in gassose, liquide e solide. Vengono presentate le formule per calcolare la concentrazione, come molarità e normalità, in questa presentazione di Chimica.
Mostra di più20 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
SOLUZIONI
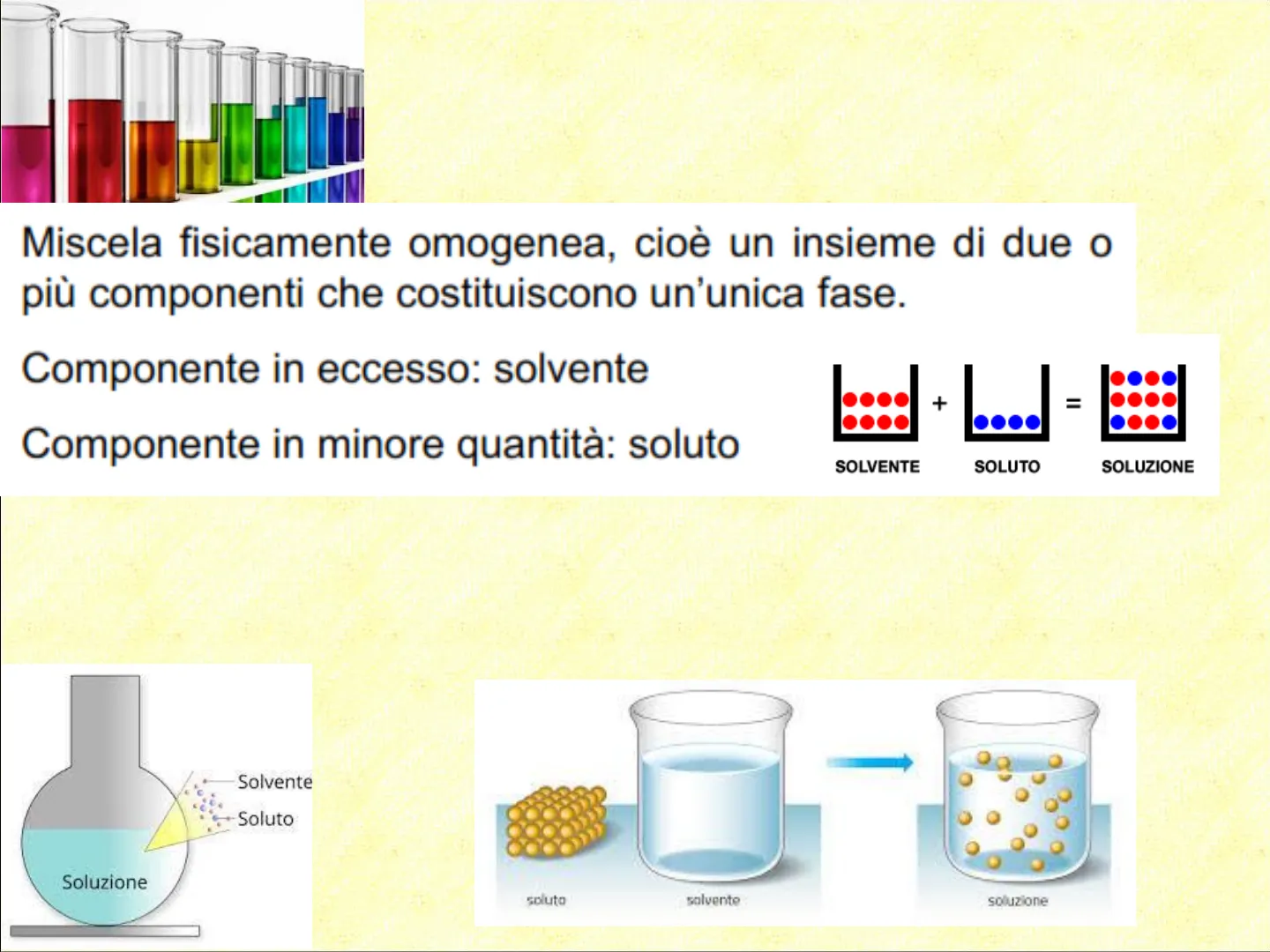
Miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un'unica fase. Componente in eccesso: solvente Componente in minore quantità: soluto
+ = SOLVENTE SOLUTO SOLUZIONE
Solvente Soluto Soluzione
soluto solvente soluzione
SOLUZIONI
Una soluzione è una miscela omogenea di più composti chimici
SOLUZIONI GASSOSE
le miscele gassose sono sempre omogenee e quindi formano sempre una soluzione
SOLUZIONI LIQUIDE
si possono formare sciogliendo in un liquido, chiamato solvente, gas, solidi o altri liquidi.
SOLUZIONI SOLIDE
sono abbastanza comuni: per esempio le leghe metalliche sono una miscela omogenea solida di più metalli.Soluzioni gassose, liquide e solide
Tipi di Soluzione
| Soluzione | Descrizione | Tipo di soluzione |
| Aria | Og e altri gas in N2 | Gassosa |
| Acqua di mare | NaCl e altri sali solidi in acqua | Liquida |
| Soluzione alcolica | Alcol liquido in acqua | Liquida |
| Acqua di seltz | CO2 gassosa in acqua | Liquida |
| Amalgama odontoiatrico | Hg liquido in Ag solido | Solida |
| Ottone | Zn solido in Cu solido | Solida |
| Catalizzatori | H2 gassoso in Pd solido | Solida |
Solventi e Soluti Polari e Non Polari
Dobbiamo distinguere tra solventi e soluti polari e non polari. Se le loro molecole presentano una polarizzazione elettrica si definiscono POLARI, altrimenti APOLARI.
8+ 8- H CI
+ - K CI
8+ 8- H H B H H 8+ 104,45° H S+ 8 95,84 pm
CI C CI CI CI
Geometria Molecolare e Polarità
IMPORTANTE !!
1 + o C O > + S × p =5,3 - 10-30 Cm == 0
1 |F| I 1 B N H μ= 0 X F/ X + H 1 ĮCII 1 + × C > 1 + p = 6,2. 10-30 Cm == 0 CI CI/ + 1 7 H H 1 H p =4,9 - 10-30 Cm E 1 ISolventi polari Solventi apolari
SIMILE SCIOGLIE IL SIMILE
Soluzioni elettrolitiche Solvatazione/idratazione
+ loni idratati
SIMILE SCIOGLIE SIMILE
Solventi polari sciolgono soluti polari mentre solventi apolari sciolgono soluti apolari. Le interazioni soluto-soluto devono essere simili alle interazioni soluto-solvente. Se nel soluto ci sono interazioni a legame ad idrogeno (NH3 ed alcol etilico) e nel solvente pure si ha possibilità di dissoluzione.
Soluzione acqua + ammoniaca
Solvente Water (H2O) 8- 8+ H O : Hydrogen bond 6+ H 8+ ..... o 6+. .. 6- H 8+ a+ 6+ H 8+ 8+ H 8+ Ammonia (NH3)
Soluzione acqua + alcol etilico
Ethanol - Water Hydrogen Bonding water hydrogen bond ethanol C. Ophardt, o. 2003
Legami a idrogeno H Hydrogen bond 8- NI soluti ionici in acqua si comportano in modo particolare: i legami tra gli ioni si rompono a causa dell'attrazione delle molecole d'acqua. Quando mettiamo il sale (NaCl) in acqua, le molecole di acqua circondano gli ioni Na+ e gli ioni CI -. Il polo positivo delle molecole d'acqua si orienta verso gli ioni CI-, mentre quello negativo si orienta gli ioni Na+. In questo modo i legami si rompono e il sale si scioglie nell'acqua.
lone cloruro (CI-) Cloruro di sodio (NaCl) lone sodio (Na+)
- + + Molecola d'acqua (H2O)
+ + 8+ Solvente + Soluto Soluzione
Solubilità
Solubilità: quantità massima di sostanza che, a una certa T, si scioglie in una certa quantità di solvente dando origine ad un sistema stabile (concentrazione di una soluzione satura)
Soluzione Supernatante Sospensione Precipitato
Concentrazione
Diluito Concentrato
CONCENTRAZIONE
soluto/soluzione
- a/a + b a a + b ma % peso · 100 Ma + mb
no Frazione molare na + np
Molarità M (mol/l) na ma 1 V PM. V
Normalità N (eq/l) nea Ze na Ze ma 1 = V V PMa V
V. 100 Va + Vb
Osmolarità (osmol/l) na ia ma la 1 = V PM. V = a = ze
% volume
Calcolare la Concentrazione Molare
- M = n/V
- Lavorare con una soluzione a molarità nota permette di misurare un numero di moli desiderate semplicemente misurando un volume di soluzione.
- Per trovare il volume di soluzione che contiene un certo numero di moli, basta scrivere:
- volume della soluzione = moli di soluto / molarità
- V = n/M
- Per trovare il numero di moli contenute in un certo volume, invece:
- moli di soluto = molarità · volume della soluzione
- n = M·V
Esercizio 1: Calcolo Grammi Zucchero e ml Acqua
1. Calcolare i gr di zucchero e i ml di acqua necessari a preparare 480,0 g di una soluzione al 3,5 % m/m di zucchero in acqua. [16,8 g, 463,2 mL]
Esercizio 3: Calcolo c% v/v
3. A 125,0 ml di etanolo si aggiunge acqua fino a 450,0 mL. Calcolare la c% v/v della soluzione ottenuta. [27,8%]
Esercizio 6: Gradazione Alcolica
6. A 40 ml di una grappa con un 45 % di alcool, un barman aggiunge acqua fino a 60 mL. Quale sarà la nuova gradazione alcolica ? [30 %]
Esercizio 1: Concentrazione Percentuale Massa/Massa
Calcola la concentrazione percentuale massa/massa (% m/m) di una soluzione ottenuta sciogliendo 15,00 g di K2SO4 (soluto) in 180,00 g di acqua (solvente).
Esercizio 2: Quantità di NaHCO3
Calcola la quantità di NaHCO3 contenuto in 600,00 g di una soluzione al 25 % m/m.
Esercizio 3: Concentrazione Percentuale m/m
Una soluzione si ottiene sciogliendo 2,50 moli di HNO3 (MM = 63,02) in 600,00 g di acqua. Calcola la concentrazione percentuale % m/m.
Esercizio 4: Concentrazione Percentuale m/V
Calcola la concentrazione percentuale in volume (% m/V) ottenuta sciogliendo 20,00 g di NaCl in 170 mL di soluzione.
FORMULARIO ESSENZIALE
m ="St. 100 m rappresenta la massa di soluto (in grammi) sciolta in 100g di soluzione
%m / V = = 'St . St . 100 SZ V V rappresenta la massa di soluto (in grammi) sciolta in 100ml di soluzione
%V /V = = St . 100 SZ rappresenta il volume di soluto (in mL) sciolto in 100ml di soluzione
MOLARITA' -> CM = n rappresenta il numero di moli di soluto sciolto in 1L di soluzione V SZ m V