Aspetti avanzati di Spettrometria di Massa: ESI, MALDI e analizzatori TOF
Documento di Università sulla Spettrometria di Massa, Aspetti Avanzati. Il Pdf, adatto per lo studio universitario di Chimica, esplora le tecniche di ionizzazione ESI e MALDI, gli analizzatori TOF e le formule correlate, con diagrammi e spettri di massa.
Mostra di più21 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Proteomica #Nº8
Aspetti avanzati di Spettrometria di Massa
Prof. Fulvio Magni- Data Lezione (04/03/2020) - Autore sbobina: Claudia Rivoletti - Revisore: Elisabetta Maia Lo spettrometro di massa deve avere alcuni aspetti per poter ottenere informazioni su macromolecole come le proteine. Per esempio, se aumenta la dimensione deve aumentare la risoluzione. Inoltre, lo spettrometro lavora sottovuoto, per non avere molecole residue di aria che possano ridurre la quantità di ioni che arrivano al rivelatore. Collegando l'HPLC, la quantità in ml/min di diluente che esce dall'HPLC ed entra nello spettrometro avrebbe un volume talmente grande che le pompe non ce la farebbero. Per poter analizzare macromolecole come le proteine è necessario utilizzare delle possibilità di ionizzazione e di analizzatore molto più performanti rispetto a tecnologie più vecchie. Nel 1982 le caratteristiche di HPLC (separazione in soluzione) e spettrometro (separazione sottovuoto) rendeva impossibile interfacciare l'HPLC con lo spettrometro (era possibile però interfacciare il gas cromatografo). Nel 1989 sembrava possibile interfacciare questi due strumenti anche se lo spettrometro è come una grossa aquila che mangia il "pesciolino" (HPLC) oppure al contrario "lo squalo" mangia l'aquila (i due ruoli sembrano non combinabili). Nel 1992 sembrava possibile combinare le due tecniche (nell'articolo si dice "ho visto l'elefante volare"). Sono, infatti, state realizzate tecniche che rendono possibile l'analisi di macromolecole e che permettono di interfacciare I'HPLC allo spettrometro di massa. Queste tecniche hanno valso il premio Nobel per la chimica a Tanaka e Fenn.
Le principali tecniche di ionizzazione sono ESI, APCI e MALDI. Le prime due rendono possibile la connessione diretta tra HPLC e spettrometro di massa, mentre la tecnica MALDI rende possibile l'analisi delle macromolecole. Nel tempo poi sono stati sviluppati anche nuovi tipi di analizzatori, di cui i più utilizzati nello studio del proteoma e del metaboloma sono TOF, quadrupoli a trappola ionica (3D e 2D), FT-ICR e Orbitrap (in assoluto i più utilizzati).
Ionizzazione electrospray (ESI)
Caratteristiche della tecnica ESI
- forma ioni multicarica [M+nH]"+, ovvero in questo caso Z corrisponde ad un numero maggiore di 1;
- permette di ottenere informazioni su molecole ad elevata massa molecolare, purché abbiano siti basici cui attaccare H+;
- ha un'elevata LOD, ovvero elevata efficienza di ionizzazione, e di conseguenza un'elevata sensibilità (perché tutto quello che introduco viene ionizzato);
- è compatibile con l'HPLC (flussi da 1mL a pochi nL);
- l'intensità del segnale dipende dalla concentrazione (es. se le 100 molecole sono in 100microL rispetto a 1 mL aumento l'intensità);
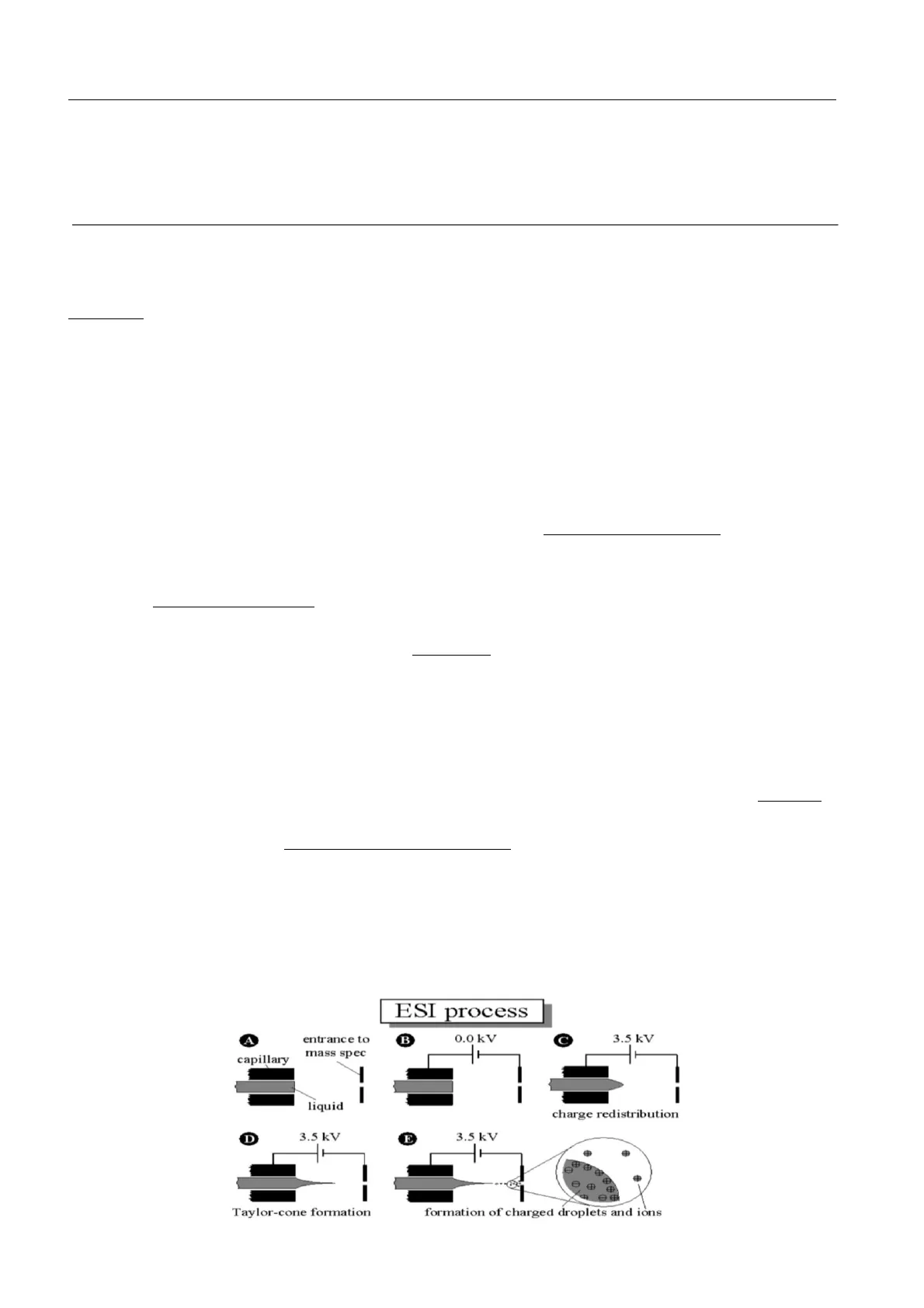
All'uscita della colonna cromatografica viene collegato un capillare, che viene poi posto davanti allo spettrometro (figura sotto, A).
ESI process entrance to mass spec B 0.0 kV c 3.5 kV capillary liquid charge redistribution D 3.5 kV E 3.5 kV Taylor-cone formation formation of charged droplets and ionsCiò permette di introdurre ciò che esce dal capillare (e che arriva dall'HPLC) nello spettrometro di massa. Viene, quindi, applicata una differenza di potenziale tra l'estremità del capillare che porta la fase mobile dall'HPLC e lo spettrometro (B, C). Applicando tale differenza di potenziale (Volt) e incrementandone il valore, il flusso di fase mobile che fuoriesce dal capillare e cade, assume una forma a cono (si assottiglia).
Il cono, detto cono di Taylor (D), tende ad assottigliarsi fino a raggiungere un punto dove si forma una nuvola di goccioline di acqua. Fino alla punta del cono di Taylor, quindi, si ha un flusso di fase mobile, mentre dopo la punta il flusso di acqua si rompe generando goccioline (E).
Le goccioline che si formano si spostano dalla zona in cui si sono formate verso lo spettrometro e mentre ciò avviene il solvente se ne va. All'interno dello spettrometro entrano, quindi, solo gli analiti che hanno trattenuto sulla superficie più di una carica. Lo spettrometro ha una pressione intorno a 10-6, mentre a livello del capillare c'è pressione atmosferica. Dunque, lo spettrometro tenderebbe ad aspirare tutto ciò che arriva dall'HPLC. In questa zona viene però collegata una pompa rotativa che aspira, in modo da creare un gradiente di vuoto (10-2/10-3, uscita dalla colonna 760 Torr, 0,2/0,3), permettendo allo spettrometro di massa di mantenere inalterato il suo stato di vuoto.
Considerazioni fisiche sul flusso laminare
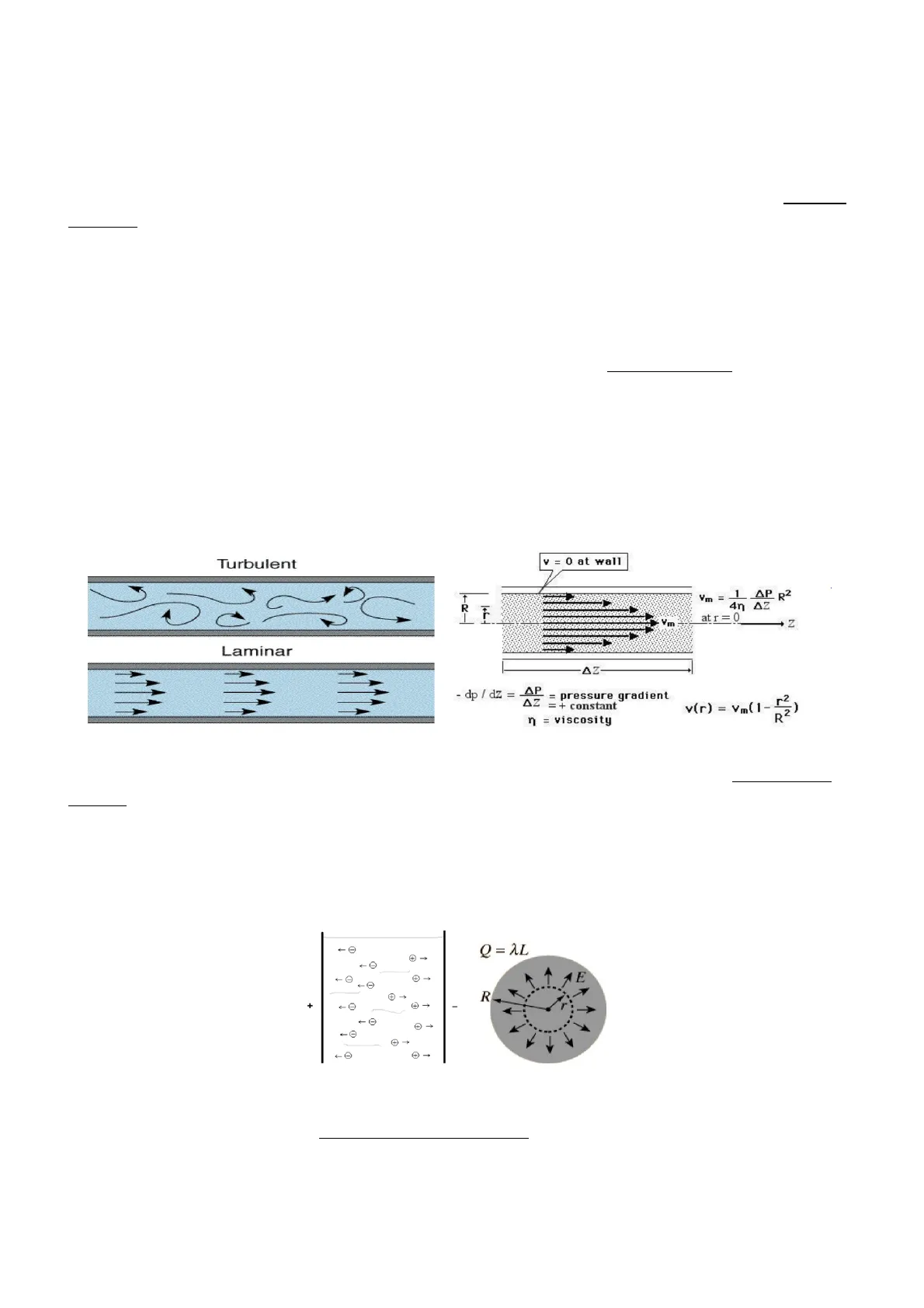
Considerazioni fisiche. All'interno del capillare che collega la colonna e porta la fase mobile davanti allo spettrometro è presente un flusso laminare (le molecole sono come dei fogli che si muovono). La parete del tubo, però, fa attrito, quindi la velocità delle molecole di fase mobile a contatto con la superficie interna è rallentata, mentre le molecole centrali si muovono leggermente più veloci.
Turbulent v = 0 at wall 1 R Vm = 1 AP 2 4η ΔΖ F at r = 0 Ym N Laminar AZ - dp / dz = AP - = pressure gradient AZ = + constant n = viscosity v(r) = Vm(1-12 D2) Ma dato che è stata applicata una differenza di potenziale, le pareti del capillare hanno una carica positiva o negativa. Gli ioni in soluzione incominciano, quindi, ad orientare il loro movimento verso l'elettrodo con carica opposta (prima si muovevano casualmente).
Dunque, da una parte si ha un movimento di molecole lungo l'asse del capillare (assiale), dall'altra si ha un movimento radiale (dovuto al campo elettrico) dal centro del capillare verso l'esterno o verso l'interno. Infatti, gli anioni e i cationi si muovono radialmente. In particolare, se si hanno ioni positivi, il polo negativo della differenza di potenziale applicata si trova a livello dello spettrometro, mentre il polo positivo si trova a livello del capillare.
+ e - e 1 R + 1 - 1 Q= AL + 1E Nel caso di ESI in cui si vogliono registrare ioni positivi, avendo applicato una carica positiva a livello del capillare, gli ioni con carica negativa si trovano verso la parete del capillare (in direzionale radiale), mentre quelli con carica positiva sono centrali. C'è quindi un aumento della concentrazione degli ioni di interesse al centro e le goccioline che si formano risultano molto ricche di ioni positivi. Gli elettroni si scaricano sulle pareti lasciando all'interno ioni positivi che escono come goccioline. Nella punta del cono ci sono essenzialmente ioni positivi.
Perché le goccioline non sono neutre? Perché questa differenza di potenziale causa una separazione di cariche.Inlet to mass spectrometer Metal capillary Taylor cone Fine spray O C Liquid O O ® Fine filament of liquid Relatively Smaller large droplet droplet Unstable droplet Gas-phase ion + High-voltage power supply 0 V -4 500 V Per registrare, invece, ioni negativi è necessario girare la polarità della differenza di potenziale, per poter concentrare ioni negativi (carica + spettrometro, carica - CRM IEM CEM ± capillare).
Gradiente di vuoto e modelli di evaporazione
+ + + + + Lungo il percorso della gocciolina si ha un gradiente di vuoto che aumenta (Patm = 10-7). Ciò permette alle particelle più volatili, ovvero alle particelle del solvente, di evaporare. La gocciolina, quindi, si rimpicciolisce fino a quando rimane solo l'analita carico. Ci sono diverse ipotesi riguardo a come ciò avvenga.
-
+ + + + + La gocciolina è ricoperta di cariche positive e mentre si muove il + + solvente evapora. Ciò porta alla diminuzione delle dimensioni L della gocciolina. La prima ipotesi (CRM, charge residual model) + + + + + prevede che al diminuire della dimensione aumenti la densità di + + + × × cariche positive, fino a quando tale densità diventa tanto elevata + + × da rompere la gocciolina. La seconda ipotesi (IEM, ion x × evaporation model) ritiene che l'aumento della densità di carica x sulla superficie (perché sta evaporando il solvente) porta all'espulsione dell'analita a causa del fatto che le cariche positive si respingono. La gocciolina si divide in due e così via fino a quando all'entrata dello spettrometro arriva solo l'analita senza solvente.
-
Per le grosse molecole, come le proteine che hanno molte cariche, un'altra ipotesi (CEM, chain ejection model) dice che la proteina, man mano che acquista cariche positive, viene espulsa dalla gocciolina una parte alla volta.
Analisi dello spettro di massa della proteina umana TNF
Nel seguente spettro di massa della proteina umana TNF (tumor necrosis factor) ci sono 7 segnali, che indicherebbero la presenza di 7 molecole diverse, anche se ne è stata inserita una sola. Ciò avviene a causa del fatto che durante il processo ESI può essere introdotto sull'analita più di un protone, cosa che l'analizzatore non può sapere, perché vede solo il rapporto
Human-TNF Mw=17352 massa/carica. Infatti, a parità di massa molecolare Mw nH+ m/z (17352) può essere trattenuto un diverso numero 17352 14 1240,4 di protoni (c'è una distribuzione di molecole 17352 15 1157,8 1021,7 multicarica), di conseguenza il rapporto 17352 16+ 16 17 15+ 17352 1085.3 1157.4 1085,5 massa/carica cambia (per esempio aumenta sia la 100 massa che la carica). La carica delle molecole è 17352 17+ 18 965,0 data dal protone che resta attaccato al sito basico. Avendo uno spettro di massa e conoscendo la carica relativa ai diversi picchi è possibile ricavare la massa molecolare della proteina di interesse 1021.4 1240.1 1335.4 965.1 1446.7 780.7 1578.0 1735.8 800 1000 1200 1400 1600 1800 + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + e e + +(m/z · z - z). Se, però non si conosce la carica relativa ai diversi picchi bisogna considerare due picchi ovvero una coppia di segnali m1 e m2, come indicato nella seguente figura:
m1 m2 m1= M + m1 n1 m2= M + m2 n2 con: m2>m1 e n1>n2 M = massa molecolare, n = numero di protoni del picco; Assumendo che gli ioni siano addotti tra la molecola neutra e protoni, si ha anche la relazione: n1 = n2 + 1 È quindi possibile fare un sistema di tre equazioni (in rosso) in tre incognite in modo da calcolare n2:
m1- 1 n2 = m2 - m1 Da qui si può risalire al valore di massa molecolare: M = n2 (m2 - 1) (m1 e m2 sono due ioni) Per esempio: Human TNF MW=17352 m2 = = 1157,4 m1 = 1085,5 Con: m1- 1 n2 = m2 - m1 M= n2 (m2-1) n2 (1157,4 - 1085,3) (1085,3 - 1) 1084,3 72,1 = 15 M = 15 x (1157,4 - 1) = 17346 Si calcola il valore di massa molecolare per ogni coppia di picchi consecutivi. In questo modo lo spettro ESI permette di risalire al valore di massa molecolare. Ci sono dei piccoli errori come fluttuazioni. Si possono, inoltre, ottenere informazioni su una molecola il cui valore di massa molecolare è al di fuori dell'intervallo di masse (es confronti MW con m/z).
Un analizzatore con un intervallo di massa fino a 2000 permette di ottenere informazioni anche su molecole più grosse se la tecnica di ionizzazione è la tecnica ESI.
I calcoli appena visti vengono fatti automaticamente da un algoritmo in tutti i programmi relativi a spettrometri di massa con interfaccia ESI. Inoltre, l'algoritmo fa una deconvoluzione dell'immagine, ovvero una ricostruzione dell'immagine dello spettro grezzo che permette di vedere un unico picco corrispondente all'aggiunta di un solo protone.