Normativa dei medicinali e preparazioni galeniche per uso orale
Documento dall'Università sulla normativa dei medicinali e le preparazioni galeniche. Il Pdf esplora soluzioni e sciroppi per somministrazione orale, analizzando fattori che influenzano la velocità di dissoluzione e fornendo esempi pratici con calcoli dettagliati, utile per studenti di Chimica.
Mostra di più23 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
PREPARAZIONI LIQUIDE PER USO ORALE: SOLUZIONI E SCIROPPI
In ambito galenico, quasi tutte le formulazioni di soluzioni acquose, anche se ci capiterà di fare formulazioni liquide che non sono per uso orale, di solito lo sono.
Lo sciroppo è chiaramente un prodotto liquido zuccherino, o quantomeno dolcificato, che ha un'applicazione per uso orale, altrimenti non si giustificherebbe il suo utilizzo.
Le soluzioni sono dispersioni omogenee a livello molecolare, cioè tutte le molecole, sia del principio attivo che degli eccipienti. Se il PA è formulato in forma solida e deve passare a una liquida, si parla di dissoluzione.
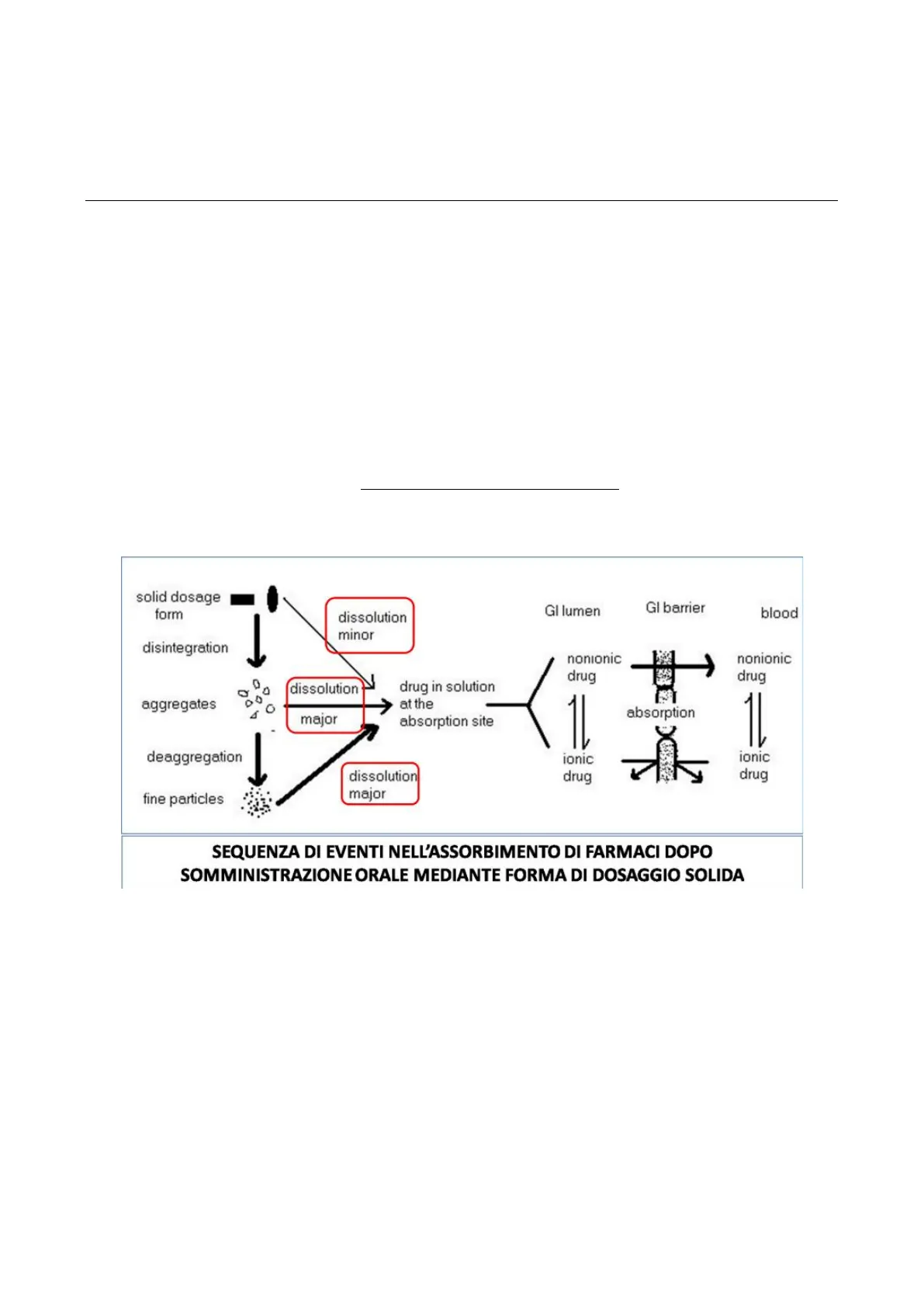
solid dosage form Gl lumen Gl barrier blood dissolution minor disintegration nonionic drug nonionic drug 00 dissolution aggregates major drug in solution at the absorption site 1 absorption deaggregation ionic drug 1L ionic drug fine particles dissolution major
SEQUENZA DI EVENTI NELL'ASSORBIMENTO DI FARMACI DOPO SOMMINISTRAZIONE ORALE MEDIANTE FORMA DI DOSAGGIO SOLIDA
Se si parte da una soluzione, ovviamente si saltano tutti quei passaggi di dissoluzione, avendo così un assorbimento immediato all'assunzione. Spesso la dissoluzione la fa il paziente stesso, es. quando scioglie la bustina in acqua.
Lo schema sopra (detto di Wagner), elenca tutte le fasi e i passaggi di dissoluzione di solido a partire da un tablet come forma di dosaggio. Avviene una disintegrazione quando la compressa viene a contatto con i fluidi biologici; si liberano perciò aggregati e via particelle sempre più piccole, aumentando la superficie specifica aumenta anche quella di contatto e allo stesso tempo anche la velocità di dissoluzione.
Questa fase influenza la velocità di passaggio della sostanza dalla fase solida a quella liquida a livello molecolare e quindi la velocità di assorbimento. La fase di disgregazione è influenzata sia dalle caratteristiche della forma di dosaggio che dalle caratteristiche del tratto GI. Quindi, la somministrazione orale può partire da forme di dosaggio solido, oppure si producono soluzioni, saltando la dissoluzione. Non sempre è facile produrre soluzioni permotivi di stabilità, sicuramente lo è in galenica perché si producono prodotti da consumare in breve tempo, perché vi sono minori problemi di sterilità e trasporto. Entro sei mesi, una soluzione galenica deve essere necessariamente consumata. I fattori che influenzano la velocità di dissoluzione sono stati descritti da Noyes e Whitney nella loro equazione, cioè un'applicazione della legge di Fick, che matematicizza il processo di diffusione di particelle.
J (flusso), cioè la quantità di massa che passa in funzione del tempo, è uguale a S, la superficie esposta dal solido, per Cs, cioè la concentrazione di solubilità, cioè la solubilità ad una specifica temperatura, nella frazione di liquido a contatto col solido, si satura la concentrazione di PA e da lì parte il gradiente di diffusione (il tutto in condizioni sink e in maniera ideale).
Parametri per aumentare la velocità di dissoluzione
Per aumentare la velocità di dissoluzione possiamo agire su tre parametri:
- agitazione, perché agitando aumenti il contatto e rinnovi rapidamente la Cs che è attorno al solido e faciliti la dissoluzione;
- la temperatura doppiamente dalla temperatura a livello del coefficiente di diffusione D; l'agitazione influenza anche il parametro h, perché riduce lo spessore di diffusione.
- granulometria, aumenta la superficie di contatto tra solvente e soluto aumenta la velocità di dissoluzione.
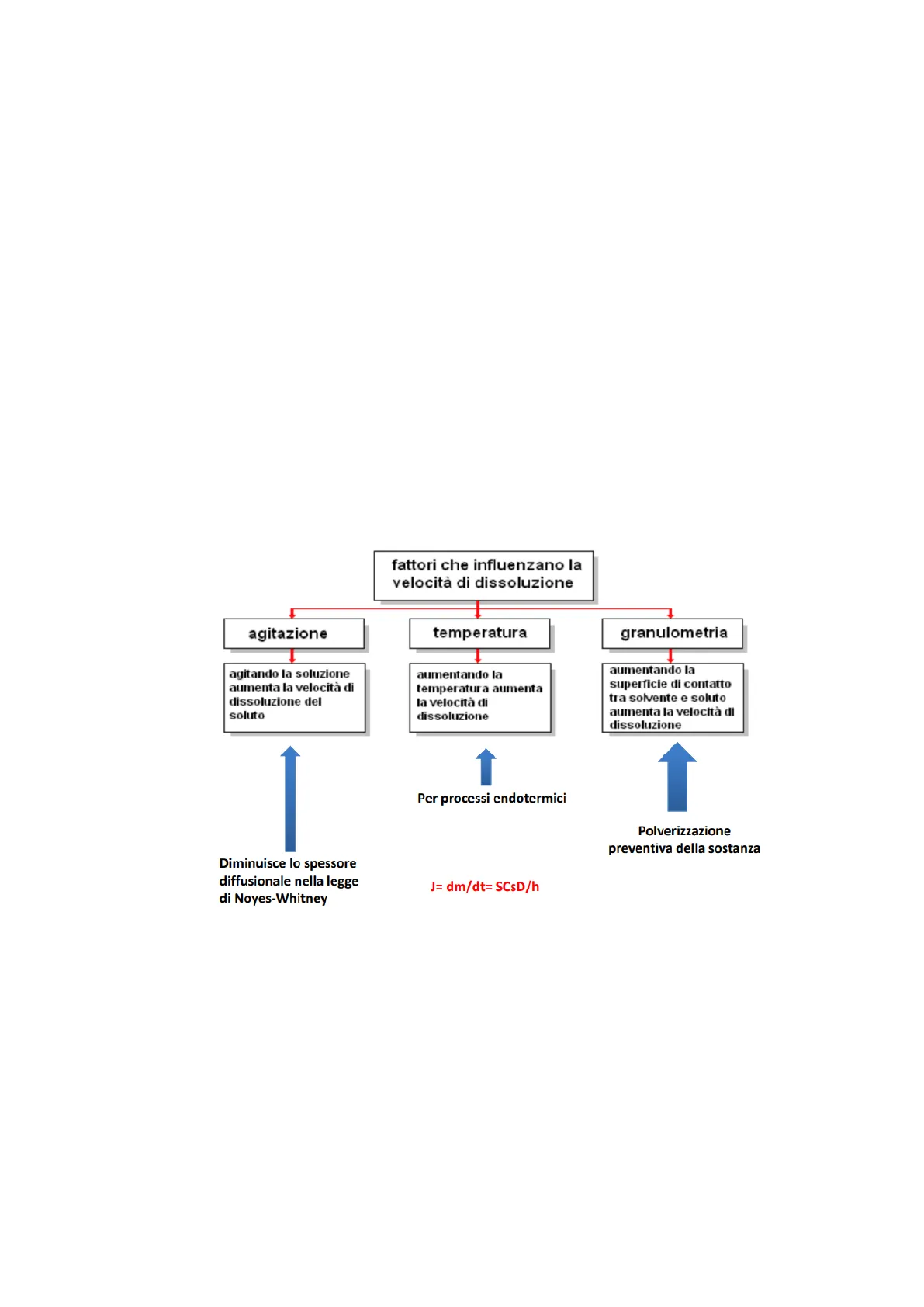
fattori che influenzano la velocità di dissoluzione agitazione temperatura granulometria 1 1 agitando la soluzione aumenta la velocità di dissoluzione del soluto aumentando la temperatura aumenta la velocità di dissoluzione aumentando la superficie di contatto tra solvente e soluto aumenta la velocità di dissoluzione Per processi endotermici Polverizzazione preventiva della sostanza Diminuisce lo spessore diffusionale nella legge di Noyes-Whitney J= dm/dt= SCsD/h
Soluzioni farmaceutiche per uso orale
In definitiva, per soluzioni farmaceutiche per uso orale intendiamo:
- Soluzioni generiche, con varie caratteristiche di limpidezza, pH, via di somministrazione ecc ...
- Sciroppi, che possono essere anche sospensioni o emulsioni. Per sciroppo si intende una formulazione "sciropposa", cioè, costituita da un'elevata concentrazione di zucchero, o almeno lo era in passato, oggi non lo è più. L'elevato contenuto di saccarosio, infatti, era dovuto a vari motivi, come l'attività antimicrobica e l'aumento della viscosità; oggi, queste funzioni sono state tutte sostituite da altri eccipienti come tensioattivi, colloidi ecc ... Inoltre, l'elevato contenuto di zucchero è problematico a livello dietetico e per i pazienti diabetici.
- Gocce, che possono essere soluzioni ma anche sospensioni. Vedremo la fisica della produzione e standardizzazione delle gocce, compresa taratura del contagocce.
- Soluzioni idroalcoliche e quindi elisir.
Vantaggi delle preparazioni liquide
I vantaggi
- I liquidi sono più facili da inghiottire e sono particolarmente accettati per uso pediatrico e geriatrico, quindi maggiore compliance;
- il PA è già disponibile all'assorbimento, non c'è la fase di dissoluzione;
- maggiore flessibilità di dosaggio, utile per principi di autogestione, quindi con elevata sicurezza;
- il farmaco risulta meno irritante per la via orale;
- sono facilmente siringabili, instillabili e deglutibili.
Svantaggi delle preparazioni liquide
Gli svantaggi sono:
- possibile alterazione microbica, in quanto fasi acquose, soprattutto in presenza di zuccheri, e chimica per via del processo di idrolisi esercitato dall'acqua sulle molecole.
- I volumi di soluzione sono difficili da stoccare e trasportare e conservare.
- Vi sono poi farmaci che non si prestano a formare soluzioni; quindi, vi sono anche problemi legati alla solubilità.
- La versatilità del dosaggio rientra anche come svantaggio, poiché è più facile sbagliare il dosaggio.
- Necessità di correzione delle proprietà organolettiche.
Dissoluzione e Solubilità
La differenza tra dissoluzione e solubilità è che la prima indica il passaggio in soluzione di una sostanza solida, mentre la solubilità è la massima quantità di sostanza che (ad una determinata temperatura) può andare stabilmente in soluzione nella quantità unitaria del solvente. In presenza di un corpo di fondo, è la concentrazione a cui si stabilisce un equilibrio tra il soluto in soluzione e l'eccesso di sostanza non disciolta.
La solubilità viene espressa come il numero di millilitri di solvente necessari a solubilizzare 1 g di sostanza, ad una temperatura compresa tra 15°℃ e 25℃. Si trova tabellata nelle schede tecniche. Quando si supera la concentrazione massima indicata dalla solubilità, anche di una molecola, il solido inizia a precipitare al fondo del recipiente.
Quando all'esame viene chiesto di determinare la solubilità, è possibile sciogliere molto solido nel solvente (a volume noto) fino ad avere la precipitazione del corpo di fondo a quella specifica temperatura, che viene stabilizzata, e si misura quanto è la massa di solido solubilizzata. La farmacopea indica un modo semplice per indicare la solubilità, cioè in mL di acqua necessari per solubilizzare 1g di soluto, e si esprime come 1:X, cioè un 1g di sostanza si solubilizza in X ml di acqua. Maggiore è il volume di acqua necessario a solubilizzare, meno solubile sarà la sostanza in esame. A partire da questo concetto, posso impostare la proporzione per sapere quanti g di soluzione posso sciogliere in un determinato volume di acqua.
Grado di solubilità secondo la farmacopea
Indicazione Volune approssimativo di solvente in millilitri per grammo di sostanza Solubilissimo meno di 1 Molto solubile da 1 a 10 Solubile da 10 a 30 Moderatamente solubile da 30 a 100 Poco solubile da 100 a 1000 Molto poco solubile da 1000 a 10000 Praticamente insolubile più di 10000 La farmacopea esprime il grado di solubilità con dei termini: andando da solubilissimo, la condizione ideale dove 1 ml di acqua scioglie 1g di sostanza a praticamente insolubile dove servono 10 L di acqua per sciogliere 1g di sostanza, a praticamente insolubile. Non esiste l'insolubilità assoluta, vi è sempre un rapporto di equilibrio in cui almeno una molecola passa in soluzione.
Modi per indicare la concentrazione delle soluzioni
Oltre a questa modalità, vi sono anche altre espressioni di solubilità, elencati qui a fianco.
% in peso (% p/p) g di soluto /100 g di soluzione % in volume (% p/v) g di soluto /100 ml di soluzione Parti in peso (A/B p/p) A g di soluto /B g di soluzione Parti in volume (A/B v/v) A ml di soluto /B ml di soluzione Molare (M) Moli di soluto / L di soluzione Molale (m) Moli di soluto / kg di solvente Parti per milione (ppm) Mg di soluto /L di soluzione
Esempio: sodio benzoato ha solubilità 1:2, cioè 1g di sale sodico di acido benzoico è solubile in 2 ml di acqua. Se ho 100 ml di soluzione, per solubilizzare me ne servono almeno 2, quindi se ho più, idealmente, devono immaginare di lasciare sempre almeno 2 ml di acqua per quel grammo di benzoato sodico. Nella realtà non è così, perché l'acqua non interagisce solamente con una molecola, ma anche con più molecole contemporaneamente. È una semplificazione funzionale alla formulazione. Se il farmaco non si scioglie in quel volume richiesto, basta aggiungere un cosolvente oppure ciclodestrine, oppure possiamo fare micelle con tensioattivi.
Si può anche salificare un principio attivo, se è possibile farlo.
Esempio: preparo 100 g di una soluzione acquosa di sodio benzoato al 5% m/m, cioè 5 g di PA in 100 g di soluzione. Se 1 g vuole 2 mL per solubilizzare il PA, mi servono 5x2= 10 mL per solubilizzare, quindi mi rimangono 90 g di acqua disponibile per il resto della preparazione (100 - 10 = 90).
Esempio: Papaverina cloridrato, solubilità in acqua 1:30, quindi 30 ml di acqua per grammo di papaverina. Immaginiamo di fare 25 g di soluzione al 5% m/m, cioè 5 grammi in 100 g di soluzione e 1,25 di g papaverina in 25 g di soluzione.
Poiché la solubilità è 1:30, 1,25x30= 37,5 ml di acqua necessari a solubilizzare. L'acqua disponibile per la preparazione è uguale a 25-1,25= 23,75 mL.