Cristallochimica: la natura degli elementi chimici
Slide di Università sulla cristallochimica e la natura degli elementi chimici. Il Pdf esplora la struttura atomica, i legami chimici (ionici, covalenti, metallici) e non covalenti (idrogeno, van der Waals), con tavola periodica e particelle atomiche, utile per lo studio della Chimica.
Mostra di più26 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Cristallochimica e Elementi Chimici
3- Cristallochimica - La natura degli elementi chimici I minerali sono costituiti di elementi chimici in varie combinazioni - questi, a loro volta, sono costituiti da protoni, neutroni ed elettroni. Altri costituenti della materia come neutrini, quark, ecc ... sono molto importanti per i fisici teorici, quindi non in questo contesto ... Protoni e neutroni sono tenuti insieme nel nucleo da forze ancora poco conosciute che sovrastano le forze di repulsione elettrostatica normalmente esistenti tra cariche dello stesso segno. Il numero atomico (Z) è il numero di protoni presenti in un elemento. Si conoscono attualmente 11O elementi diversi, ma alcuni di questi con numero atomico 43 (Tc), 61 (Pm), 85 (At) e maggiore di 92 (elementi transuranici) non sono mai stati ritrovati in natura, ad accezione del Pu (94). Un isotopo di un elemento (es: 40K) è un atomo che differisce da un altro isotopo dello stesso elemento (es: 39K) per il numero di neutroni (20 vs. 19, rispettivamente; Z=19). La somma dei protoni e dei neutroni è il peso atomico (40 e 39, nel caso precedente).
Particelle Atomiche Principali
The Principal Atomic Particles Particle Electric Charge Atomic Mass Unitsª Proton +1 1.00728 Neutron 0 1.00867 Electron -1 0.00055 a1 AMU = 1/12 the weight of a 12C atom.
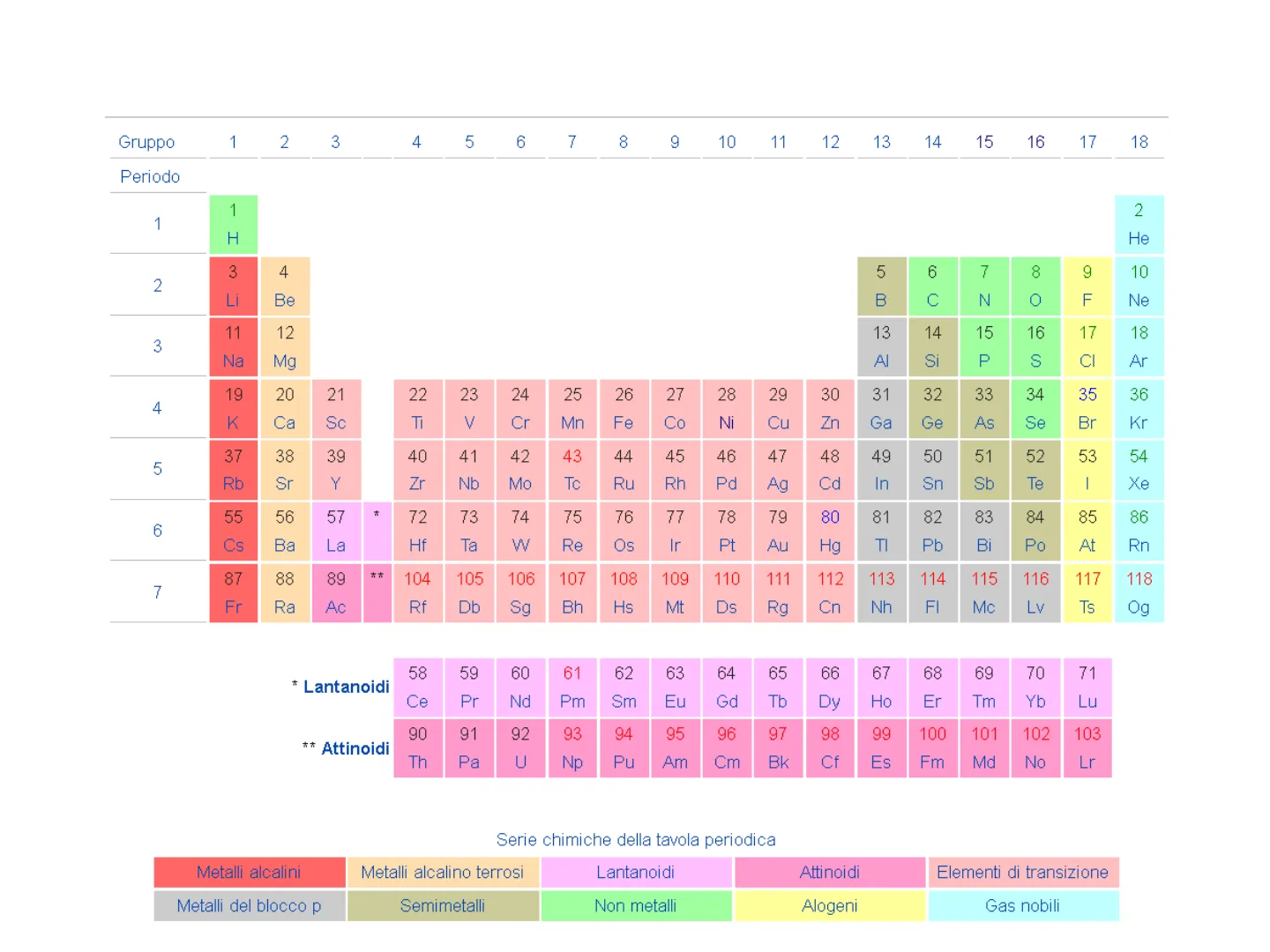
Tavola Periodica degli Elementi
Serie Chimiche della Tavola Periodica
Tavola Periodica degli Elementi Gruppo 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 Periodo 2 1 H He 5 6 7 8 9 10 2 Li Be B C N 0 F Ne 11 12 13 14 15 16 17 18 3 Na Mg Al Si P S CI Ar 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 55 56 57 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg TI Pb Bi Po At Rn 87 88 89 104 105 106 107 108 109 110 111 112 113 114 115 116 117 118 7 Fr Ra Ac Rf Db Sg Bh Hs Mt Ds Rg Cn Nh FI Mc Lv Ts 0g 58 59 60 61 62 63 64 65 66 67 68 69 70 71 Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu 90 91 92 93 94 95 96 97 98 99 100 101 102 103 ** Attinoidi Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Serie chimiche della tavola periodica Metalli alcalini Metalli alcalino terrosi Lantanoidi Attinoidi Elementi di transizione Metalli del blocco p Semimetalli Non metalli Alogeni Gas nobili
Gruppi della Tavola Periodica
1 3 4 4 5 6 * Lantanoidi **Tavola Periodica degli Elementi I gruppi (o famiglie) raggruppano gli elementi che si trovano sulla stessa colonna della tavola periodica.
- I gruppi sono indicati numericamente da 1 a 18 dalla colonna più a sinistra (i metalli alcalini) alla colonna più a destra (i gas nobili).
He 3 4 5 6 7 8 9 10 " Ogni gruppo comprende gli elementi che hanno la stessa configurazione elettronica esterna (cioè il modo in cui gli elettroni si dispongono attorno al nucleo).
13 14 15 16 17 18 3
- Le proprietà chimiche degli elementi dipendono dalla loro configurazione elettronica: all'interno di ogni gruppo si trovano elementi con caratteristiche chimiche simili (cioè che si comportano in 35 36 Ca Co Ga Ge AS Se Br maniera simile durante lo svolgimento delle reazioni chimiche).
40 41 48 52 53 54 49 50 51 Te Gli elementi mostrano un chiaro andamento delle proprietà lungo il gruppo:
81 56 4 00 Au Hg 83 95 i livelli energetici riempiti, e gli elettroni esterni si trovano a maggiore distanza dal nucleo. 86 89 1 Xe 4 106 107 |108 |109 |110 111 112 11390 115 116 117 118 Muovendosi dall'alto verso il basso diminuisce l'energia di ionizzazione, poiché è più facile allontanare un elettrone dall'atomo, in quanto gli elettroni sono meno strettamente legati al nucleo.
58 59 60 61 62 64 66 67 68 70 63 65 71 69 L'antanoidi Ce Eu Gd Tb Pr Nd Pm Sm Tm Lu Similmente, un gruppo generalmente presenta una diminuzione dell'elettronegatività andando dall'alto verso il basso, poiché aumenta la distanza tra gli elettroni di valenza e il 92 95 96 98 9 nucleo.
Serie Chimiche e Proprietà
Serie chimiche della tavola periodica Metalli alcalini Metalli alcalino terrosi Lantanoidi Attinoidi Elementi di transizione Metalli del blocco p Semimetalli Non metalli Alogeni Gas nobili Sc Fe 38 39 44 43 45 46 Kr 37 47 42 'O muovendosi dall'alto in basso i raggi atomici degli elementi aumentano poiché aumentano Rr CS Ba OS b At Dy Ho Er 5Tavola Periodica degli Elementi
Periodi della Tavola Periodica
- I periodi (o serie) raggruppano gli elementi che si trovano sulla stessa riga della tavola periodica. Ogni periodo incomincia con un elemento che ha nella configurazione elettronica esterna un elettrone di tipo ns; il n. atomico Z aumenta di un'unità ad ogni passaggio procedendo verso destra.
He
- Gli elementi dello stesso periodo hanno lo stesso numero di orbitali atomici.
7 8 9 2 10
- Sebbene il gruppo di appartenenza influenzi fortemente il comportamento chimico degli elementi, in alcuni casi gli elementi che mostrano proprietà chimiche simili sono quelli appartenenti allo stesso periodo, come nel caso dei lantanoidi e degli attinoidi del blocco f.
Al Si P S CI Ar 19 20 23 24 26 27 31 32 34 21 22 5 30 28 29 33 35 36 Si osservano in seno ai periodi variazioni monotone del raggio atomico, dell'energia di ionizzazione, dell'affinità elettronica e dell'elettronegatività:
44 45 46 47 48 49 51 50 52 53 54 muovendosi da sinistra verso destra il raggio atomico solitamente diminuisce poiché ciascun Cd Rh Xe elemento possiede rispetto al precedente un protone e un elettrone in più, per cui la forza con cui gli Ba Re OS Pb Bi Po At Hg Ir Pt Au Rn 118 elettroni sono attirati verso il nucleo aumenta.
87 89 108 88 104 105 106 107 109 110 111 112 113 114 115 116 117
- Questo fa si che anche l'energia di ionizzazione (energia richiesta per allontanare un e-) aumenti da sx vs. dx: tanto più strettamente l'elettrone è legato all'atomo, tanto maggiore è l'energia richiesta per allontanarlo.
58 59 60 61 62 63 64 Lantanoidi
- L'elettronegatività (capacità dell'atomo di attrarre gli e coinvolti nel legame covalente) aumenta allo stesso modo dell'energia di ionizzazione a causa dell'attrazione esercitata sugli elettroni dal nucleo.
Pa Cf Cm | Bk Es Fm Md No Lr
- I metalli (lato sx del periodo) hanno generalmente una minore (meno negativa) affinità elettronica (energia scambiata quando un e è aggiunto ad un atomo) dei non metalli (lato dx del periodo), con l'eccezione dei gas nobili (affinità positiva).e della tavola periodica Metalli alcalini Metalli alcalino terrosi Lantanoidi Attinoidi Elementi di transizione Metalli del blocco p Semimetalli Non metalli Alogeni Gas nobili Th Am Np Pu 65 66 70 71 67 68 69
Blocchi della Tavola Periodica
Tavola Periodica degli Elementi A causa dell'importanza del guscio elettronico più esterno, le diverse regioni della tavola periodica sono talvolta chiamate blocchi, denominati secondo il sottoguscio in cui risiede l'"ultimo" elettrone.
- Il blocco s comprende i primi due gruppi (metalli alcalini e metalli alcalino-terrosi) nonché l'idrogeno e l'elio.
- Il blocco p comprende gli ultimi sei gruppi, che corrispondono ai gruppi da 13 a 18, e contiene, tra gli altri, tutti i metalloidi.
- Il blocco d comprende i gruppi da 3 a 12 e contiene tutti i metalli di transizione.
- Il blocco f, di solito collocato sotto il resto della tavola periodica, comprende i lantanoidi e gli attinoidi.
blocco s 1 blocco p 18 +1s 2 13 14 15 16 17 +-25++ 2p blocco d 3 5 6 7 8 9 10 11 12 - 3d 4p +55- 4d 5p +65 5d 6p +-7s- 6d 7p blocco f 4f 5f Ionization energy Electron affinity Atomic radius Nonmetallic character Metallic character Electron affinity Ionization energy Atomic radius 1s+ 3p -4s
Abbondanza degli Elementi sulla Terra
Abbondanza degli elementi In aggiunta alle analisi delle rocce accessibili (affioranti o campionabili), le stime dell'abbondanza degli elementi sulla Terra si basano su:
- massa e distribuzione della densità nella Terra ottenute con metodi geofisici;
- composizione dei magmi mantellici (basalti alcalini, komatiti, kimberliti ... ) e dei campioni che con essi arrivano alla superficie (xenoliti);
- composizione delle meteoriti ...
Elementi più Abbondanti nella Crosta Terrestre
The Eight Most Abundant Elements in the Earth's Crusta Earth's Crust Common Oxidation State Total Earth Weight % Element Weight % Atom % Volume % 0 46.6 62.5 91.7 -2 29.5 Si 27.7 21.2 0.2 +4 15.2 Al 8.1 6.5 0.5 +3 1.1 Fe 5.0 1.9 0.5 +2/+3 34.6 Ca 3.6 1.9 1.5 +2 1.1 Na 2.8 2.6 2.2 +1 0.6 K 2.6 1.4 3.1 +1 0.1 Mg 2.1 1.8 0.4 +2 12.7 Total 98.5 99.8 ~100 94.9 a Adapted from Mason and Moore (1982).
Gli Elettroni e Numeri Quantici
Gli elettroni In un atomo neutro il numero di elettroni eguaglia quello dei protoni.
- Gli elettroni orbitano intorno al nucleo non caoticamente, ma secondo determinati livelli energetici rappresentati da 4 numeri quantici: n, I, mi e ms- Il Principio di esclusione del Pauli postula che: «Non possono esistere due elettroni in uno stesso atomo con tutti e 4 i numeri quantici uguali». Il numero quantico principale n può assumere qualsiasi numero intero positivo e si identifica con i livelli K, L, M, N ... (per n = 1, 2, 3, 4 ... ). Rappresenta il raggio medio dell'orbitale e riflette la sua energia ( | E | x 1/n).
(a) n =3 n=1 n=2 S S S Probability of finding electron (47 r2 (2) ITo 0 Distance from the nucleus (r)
Momento Quantico Angolare e Spin
Gli elettroni Il momento quantico angolare / assume valori tra 0 e n -1 e rappresenta le diverse forme dei sottolivelli. Questi vengono normalmente identificati con le lettere s, p, d e f che corrispondono a valori di / = 0, 1, 2 e 3.
- Il numero quantico magnetico m può assumere un numero intero compreso tra -le +l. Distingue tra orbitali con differenti orientazioni in un sottolivello...
- Il numero quantico di spin ms distingue tra i due elettroni che può contenere al massimo un orbitale. I valori possibili sono +1/2 e -1/2 e stanno ad indicare il movimento dello spinning rispettivamente in un verso ed in quello opposto ...
Z A x S Z Z e m spin morb P.1 Po P1 Z 2 Z Z A -y Ax d do d. d2 z Z Z Z Z y y × × x x X x 13 fo f2 f3 spin up spin down AX x A x Ax x 41 NO Z r e e m spin
Configurazione Elettronica e Numeri Quantici
Valency 1 0 HNM 4 MNHOHNM 4 MN 10 1 3 Lithium Li 1s2 2s Beryllium Be 1s2 252 5 Boron B 1s2 202 2p1 Carbon C 1s- 2s2 2p2 7 Nitrogen N 1s2 2s2 2p3 8 Oxygen O 132 2$2 20 9 Fluorine F 1s2 2s2 205 10 Neon Ne 1s2 2$2 2p6 11 |Sodium Na 1s2 2$2 2p6 3st 12 Magnesium Mg 1s2 282 2po 35 13|Aluminum A1 1s2 2s2 205 3s 3p 14 Silicon Si 1s2 2$2 205 3s2 302 15 Phosphorous P 1s2 206 382 3p 16 Sulfur S 1s2 2s2 2p6 352 304 17 Chlorine C1 132 2$2 265 382 3p2 18 Argon Ar 1s2 2s2 205 3s 3p 19 Potassium K 1s2 252 2pº 382 305 4st 20|Calcium Ca 182 202 206 352 30€ 432 21 |Scandium Sc 1s2 2s2 205 382 305 3d1 482 22 Titanium Ti 1s2 2s2 20 3s2 3p6 3d2 432 23 Vanadium V 182 2$2 200 352 3po 3d3 4s2 24 Chromium Cr 132 232 20º 382 305 385 4s' 25 Manganese Mn 1,2 2:2 206 382 306 3d5 482 26 Iron Fe 182 2s2 2p6 382 305 3d5 482 27 Cobalt Co 1:2 232 2p 332 305 3d? 452 28 Nickel Ni 1s2 2s2 205 3s2 3po 3dª 482 29 Copper Cu 1s2 252 205 3s2 306 3d10 4st 30 Zinc Zn 1s2 2s2 2p6 3$2 305 3d10 482 31 |Gallium Ga 1s2 2$2 265 382 306 3₫10 432 4D1 spin ms + , - +, - +, - + , - + . - +, - + , - +, - + , - + , - +,- + ,- +, - + , - +, - -4,-3,-2,-1,0,+1,+2,+3+4 orbital notation symbol 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 5g orbital quantum number I=0 ... n-1 0 C 1 0 1 2 0 1 2 C 2 3 4 period notation symbol × L M Z o principal quantum number C 1 2 3 4 5 Hydrogen H 1s1 2 |Helium He 1s2 4 Z 1 2 Σ 1 2 4 5 6 7 8 8 8 KL 1 2 4 6 7 8 8 8 8 8 8 8 8 8 No. of electron 1 N m 4 5 7 8 9 10 11 12 13 15 16 17 18 19 20 Atomic Number 1 m 4 5 6 8 9 10 11 12 13 15 16 17 18 19 20 Symbol I He 3 Be Beryllium Boron Carbon Nitrogen Oxygen Fluorine Sodium Magnesium Aluminium Silicon Phosphorous Sulphur Chlorine Argon Potassium Calcium maximal number of electrons in period 2 8 18 32 50 shell 2 2 00 2 6 10 2 6 10 14 2 6 10 14 18 magnetic quantum number m C 0 0 -1,0,+1 -2,-1,0,+1,+2, -1,0,+1 -2,-1,0,+1,+2, 0 -1,0,+1 -2,-1,0,+1,+2, -3,-2,-1,0,+1,+2,+3 33 Arsenic As 1s2 2$2 2p5 352 305 3₫10 4$2 4p 34 Selenium Se 1$2 252 2pº 352 306 3d10 432 4D 4 35 Brome Br 1s2 2s2 205 352 306 3₫10 482 4p5 36 Krypton Kr 1s- 2s2 20 352 30 3d10 6 432 4p 2 2 2 2 2 2 2 2 2 2 2 N 2 2 2 N Elements Hydrogen Helium Lithium @ Aco Z. Muradjan MODERN QUANTUM NUMBERS NOTATION 2 Distribution of electron 1 2 2 6 7 muzouž Na Mg Thantax Ca Neon 3 8 2 14 14 N 3 5 -1,0,+1 32 Germanium Ge 1s2 202 205 352 3p6 3₫10 432 4p2 0 -3,-2,-1,0,+1,+2,+3 3 1 6