Metodos opticos: Generalidades sobre espectroscopia y radiacion electromagnetica
Documento de Universidad sobre Metodos Opticos: Generalidades. El Pdf explora la espectroscopia, la naturaleza de la radiacion electromagnetica, sus modelos ondulatorio y corpuscular, y los componentes como selectores de longitud de onda y detectores, ideal para Fisica.
Ver más13 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Métodos Ópticos: Generalidades
Espectroscopia
La espectroscopía es una rama de las ciencias Física y Química que se ocupa del estudio de los espectros. Este estudio es muy amplio y comprende desde los diversos métodos para la obtención de espectros, su medida y aplicación química, principalmente de tipo analítico (que constituye lo que se denomina 'espectroquímica'), hasta su interpretación teórica en relación con la estructura atómica-molecular de la materia. De hecho, fue el primero de los campos que dio datos suficientes para interpretar la estructura de la materia. Su estudio consiste en la interacción entre la radiación electromagnética y la materia. De esta interacción se saca información de: ángulos de enlace, distancia entre moléculas, geometría de las moléculas, identificación de elementos y moléculas, concentración de un elemento o compuesto. Por ello, un espectro puede definirse como una representación gráfica (o fotográfica) de la distribución de intensidad de radiación electromagnética emitida o absorbida por una muestra en función de la longitud de onda (o de la frecuencia) de dicha radiación.
Naturaleza de la Radiación Electromagnética
Para explicar la naturaleza de la radiación electromagnética había dos modelos propuestos:
Modelo Ondulatorio
La describe como formada por dos campos (eléctrico y magnético), perpendiculares entre sí, que se desplazan desde la fuente generadora de la radiación con la velocidad de la luz en el vacío. Campo eléctrico ad x Z Campo magnético Las magnitudes que definirían dicha radiación son:
- Frecuencia (v): Es el número de oscilaciones completas de la onda cada segundo. Sus unidades son: 'inversa de segundo' [1/s, s-1] o Hertz [Hz]. amplitud 6 periodos en un segundo frecuencia = 6 Hz 1 segundo tiempo 1° periodo = 1/6 segundo L.C.L Prof. Elena Falqué López 1"Análisis Instrumental" Métodos ópticos: Generalidades
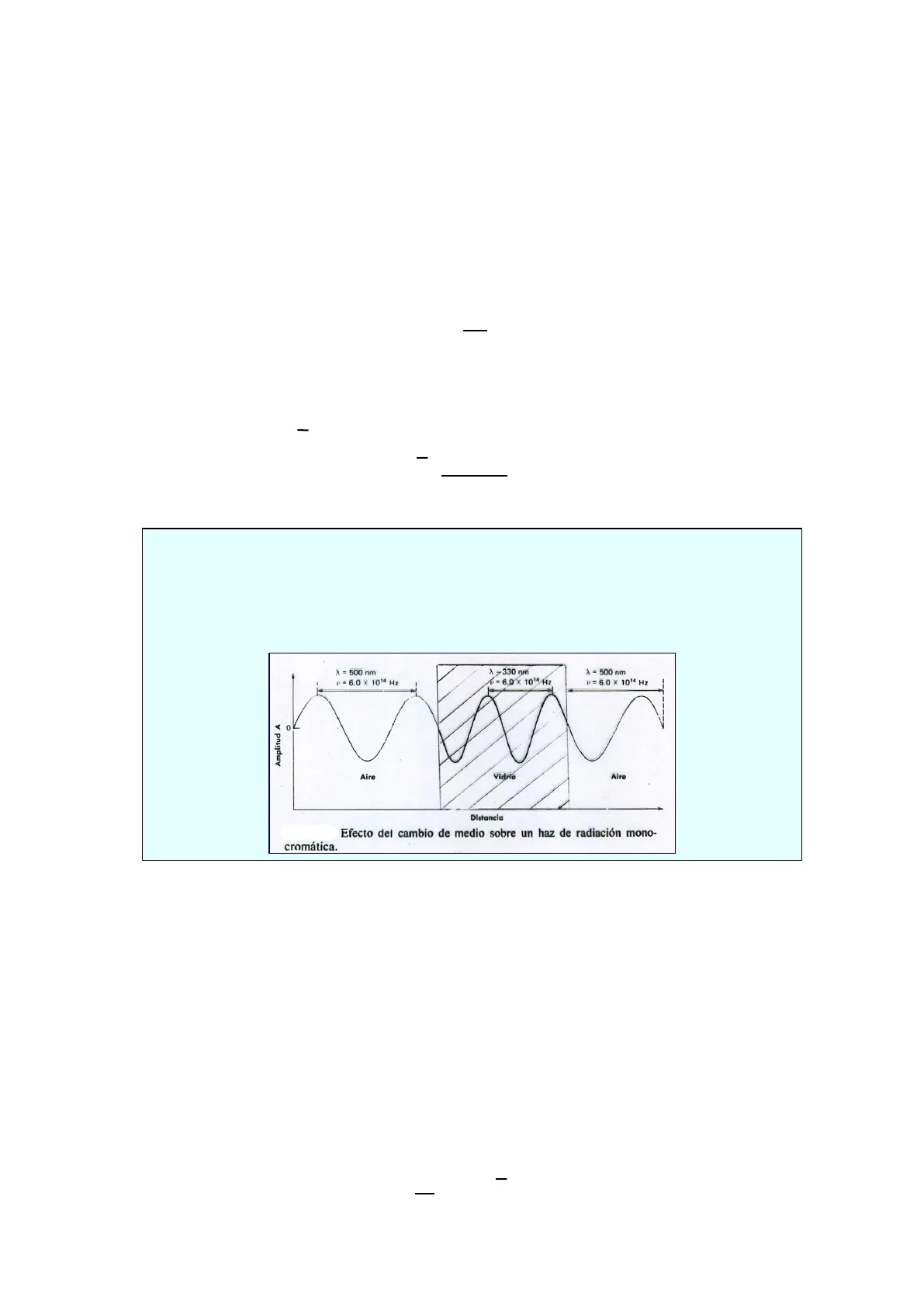
- Longitud de onda (2): Es la distancia lineal entre máximos o mínimos sucesivos de una onda. Sus unidades más frecuentes son: 1 Å (angström) = 10-10 m = 10-8 cm 1 nm (nanometro) = 10-9 m = 10-7 cm Ambas están relacionadas a través de la siguiente expresión: V= C 2 _ _ donde c es la velocidad de la luz en el vacío [c=2,99792458.108 m/s ~ 3.108 m/s =3.1010 cm/s]. Número de onda ( ): Es el número de ondas por cm. Su unidad es [cm-1 ]: = 1 2 (en cm) En un medio distinto del vacío, la velocidad de la luz es igual a "c/n" (donde n es el índice de refracción). Como 'n' es siempre ≥ 1, la luz se propaga más lentamente en un medio material que en el vacío. Cuando la luz pasa de un medio a otro cuyo índice de refracción es mayor, su frecuencia no varía, pero la longitud de onda disminuye. X = 500 nm P = 6.0 × 1014 Hz X -330 nm v = 6.0 × 1014 Hz A = 500 nm v = 6.0 × 1014 Hz 0 Amplitud A Aire Vidrio Aire Distancia Efecto dei cambio de medio sobre un haz de radiación mono- cromática.
Modelo Corpuscular
Se basa en las Leyes de Newton de la Mecánica clásica, y considera la luz, o las radiaciones electromagnéticas, como formadas por un flujo de partículas o corpúsculos (denominados fotones). La energía del fotón depende únicamente de la frecuencia de la radiación: E = h.v donde h: constante de Planck = 6,626.10-34 J.s = 6,626.10-27 erg.s Al combinar ambas teorías, se obtiene que: E = h.v = h. c = h.c.6 2 Prof. Elena Falqué López 2"Análisis Instrumental" Métodos ópticos: Generalidades
Espectro Electromagnético
Existen distintos tipos de energía: traslación, rotación, vibración, electrónica, nuclear y de orientación de spines. Los distintos tipos de energía de los sistemas atómicos o moleculares son de un orden de magnitud bastante diferente, por lo que las transiciones entre los correspondientes niveles de energía dan lugar a emisión o absorción en distintas zonas de frecuencia. La siguiente clasificación corresponde a valores de u crecientes (es decir, de E crecientes; es decir, de 2 decrecientes):
- Región de las radiofrecuencias (u ondas de radio). [3.106 - 3.1012 Hz] Originadas por transiciones entre niveles de energía muy baja, debidas a las orientaciones de los momentos magnéticos de spin nuclear y electrónico en presencia de un fuerte campo magnético exterior. RMN (Resonancia magnético nuclear) => para el spin nuclear. RSE o RPE (Resonancia de spin electrónico / Resonancia paramagnético electrónica) => para el spin electrónico. El estudio se realiza en moléculas con electrones desapareados. V MO (Microondas) => Provoca rotación de las moléculas. Para que una molécula sea activa en el microondas es necesario que tenga el momento dipolar (u) # 0, y que este sea permanente. Por tanto, las moléculas homonucleares no se pueden estudiar en esta zona.
- Región del Infrarrojo (IR). [3.1012 - 3.1014 Hz] Corresponde a cambios de la energía vibratoria de las moléculas; es decir, es la energía necesaria para producir transiciones vibracionales. En el IR lejano también se estudian las transiciones rotacionales puras. En el IR no es necesario que la molécula tenga momento dipolar permanente, pero sí que cambie su momento dipolar durante la vibración; por lo que para moléculas diatómicas, sólo las heteronucleares (FH, ClH, CO, NO ... ) presentan espectro en IR.
- Región del visible (vis) y ultravioleta (UV). [3.1014 - 3.1016 Hz] Corresponde a cambios de niveles energéticos de los electrones externos o de valencia o de la corteza de átomos, iones atómicos, moléculas e iones moleculares, por ello también se llaman espectros electrónicos. Como para dichas transiciones intervienen solamente los electrones externos, los espectros varían en función de si participan en el proceso átomos individuales o bien compuestos moleculares: · Átomos individuales. Los espectros de absorción y de emisión presentan líneas definidas, que corresponden a las transiciones entre los niveles energéticos permitidos del átomo. Dan espectros de líneas. Prof. Elena Falqué López 3"Análisis Instrumental" Métodos ópticos: Generalidades 5p 4.0 40 3.0 Absorbancia Energia, eV 2.0 3p 1.0 285 nm 330 nm 590 nm 200 300 400 500 600 0 3 Longitud de onda, nm (a) (b) · Moléculas. Los espectros de absorción y emisión son más complicados, ya que las transiciones electrónicas vienen acompañadas de cambios simultáneos en los estados de vibración o rotación de las moléculas, por eso se obtienen espectros de bandas. IR VIS UV E O-NYA Energia E 200 300 500 600 Longitud de onda, nm E O-NGA
- Región de los rayos X. [3.1016 - 3.1018 Hz] Corresponde a saltos electrónicos de electrones internos. Estos son característicos de cada átomo y prácticamente no dependen de los enlaces químicos; es decir, no dependen de la molécula en que se encuentren dichos átomos. Son las radiaciones de menor longitud de onda atribuibles a cambios reversibles en la composición electrónica del átomo.
- Región de los rayos y. [3.1018 - 7.1021 Hz] Corresponden a cambios energéticos de los niveles nucleares, y nos dan información sobre la estructura nuclear. Son prácticamente independientes del entorno de los núcleos atómicos. Los átomos radioactivos emiten espontáneamente rayos y con energías definidas y discretas que corresponden a los niveles cuantizados del átomo. Prof. Elena Falqué López 4"Análisis Instrumental" Métodos ópticos: Generalidades Espectro visible por el ojo humano (Luz) Ultravioleta Infrarrojo 400 nm | 450 nm 500 nm 1 550 nm 600 nm 650 nm 700 nm 750 nm Rayos cosmicos Rayos Gamma Rayos X UV- A/B/C Ultravioleta Infrarrojo Radar UHF VHF Onda media Onda corta Onda larga Frecuencia extremadamente baja Microondas Radio 1 fm 1 pm 1 A 1 nm 1 um 1 mm 1 cm 1 m 1 km 1 Mm Longitud de onda (m) 10-15 -14 10-13 10-12 10-11 10-10 10-9 10-8 10-7 10 -6 10-3 10 4 10 -3 10-2 10 -1 10° 101 102 103 104 103 10º 107 Frecuencia (Hz) 10 23 10 22 10 2 10 19 10 17 10 15 10 14 10 12 10 10 10 107 10 105 10 10 10 [1 Tera-Hz) (1 Mega-Hz) (1 Kilo-Hz) Energía Número de onda a Longitud de onda X Frecuencia Tipo de radia- ción Tipo de Tipo de kcal/mol Electro- volts ev cm -1 cm Hz espectroscopio transición cuántica 9.4 × 107 4.1 × 106 3.3 × 1010 3 . 10 11 1021 Rayos gamma 4 Emisión de rayos gamma Nuclear 9.4 × 105 4.1 × 104 3.3 × 108 3 × 10-9 1019 Emisión absorción de rayos X Electrónica (capa interna) 9.4 × 103 4.1 × 102 3.3 ¥ 106 3 × 10 7 1017 Ultra violeta Absorción UV en el vacío 9.4 x 10' 4.1 Y 10º 3.3 × 104 3 × 10-5 1015 A UV Vis absorción emisión, fluorescencia 9.4 x 10 4.1 × 10-2 3.3 X 102 3 × 10 3 1013 Infra- rrojos Absorción IR, Raman Vibración molecular Rotación molecular 9.4 × 10 4.1 x 10- 3.3 × 10° 3 × 10 ' 1011 Micro onda Absorción de microondas 9.4 ¥ 10 5 4.1 > 10 6 3.3 × 10 2 3 . 10' 109 Resonancia paramagnética electrónica Estado de espín inducidos 1 magnéticamente Radio Resonancia magnética nuclear 9.4 × 10 7 4.1 / 10-8 3.3 × 10 4 3 . 103 107 Prof. Elena Falqué López 5 10 21 [1 Zetta-Hz) 10 18 (1 Exa-Hz) 10 15 [1 Peta-Hz) 10 13 10 11 109 (1 Giga-Hz) 8 4 3 Rayos X t Electrónica (capa externa) Visibles"Análisis Instrumental" Métodos ópticos: Generalidades
Clasificación de los Métodos Ópticos
Los métodos ópticos se clasifican en espectroscópicos y no espectroscópicos:
Métodos Espectroscópicos
Los cuales pueden ser de 3 tipos fundamentales:
- a. ABSORCIÓN. Si hacemos incidir una radiación con una longitud de onda determinada, interaccionan los fotones con la materia, produciéndose una absorción de energía por dicha materia y, dependiendo de la energía, se producen distintos fenómenos: transiciones electrónicas, vibraciones, rotaciones ... Se obtiene el espectro de absorción.
- b. EMISIÓN. Si un átomo o molécula absorbe energía, pasará a un estado excitado, en el cual permanecerá un tiempo (que depende de su estado de relajación), para después emitirla y volver a su estado fundamental. El tiempo de relajación es del orden de 10-12 s; transcurrido este, se produce la emisión: espectro de emisión. La emisión se puede producir de dos formas: of Se transforma la energía absorbida en energía calorífica, y se transmite este calor al medio. * Se reemite la radiación absorbida. Generalmente, la emisión ocurre como combinación de las dos formas. En el caso de que suceda como la segunda, nos encontramos con los espectros de emisión. Generalmente, los espectros de emisión moleculares se estudian en absorción, ya que es difícil excitar las moléculas, sin romperlas, a niveles energéticos superiores para obtener los espectros de emisión.
- c. RAMAN. En el espectro Raman interviene un tipo especial del proceso de dispersión. La dispersión es la variación en el índice de refracción de una sustancia con la frecuencia o la longitud de onda. Difiere de la dispersión ordinaria en que parte de la radiación dispersada sufre cambios cuantizados de frecuencia. La emisión de la radiación puede ser de: * la misma v => dispersión de Rayleigh. * v inferior a la de la radiación incidente => líneas de Stokes. * v superior a la de la radiación incidente => líneas de anti-Stokes. IR y Raman son técnicas complementarias, dado que la primera mide la radiación absorbida por el sistema, y Raman mide la dispersada. Prof. Elena Falqué López 6