Coagulopatia nel trauma: meccanismi e valutazione diagnostica
Documento sulla coagulopatia nel trauma. Il Pdf, utile per l'Università in Scienze, esplora i meccanismi di coagulazione intrinseca ed estrinseca, le loro alterazioni e l'importanza della triade letale, supportato da diagrammi e tabelle.
Mostra di più17 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Coagulopatia nel trauma
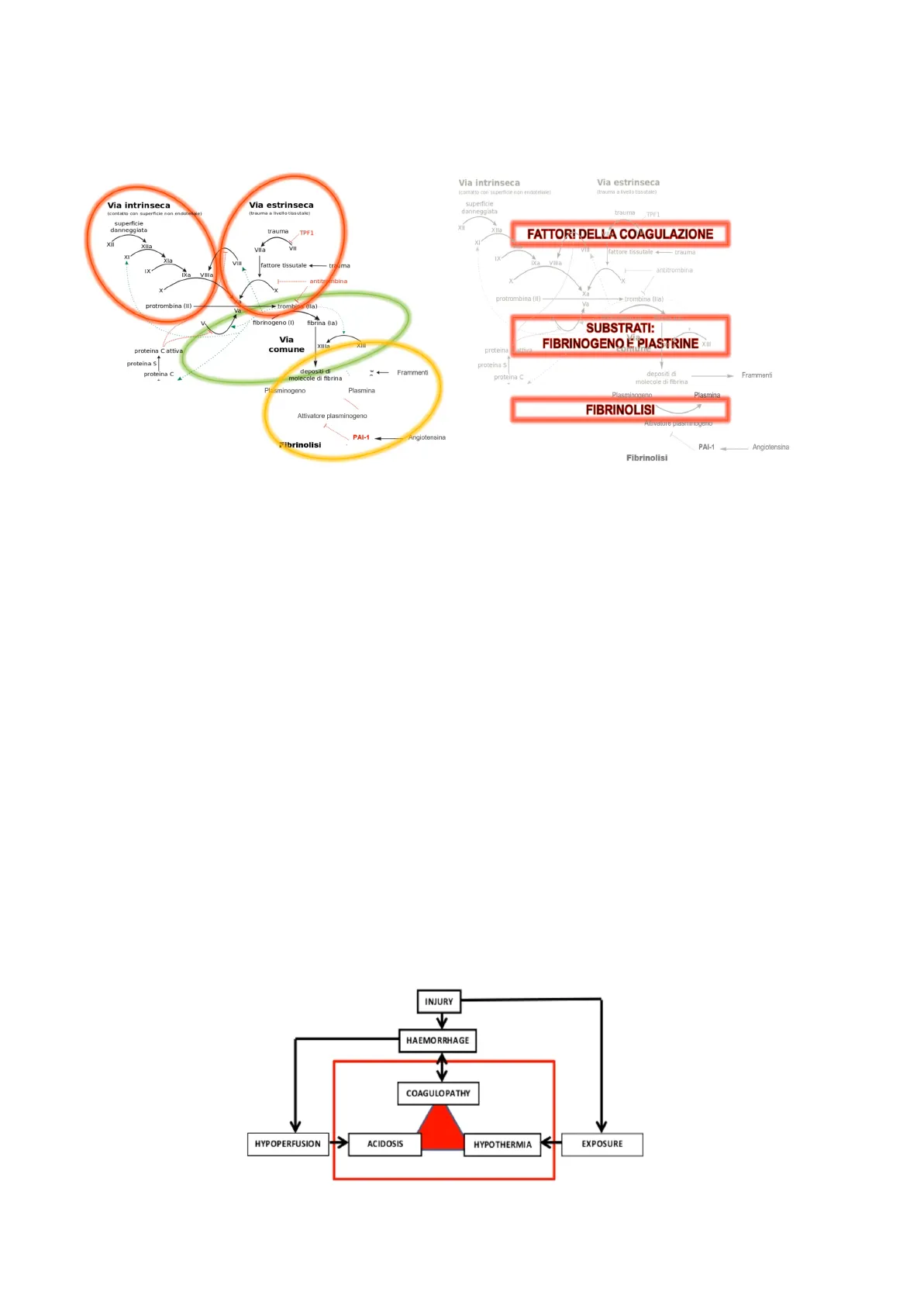
Via intrinseca
(contatto con superficie non endoteliale)
superficie
danneggiata
trauma
TPF
XII
Xlla
FATTORI DELLA COAGULAZIONE
XI
fattore tissutale 4- trauma
IX
IXa VIIIa
· antitrombina
IXa VIIIa
antitrombina
×
×
xã
protrombina (II)
trombina (Ila) ..
protrombina (II)-
trombina (Ila).
va
fibrinogeno (1)
fibrina (la)
Via
comune
XIIla
XIII
proteina C attiva
proteina
Lattiva
proteina S
Frammenti
proteina C
depositi di
molecole di fibrina
Plasminogeno
Plasmina
FIBRINOLISI®
Allivature plasminogeno
PAI-1
Angiotensina
Fibrinolisi
PAI-1
Angiotensina
Fibrinolisi
- La via estrinseca è più rapida per il minor numero di fattori che vi prendono parte. Essa viene
attivata quando una lesione di un vaso sanguigno produce la liberazione, dalle cellule
danneggiate, di fosfolipidi e di un complesso proteico detto fattore tissutale o tromboplastina
tissutale. - La via intrinseca è più lenta, perché comprende un maggior numero di fattori della
coagulazione. Questa via è innescata dall'attivazione del fattore XII, o fattore di Hageman, che
si verifica quando il sangue entra a contatto con superfici diverse da quella vasale. A
differenza della via estrinseca, la via intrinseca prevede il coinvolgimento solo di fattori
plasmatici e non di altri fattori, come ad esempio quelli tissutali.
Una lesione tissutale è in grado di attivare sia la via estrinseca che la via intrinseca, in quanto in
caso di danno al vaso, non solo si libera la tromboplastina tissutale ma si espone il sangue
all'inevitabile contatto con una superficie "estranea" diversa da quella endoteliale.
Cosa succede nel trauma?
Nel trauma, si verifica un'emorragia, spesso così profonda da provocare shock emorragico, che
rappresenta la forma più frequente di shock nel politrauma.
L'emorragia innesca:
- ipoperfusione, con conseguente sviluppo di acidosi metabolica, generalmente lattica.
- coagulopatia, alla cui genesi partecipa anche il trauma stesso.
Inoltre, il paziente traumatizzato è esposto a basse temperature, indipendentemente dalla
stagione (succede anche in estate), che determina ipotermia.
La coagulopatia, l'acidosi e l'ipotermia costituiscono la triade letale del trauma, in quanto la loro
associazione aumenta la mortalità del trauma anche dopo l'emostasi chirurgica, se non trattati
precocemente.
INJURY
HAEMORRHAGE
COAGULOPATHY
HYPOPERFUSION
ACIDOSIS
HYPOTHERMIA
Via estrinseca
(trauma a livello tissutale)
Via intrinseca
Via estrinseca
(trauma a livello tissutale)
(contatto con superficie non endoteliale)
superficie
danneggiata
trauma
TPF 1
XII
Xila
VIla
VII
XI
Xla
VÌ !!
fattore tissutale 4 trauma
IX
proteina C
+
depositi di
molecole di fibrina
==
Frammenti
Plasminogeno
Plasmina
Attivatore plasminogeno
proteina s
SUBSTRATI:
FIBRINOGENO E PIASTRINE
XIII
Va
EXPOSURE
11. Coagulopatia
INCIDENZA DI MORTALITA'
100%
80%
60%
40%
20%
ONormal
Coagulopathy
0%
0-14
15-29
30-44
45-59
59-64
Injury Severity Score
La coagulopatia correla con la prognosi del
paziente traumatizzato: quanto più le
condizioni cliniche sono gravi (Injury severity
score >15, che definisce il trauma grave),
tanto più la coagulopatia si esacerba,
determinando un aumento della mortalità.
Perché il paziente traumatizzato va incontro a coagulopatia?
- DILUIZIONE PRIMARIA, determinata dal richiamo di liquidi dall'interstizio (e dal III spazio)
al
compartimento
intravascolare.
Questo
fenomeno,
consensualmente alla
vasocostrizione, consente di mantenere la volemia e la PA in corso di emorragia. - DILUIZIONE SECONDARIA, avviene per infusione di un eccessivo quantitativo di da fluidi
e/o emocomponenti che non contengono molecole che contribuiscono alla coagulazione.
Se non accompagnata da plasma o concentrati di fattori della coagulazione, anche la
somministrazione di sole emazie concentrate contribuisce all'emodiluzione, perché il
plasma ivi contenuto (1 U EC 250 ml = 35 ml di plasma) non è sufficiente a soddisfare le
richieste. Al fine di ridurre l'entità della diluizione secondaria, se il paziente non risponde
alla somministrazione di 1L di cristalloidi, si procede con la trasfusione di emocomponenti.
La diluizione secondaria determina una deficienza relativa di fattori della coagulazione, Hb
e piastrine. Esiste una correlazione tra il grado di diluizione ed il quantitativo di fattori
della coagulazione e dei substrati. In uno studio in vitro sono stati valutati i valori di PT (s),
ptt, fibrinogeno e PLT in campioni con diluizioni crescenti, riscontrando significativi cambi
delle microstruttura del coagulo per diluizioni > 20% con correlazione alla concentrazione
di fibrinogeno e di piastrine.
Table of results for the standard laboratory markers, rheological measurements and imaging results for all dilutions. (n = 18 for each dilution) *denotes a significant deviation from
the baseline value using one way ANOVA Tukey's pairwise analysis where p < 0.05).
Dilution
Vol %
Standard Laboratory Markers
Rheology
Fibrinogen (clauss)
Haematocrit
Platelet Count
×10°
Mean (SD)
Prothrombin
Time, PT
sec
Thromboplastin
Time APTT
TCP.
Clotting Time
sec
Clot Strength
Pa
Mean (SD)
Mean (SD)
Mean (SD)
sec
Mean (SD)
Mean (SD)
0%
2.7 (0.3)
0.411 (0.033)
259 (61)
10.4 (0.4)
25.7 (1.7)
219 (73)
178 (51)
0.007 (0.003)
10%
2.3 (0.5)
0.370 (0.024)
226 (51)
11.3 (0.7)
26.3 (2.7)
0.005 (0.002)
20%
2.1 (0.5)"
0.347 [0.021]"
199 (37)"
118 (0.6)
296 (28)
217 (70)
0.004 (0.002)
40%
1.2 (0.3)*
0.261 (0.020)*
158 (29)*
13.9 (1.0)*
34.0 (3.0)*
238 (83)
0.003 (0.002)
60%
0.7 (0.2)*
0.197 (0.034)*
94 (16)*
19.1 (3.0)*
50.8 (8.9)*
267 (70)
0.001 (0.001)
Lawrences et al Thrombosis Research 2014;134:488-494
Questi risultati sono particolarmente rilevanti se si considera che solo il 15-20% del
fibrinogeno totale è inglobato nel coagulo, per cui, anche piccole variazioni della
concentrazione di fibrinogeno determinano grandi modificazioni nella forza del coagulo,
tali che il coagulo potrebbe essere così lasso da essere dislocato facilmente, banalmente
anche per effetto della pressione sanguigna; mentre servono diluizioni ben più elevate
per notare alterazioni di PT e aPTT. - ANTICOAGULAZIONE SPONTANEA - normalmente nel nostro organismo sono presenti dei
fattori anticoagulanti che impediscono la coagulazione spontanea del sangue nei vasi. Essi
sono:
●
Proteina C (attivata da Proteina S)
●
Antitrombina III
Nel trauma accade che il danno tissutale e l'ipoperfusione provocano un'aumentata
espressione endoteliale di trombomodulina, che agisce come cofattore della trombina nel
processo di attivazione della proteina C: aumenta cosí l'effetto anticoagulante naturale.
2
G'GP
g1
11
Activated Partial
Mean (SD) - AUTOEPARINIZZAZIONE ENDOGENA - normalmente, la superficie endoteliale è protetta
dal glicocalice, che, tra le altre funzioni, maschera delle molecole eparino-simili presenti
sull'endotelio. Nel trauma, la lesione vasale causa la distruzione del glicocalice, esponendo
le molecole eparino-simili, che mediano un effetto scoagulante. - DISFUNZIONE PIASTRINICA - caratterizzata dall'incapacità delle piastrine di rispondere agli
stimoli (ADP, acido arachidonico, collagene). La disfunzione piastrinica colpisce quasi il
50% dei traumi maggiori e, quando presente, aumenta di 10 volte il rischio di mortalità. - IPERFIBRINOLISI PRECOCE - la fibrinolisi consiste nella degradazione del fibrinogeno ad
opera della plasmina. Se questo meccanismo accade troppo precocemente (come nel caso
di alcuni politraumi), il coagulo verrà distrutto e si avrà una ripresa di un sanguinamento
precedentemente controllato. L'iperfibrinolisi sembra determinata dall'inattivazione del
PAI-1 (Plasminogen Activator Inhibitor), molecola che blocca la formazione di plasmina
tramite inibizione di tPA. L'inattivazione del PAI-1 induce un aumento del tPA, che
attivando il plasminogeno in plasmina, media l'effetto scoagulante.
Protein S
Sphingolipids
HDL
Fibrin Split Products
Fibrin
Va
VIIla
To
Plasmin
Protein C inhibitor
a1-antitrypsin
tPA
PAI-1
aPC
a2-macroglobulin
a2-antiplasmin
Plasminogen
Slow
Fast
PC
PC
TM
Ila
Endothelium
EPCR
Inoltre, il PAI-1 può anche essere inattivato dall'attivazione dei neutrofili, meccanismo che
contribuisce ulteriormente alla riduzione della sua azione.
L'iperfibrinolisi rappresenta un fattore prognostico indipendente per mortalità (Rourke et
al), la cui incidenza dipende dalla gravità del trauma. Esistono delle iperfibrinolisi
conclamate, che portano ad un aumento della mortalità fino al 100%, e delle situazioni
riconducibili ad aumentata attivazione del sistema fibrinolitico, che determinano un
aumento della mortalità variabile.
FENOMENO
Incidenza
Mortalità
IPERFRINOLISI
Conclamata
5%
60-100%
traumi maggiori
Attivazione sistema
fibrinolitico
40-50%
12%
traumi maggiori
(vs. 1%, p<0.01)
Ipotermia
Lo sviluppo di ipotermia nel paziente traumatizzato è causato da:
- permanenza eccessiva sul luogo del trauma (la temperatura ambientale è minore della
termperatura corporea), - infusione di soluzioni fredde/refrigerate o non riscaldate
- perdita
volemica, a seguito della quale si innesca vasocostrizione, cui consegue la
riduzione della temperatura corporea
L'ipotermia alimenta la coagulopatia, agendo a tutti i livelli della coagulazione: - PIASTRINE
○
riduzione della funzionalità piastrinica (per TC < 34°C):
alterazione della forma riduzione dell'emissione di pseudopodi, che le
rende difficilmente ancorabili al fibrinogeno
alterazione della funzione dei recettori di superficie, con conseguente
riduzione dell'aggregazione piastrinica
riduzione del numero di piastrine per aumentato sequestro splenico
○
3 - FATTORI DELLA COAGULAZIONE
○
riduce la produzione e la funzione dei fattori della coagulazione, tale che per ogni
riduzione di 1°℃ si assiste alla riduzione del 10% dell'attività dei fattori della
coagulazione. Quando la temperatura raggiunge valori inferiori a 36°C, il PT e
aPTT si allunga progressivamente.
●
FIBRINOGENO
○
riduce la sintesi di fibrinogeno
○
aumenta la degradazione del fibrinogeno perché attiva la fibrinolisi per inibizione
del PAI-1 e dall'antiplasmina
Inoltre, l'ipotermia influisce sulla funzionalità epatica provocando la riduzione di: - metabolismo del citrato - gli emocomponenti contengono citrato, che riduce l'evenienza di
coagulazione. Normalmente, il citrato viene metabolizzato rapidamente (in circa 30') ma
in caso di ipotermia il metabolismo si rallenta, aumentando il rischio di sanguinamento; - clearance dei farmaci
- sintesi di proteine di fase acuta
Acidosi
L'acidosi è causata da ipoperfusione d'organo con conseguente switch al metabolismo anaerobio,
che determina un'acidosi metabolica con prevalente componente lattica.
All'acidosi metabolica può partecipare l'infusione rapida di soluzione fisiologica con conseguente
acidosi ipercloremica (bastano 1500 ml di SF).
Inoltre, nel paziente traumatizzato non è raro riscontrare una di acidosi respiratoria, come
risultato di un'ipoventilazione con conseguente ipercapnia.
L'acidosi influenza la coagulazione nei seguenti modi:
- per pH < 7.4
○
Riduce l'attivazione dei fattori della coagulazione,
soprattutto della via comune (V e X), anche se meno
intensamente rispetto all'ipotermia; per raggiungere
avere una completa inattivazione dei fattori bisogna
arrivare a pH 6.6
o
Aumenta la degradazione del fibrinogeno
O
Altera la funzionalità piastrinica, che per pH di 6.8
risulta dimezzata
Buffer or HCI
0
PH = 5.9
20.
-t-
ADP
Aggregation (%)
40
PH = 6.8
60
80
PH = 7.4
100
O
1
2
3
5
Time (min)
ADP = adenosine diphosphate
Green FW et al. Gastroenterology. 1978;74:38-43.
ATTIVAZIONE FATTORE V
3
2.5
2
1.5
1
0.5
0
6.2
6.6
7
7.4
7.8
8.2
8.6
9
PH
ATTIVAZIONE FATTORE X
5
4
3
2
1
0
6.2
6.6
7
7.4
7.8
8.2
8.6
9
PH - per pH < 7.10
○
Inibizione generazione di trombina per il 50%
4