Inquadramento clinico del paziente neoplastico: diagnosi e terapia
Documento sull'inquadramento clinico del paziente neoplastico. Il Pdf, adatto a studenti universitari di Biologia, offre una panoramica completa del percorso terapeutico oncologico, esaminando diagnosi, stadiazione, valutazione del paziente e scelta del trattamento, con dettagli su biopsie, citofluorimetria e chemioterapia.
Mostra di più11 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Valutazione della Malattia
- VALUTAZIONE DELLA MALATTIA (Diagnosi e stadiazione)
- VALUTAZIONE DEL PAZIENTE (Performance status, comorbidità, età, ecc ... )
- SCELTA DEL TRATTAMENTO
- VALUTAZIONE DELLA RISPOSTA
- FOLLOW-UP
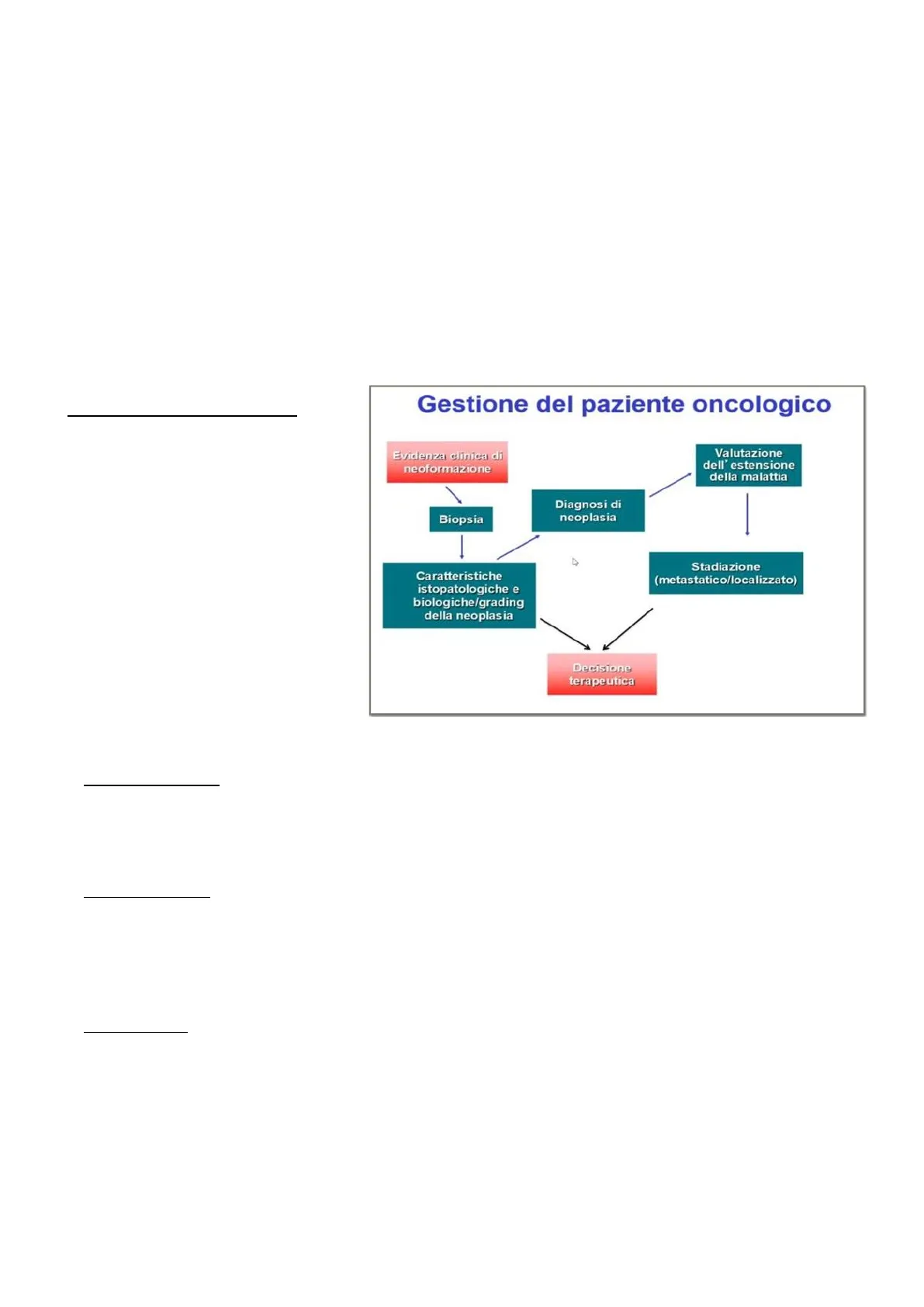
1. VALUTAZIONE DELLA MALATTIA ALGORITMO DIAGNOSTICO Tutto parte dall'evidenza di una neoformazione e dal sospetto che questa possa essere una neoplasia. In presenza di una qualsiasi neoformazione è necessario stabilire con assoluta sicurezza cosa si ha di fronte, cioè dare "un nome ed un cognome" alla malattia. Per fare questo occorre fare un prelievo bioptico che consenta di conoscere la patologia e in virtù di ciò prendere decisioni terapeutiche adeguate.
Gestione del paziente oncologico Evidenza clinica di neoformazione Valutazione dell' estensione della malattia - Biopsia Diagnosi di neoplasia 4 Stadiazione (metastatico/localizzato) Caratteristiche istopatologiche e biologiche/grading della neoplasia Decisione terapeutica
Tipi di Biopsia
Esistono diversi tipi di biopsia:
- biopsia escissionale > rimozione totale della lesione sospetta per neoplasia, estendendo il margine di lesione ad almeno 2-5 mm di cute normale. In questo modo possiamo ottenere informazioni complete non solo sulla natura della lesione ma anche sulle caratteristiche dei tessuti circostanti la neoformazione, quindi valutare se questi siano o meno infiltrati dalla malattia. Se in seguito alla biopsia ho dei margini liberi dalla malattia allora, in alcuni casi, questa forma di biopsia può anche essere curativa
- biopsia incisionale > si preferisce nei casi in cui si necessita della diagnosi ma non è possibile procedere con una biopsia escissionale perché non si hanno dei veri e propri margini ben definiti di tessuto sano che non lasciano molto spazio per muoversi (es. neoplasie dei tumori testa-collo, soprattutto del cavo orale) oppure nei casi in cui si ha una malattia localmente avanzata troppo estesa che non ha un margine di resecabilità. In questo caso viene asportata solo una parte della lesione, per conoscerne la natura neoplastica benigna o maligna o infiammatoria in modo da poter programmare successivamente l'intervento di escissione eventuale in maniera corretta.
- biopsia Tru-cut (o agobiopsia) > "biopsia con ago tranciante"; in sostanza si entra con un ago mediante il quale si preleva un frustolino di tessuto del diametro dell'ago = mininvasivo, utilizzata soprattutto per la diagnosi di tumori alla mammella o alla tiroide. Tuttavia, non è sempre facilissimo da eseguire e non sempre si ottiene un campionamento adeguato: può accadere che sia difficile arrivare direttamente alla sede della malattia oppure che la mano del chirurgo non sia performante al momento del prelievo per cui si può prelevare erroneamente del tessuto sano (soprattutto quando le dimensioni della neoformazione sono ridotte) che falsa la diagnosi che quindi non sarà conclusiva, perciò bisognerà ripetere la biopsia (magari procedendo per via eco-guidata) oppure scegliere una strategia differente. N.B. La biopsia ossea prevede un prelievo di un frustolo di tessuto osseo con metodo simile al tru-cut, frustolo di tessuto osseo che viene poi sottoposto a decalcificazione e analizzato istologicamente come gli altri tessuti.
- agoaspirato > altro approccio meno invasivo con il quale si cerca, attraverso una depressione della siringa, di aspirare del materiale dalla neoformazione. In questo caso però l'ago è più piccolo rispetto a quello utilizzato nella Tru-cut, per cui non si ottiene un frustolino di tessuto ma singole cellule = esame citologico (le cellule aspirate vengono strisciate su vetrino), meno informativo rispetto agli esami precedenti che invece erano istologici e con i quali si può valutare comunque la cellularità alterata ma inquadrandola nel contesto di un tessuto. Con l'agoaspirato è quindi possibile visualizzare delle cellule aberranti che permettono di supporre (con minore o maggiore chiarezza a seconda del caso) la presenza di un processo eteroplastico. Tuttavia si ottengono maggiori informazioni in caso di tumori solidi rispetto ai tumori ematologici: ad esempio, se si esegue l'agoaspirato su un cancro della mammella e si evidenzia una cellularità neoplastica, si è quasi sicuri che questo nodulo abbia bisogno di un'exeresi per cui in questo caso l'agoaspirato mi dà semaforo verde per passare il paziente al chirurgo. Se invece si effettua l'agoaspirato di un linfonodo nel caso di un linfoma la questione si complica perché molto spesso quello che viene fuori è una cellularità ricca in linfociti, cioè il linfonodo presenta un tappeto di linfociti che non da altre informazioni aggiuntive per permettere all'anatomopatologo di poter fare una diagnosi (es. nel linfoma di Hodgkin la cellula patognomica è la cellula di Reed-Sternberg, che però raramente è presente nei tessuti > quindi per fare diagnosi di linfoma si necessita della biopsia linfonodale perché questa permette di mettere in evidenza il sovvertimento architetturale della struttura linfonodale). N.B. L'agoaspirato può essere effettuato anche a livello midollare: in questo caso si utilizza un ago abbastanza robusto perché si deve trapassare la parte di osso compatto e arrivare alla parte spugnosa dell'osso dove, in mezzo alle trabecole, è contenuto il midollo osseo (è la rottura delle trabecole che dà dolore). Il midollo osseo è una sede estremamente importante di diverse attività, tra cui la proliferazione e la maturazione di cellule staminali e progenitori ematopoietici ed è sede di infiltrazione da parte di neoplasie di origine ematopoietica e non (anche i tumori solidi nelle fasi più avanzate possono dare infiltrazioni midollari). In passato (ed oggi in rari casi) l'agoaspirato midollare veniva eseguito a livello sternale, ma l'operazione a livello di questa sede non è ne facile né psicologicamente favorevole per il paziente. La sede più frequentemente utilizzata è la spina iliaca postero- superiore. Una volta aspirato, il sangue midollare prelevato (il quale contiene dei piccoli frustoli costituiti da piccole trabecole ossee rotte durante la procedura) viene posto su dei vetrini e strisciato insieme ai frustoli stessi: questo permette sia una valutazione citologica data dall'aspirato midollare (es. per l'eventuale presenza di cellule blastiche) sia una valutazione istologica data dai frammenti di tessuto osseo asportato. In sostanza l'agoaspirato midollare è un approccio che si utilizza principalmente per valutare lo stato di benessere del midollo osseo, per la stadiazione di alcune neoplasie (si valuta l'eventuale coinvolgimento metastatico del midollo) e qualche volta anche come tentativo diagnostico (es. per le neoplasie di tipo ematologico). Ovviamente questa procedura può anche essere utilizzata nei casi in cui si renda necessario il trapianto di midollo.
Citofluorimetria a Flusso
Componenti del Citofluorimetro
Citofluorimetria a flusso (utilizzata per l'emocromo ma anche per caratterizzare alcune neoplasie ematologiche) COMPONENTI DI BASE DEL CITOFLUORIMETRO 1 Sorgente luminosa Camera di flusso Sistema ottico Rilevatore di luce Computer CAMERA DI FLUSSO Campione (con alcune cellule marcate) Cellule in sospensione Side scatter - complessità cellulare e fluorescenza emessa dalle cellule marcate Forward scatter - dimensione delle cellule sione laser (sorgente luminosa) fluorocromo anticorpo cellula flusso
Tecniche Citofluorimetriche
Questa metodica permette di studiare le cellule presenti nel circolo ematico, nel midollo osseo, nei fluidi corporei (es. liquido cefalorachidiano) o le cellule tumorali. In particolare, la citofluorimetria, o citometria, a flusso è una tecnica di laboratorio che consente di rilevare, contare e caratterizzare specifiche popolazioni cellulari utilizzando un fascio di luce laser (in grado di misurare contemporaneamente alcuni parametri morfologici - in grado di identificare anche componenti particolari contenuti all'interno delle cellule); è detto a flusso perché le cellule fluiscono velocemente e singolarmente "in fila indiana" attraverso il raggio di luce che le colpisce. Le tecniche citofluorimetriche prevedono diverse fasi:
- un campione di cellule viene sospeso in un fluido (il liquido di sheat)
- prima del test e sulla base delle cellule da analizzare, il campione viene trattato con coloranti specifici (fluorocromi) in grado di discriminare i diversi sottotipi cellulari = il fluorocromo è attaccato ad anticorpi monoclonali che riconoscono particolari distretti cellulari o antigeni marcatori. il campione contenente le cellule marcate viene introdotto nello strumento chiamato citofluorimetro. Nello strumento il fluido contenente le cellule viene incanalato nella camera di flusso, cioè attraverso un foro molto stretto in modo tale da creare un flusso all'interno del quale le cellule risultano organizzate in fila, una dietro l'altra. Il flusso di cellule viene posto davanti ad un rilevatore che analizza ciascuna cellula presente all'interno del flusso ad una velocità altissima (da centinaia a migliaia di cellule per secondo)
- il citofluorimetro contiene uno o più laser e più rilevatori in grado di identificare alcune caratteristiche, uniche per ciascuna cellula. Ciascun laser colpisce le cellule presenti nel flusso, generando per ciascuna di esse uno scatter caratteristico e dipendente dalle caratteristiche della stessa. Le caratteristiche possono essere fisiche (dimensione e complessità cellulare) o possono dipendere dal segnale generato dal fluorocromo intercettato dal laser. La combinazione di queste informazioni genera un profilo caratteristico per ciascuna cellula presente all'interno del campione
- il segnale rilevato dai rilevatori (o detector) viene amplificato e inviato al computer e qui convertito in formato digitale e mostrato sul computer sotto forma di grafici (istogrammi o dot-plot)
Applicazioni della Citofluorimetria
Tra le diverse applicazioni della citofluorimetria, di notevole interesse è la possibilità di poter fare diagnosi, classificazione e prognosi dei tumori ematologici, es. leucemie e linfomi. Attraverso l'utilizzo di anticorpi che evidenziano l'eventuale presenza/assenza di particolari marcatori cellulari (antigeni CD - cluster of differentiation) è possibile definire il grado di differenziazione delle leucemie linfoidi acute T e B, parametro di rilevante importanza prognostica.
T cell CD antigen. CD45R CD45R CD28 CD28 CD2 CD2 CD3 TH Tc TCR TCR CD8 CD4 LFA1 LFA1 B cell CD antigen. CD40 CD80 CD86 CD52 CD267 CD19 B Cell CD269 CD22 CD268 CD20 CD32b
La tipizzazione linfocitaria è stata ed è oggi utilizzata anche in altre condizioni, quali malattie autoimmuni, stati di immunodeficienza congenita, malattie ematologiche non tumorali, trapianti.
Biopsia Standard vs Biopsia Liquida
Biopsia Standard
STANDARD BIOPSY
- Procedura +/- invasiva che può essere associata ad un minimo di fastidio/dolore
- Non è di facile esecuzione e non sempre praticabile
- Anche se si tratta di una piccola puntura, in alcuni casi si può associare a molti rischi come nel caso di biopsia polmonare TAC-guidata (pneumotorace) o biopsia epatica (sanguinamenti)
- Time-intensive = procedura che impegna molto tempo
- È un esame limitato al campionamento del tessuto, cioè alla quantità di tessuto che si riesce a prelevare
- Nei casi di malattia metastatica la biopsia potrebbe non essere rappresentativa dell'intero tumore: la neoplasia nasce da un'unica cellula ma da vita molto rapidamente ad una popolazione cellulare eterogenea, costituita cioè da più cloni diversi che possono ulteriormente differenziarsi. Es. il cancro della mammella metastatizza a livello osseo e a livello epatico: questi siti diversi di homing possono indicare che questi cloni hanno sviluppato caratteristiche specifiche che hanno permesso loro di insinuarsi in queste nuove sedi. Per cui in caso di metastasi si potrebbe avere una malattia molto dedifferenziata che non ricorda più il tessuto di origine, rendendo difficoltosa la caratterizzazione della neoplasia primaria
Biopsia Liquida
LIQUID BIOPSY
- Minimamente invasiva (bisogna effettuare solo un prelievo di sangue periferico, quindi un emocromo specifico)
- Minori rischi e minimo dolore
- Facilmente ottenibile, veloce, ripetibile
- È possibile mettere in evidenza eventuali cellule tumorali rilasciate nella circolazione sistemica o anche materiale genetico (DNA circolante), così da ottenere informazioni sulle mutazioni (anche in caso di più cloni cellulari) e quindi su tutto il tumore rappresentato nella persona > in base a ciò che si ottiene si può meglio definire una strategia terapeutica efficace
- È un campo ancora nuovo e non ancora pienamente validato per uso clinico (si sta lavorando affinché in futuro possa diventare tecnica di routine): ad oggi viene principalmente utilizzata quando non si hanno a disposizione altre opzioni diagnostiche per cercare di capire se la neoplasia esprime determinate mutazioni > davanti ad una neoplasia rara oppure una neoplasia frequente ma recidivante/resistente a tutti i trattamenti standard, la liquid biopsy permette di evidenziare eventuali mutazioni driver che verranno sfruttate per un nuovo approccio terapeutico. Non è pertanto utile negli stadi precoci di malattia !!!
CD3