Emergenze medico-chirurgiche: ossigenoterapia e ventilazione per insufficienza respiratoria
Documento del Prof. Monti G. su Emergenze medico-chirurgiche – O2 terapia e ventilazione. Il Pdf esplora le strategie terapeutiche per l'insufficienza respiratoria, concentrandosi sull'ossigenoterapia e la ventilazione, utile per lo studio universitario.
Mostra di più13 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Emergenze Medico-Chirurgiche
O2 Terapia e Ventilazione
Pag. 1 a 13
Emergenze medico-chirurgiche - Prof. Monti G. - Dispnea, O2 terapia, ventilazione
Emergenze medico-chirurgiche
O2 terapia e ventilazione
Prof. Giacomo Monti - 12/03/2024 - Autori: Ilaria Leonardo, Marco Gambirasio - Revisore: Francesca Pirone
Le strategie terapeutiche dell'insufficienza respiratoria si basano su tre cardini:
- Terapia eziologica: il professore rimanda a quanto studiato nei corsi precedenti e in particolare consiglia
di ripassare il trattamento (con dosaggi) di edema polmonare acuto (nitroglicerina per le crisi ipertensive),
CAP (community-acquired pneumonia) e BPCO riacutizzata. - Terapia di supporto: mantiene in vita il paziente così da permettere alla terapia eziologica di fare effetto;
si compone di tre presidi terapeutici- Ossigenoterapia
- Ventilazione non invasiva (NIV)
- Ventilazione meccanica invasiva (MIV)
- Prevenzione delle complicanze precoci e tardive: questo vale soprattutto nella ventilazione meccanica
e in particolare per l'iperossia, che può derivare dal trattamento dell'insufficienza respiratoria ipercapnica.
Ossigenoterapia
L'ossigenoterapia è il capostipite del supporto respiratorio.
Bisogna sempre ricordare che l'ossigeno è un farmaco, che va somministrato secondo un preciso schema
terapeutico basato su concentrazioni (FiO2) e dosi-tempi (L/min) prestabiliti. Quello che interessa realmente
è la FiO2 perché ci sono diverse modalità (tipi di device e L/min) per ottenere una stessa FiO2.
Strumenti per la Somministrazione di Ossigeno
Gli strumenti a disposizione per la somministrazione di ossigeno sono:
- Cannule nasali a basso flusso (LFNC): sono ben tollerate ma non permettono di erogare quantità di
ossigeno troppo alte. Scolasticamente si fa riferimento a un limite di 6 L/min di ossigeno da poter erogare
con le cannule nasali, al di sopra del quale si rischia di causare perforazione nasale; in realtà il limite
dovrebbe essere più basso (intorno ai 3-4 L/min). - Maschera di Venturi (il più diffuso): questo presidio permette di erogare quantità
maggiori di ossigeno nel tempo e contestualmente di somministrarlo ad una FiO2
nota e compresa tra 28 e 85%. Il limite massimo erogabile è 15 L/min, che
corrisponde ad una FiO2 del 60%.
Le machere di Venturi sono dei dispositivi fisici che permettono di creare un flusso
d'aria che va verso il paziente, con una miscela nota di ossigeno e aria ambiente,
attraverso la combinazione tra le proprietà meccaniche del nottolino (o venturimetro,
ovvero la parte colorata del sistema) e il flusso di O2 che viene selezionato a livello
dell'erogatore (L/min). Ad ogni colore del nottolino corrispondono dimensioni
diverse sia del foro interno (per il passaggio del flusso di O2) che dei fori sull'ugello
(per il passaggio dell'aria ambiente).
Il funzionamento del device si basa sull'effetto Venturi: quando il flusso di O2 passa
attraverso una riduzione di calibro, la pressione si riduce e la velocità del flusso
aumenta; questo crea una depressione (pressione subatmosferica) nello spazio oltre
il foro, ovvero un effetto "vuoto" che risucchia l'aria ambiente dentro il sistema
attraverso le aperture del venturimetro.
Solo il corretto accoppiamento tra il colore del nottolino e il flusso di O2 genera
una miscela con FiO2 nota e un flusso adeguato al picco di flusso espiratorio del
malato. Al crescere della FiO2 che si vuole ottenere, la dimensione dei buchi
sull'ugello diminuisce in modo da pescare meno aria ambiente e prenderne di più
dalla sorgente di O2.
Quindi, quando si prescrivere l'ossigenoterapia tramite maschera di Venturi è
importante prescrivere la FiO2 desiderata, così che l'infermiere accoppi i L/min al
nottolino corretto. Se il malato non migliora con la terapia impostata, per aumentare
la FiO2 bisogna aggiustare sia i L/min che cambiare il nottolino.
Tabella Colore, Flusso e Concentrazione
Colore
azzurra
bianca
arancione
gialla
rossa
verde
reservoir
Flusso
2 l/min
4 l/min
6 l/min
8 l/min
10 l/min
15 l/min
15 l/min
Conc.
24%
28%
31%
35%
40%
60%
75-85%
Air
Air
aria
fonte di O2
paziente
O
O
aria
aria
O
O2
AirEmergenze medico-chirurgiche - Prof. Monti G. - Dispnea, O2 terapia, ventilazione
Pag. 2 a 13
Ad esempio, se si vuole passare dal 31% al 35% bisogna sostituire il nottolino arancione con il giallo.
Questo perché passare direttamente da 6 L/min a 8 L/min non permette di sapere esattamente quello che
sta succedendo e non è scontato che la FiO2 salga.
- Maschera con reservoir: è costituita da una maschera collegata a un sacchetto (reservoir),
nel quale entra 02 con una concentrazione del 100%; la maschera è dotata di due valvole
che si chiudono in inspirazione (per collasso) e si aprono in espirazione (circuito
monodirezionale di non-rebreathing). Nonostante la FiO2 nel reservoir sia del 100%, con
un flusso di 15 L/min il paziente arriva a respirare una FiO2 del 75-85% perché non c'è
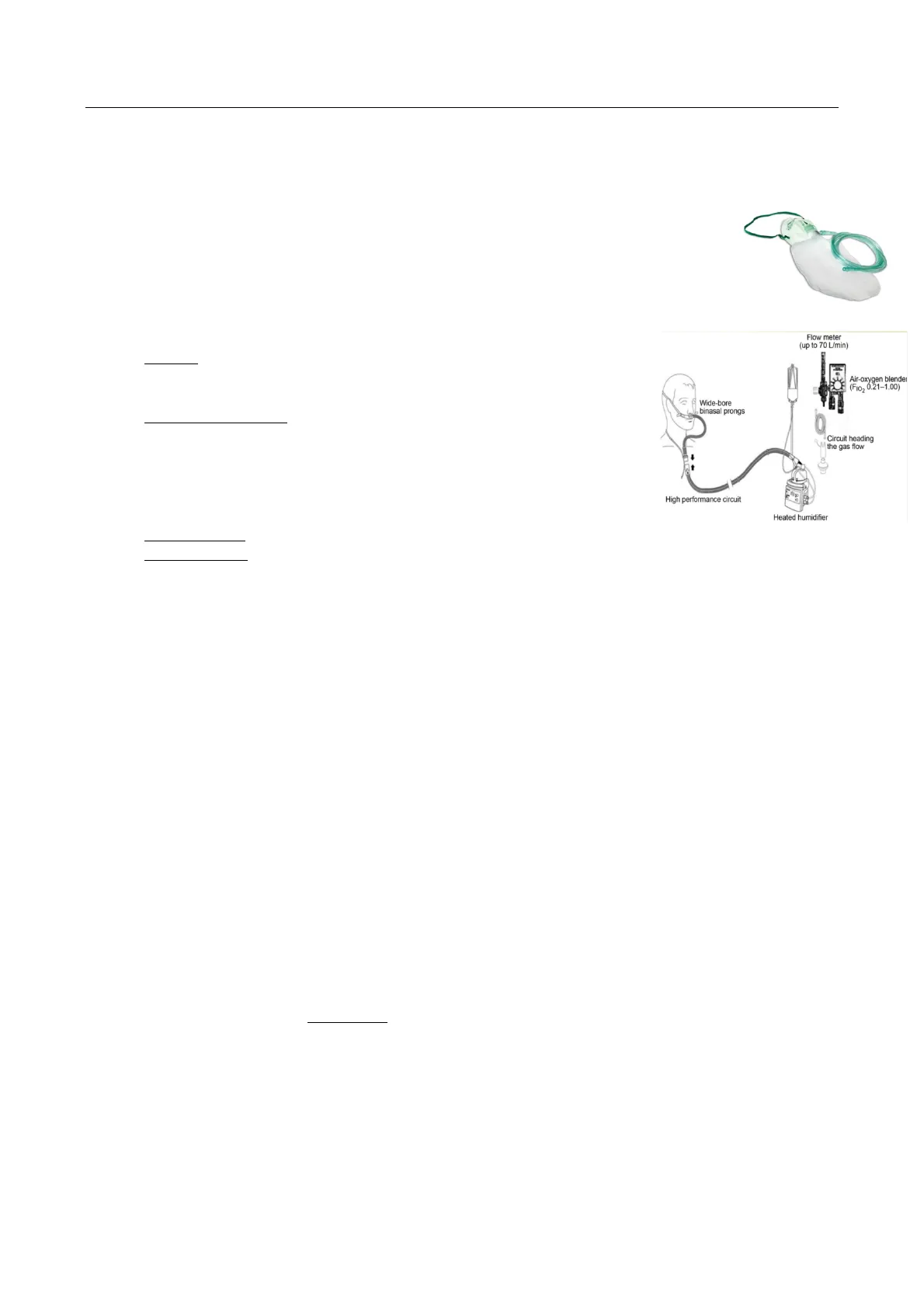
un sigillo completo sulla faccia e questo permette l'infiltrazione di un po' di aria ambiente. - Cannule nasali ad alto flusso (HFNC): è il device più moderno, costituito da
- Blender (miscelatore): sistema capace di generare una mescola di aria e
ossigeno in proporzioni variabili, che permette di raggiungere FiO2 dal
21% (solo aria ambiente) al 100% (solo O2 puro). - Umidificatore attivo: il flusso d'aria che va verso il malato entra in
contatto con una sorgente di umidità (una campana in cui viene fatta
scaldare dell'acqua); in questo modo l'aria viene saturata con vapore
acqueo a una temperatura di 30°-40°; l'umidificazione dell'aria evita la
perforazione del setto nasale, cosa che avverrebbe sparando alte quantità
di O2 (gasso secco) direttamente nel naso.
Flow meter
(up to 70 L/min)
Air-oxygen blender
(FIO2 0.21-1.00)
Wide-bore
binasal prongs
Circuit heading
the gas flow
High performance circuit
Heated humidifier - Sistema di tubi, che porta il flusso d'aria verso il paziente.
- Cannule nasali, più performanti rispetto alle classiche cannule dell'ossigeno.
- Blender (miscelatore): sistema capace di generare una mescola di aria e
Vantaggi delle HFNC
Solitamente, quando bisogna aumentare la FiO2, si preferisce abbandonare gli occhialini a favore delle
maschere che coprono tutta la faccia (naso e bocca) perché se l'O2 entra dal naso ma il malato respira con
la bocca (che è libera nel caso delle cannule nasali) ovviamente non respira quello che gli vogliamo dare;
dunque, uno dei limiti degli occhialini è l'imprevedibilità del risultato, che dipende dalla modalità di
respirazione del malato.
Questo limite nelle HFNC viene superato dal fatto che il flusso di mescola erogato va dai 20 ai 60 L/min,
superiore al picco di flusso inspiratorio del malato (circa 15 L/min). Se, per esempio, diamo ossigeno a un
flusso di 3 L/min, il paziente prende i restanti 12 L/min dalla bocca. Se, invece, il malato inspira ossigeno
a 20 L/min, i 5 L/min in eccesso escono dalla bocca; nelle HFNC, quindi, il cavo orale viene riempito dalla
mescola che somministriamo e in questo modo, anche respirando dalla bocca, il malato respira l'aria che
noi gli abbiamo messo in bocca attraverso il naso. Il vantaggio delle HFNC è che la bocca è libera e quindi
il malato può mangiare, parlare e sentirsi meno claustrofobicamente costretto dalla mascherina.
Le HFNC oltre ad essere un sistema di ossigenoterapia, perché permettono di modificare la FiO2 respirata
dal paziente aumentando la quantità di ossigeno nella mescola respiratoria, permettono anche di mettere
in atto una terapia basata sulle pressioni, perché riescono a creare una minima pressione positiva di fine
espirazione (PEEP). Infatti, quando il malato è posto di fronte a un flusso che arriva fino a 60 L/min,
l'espirazione sarà più difficoltosa e questo fa si che la pressione residua nel polmone alla fine
dell'espirazione aumenti. Quindi, le HFNC sono un sistema a ponte tra reservoir/Venturi e la CPAP.
Indicazioni per HFNC
Le due indicazioni principali le HFNC sono i pazienti:
- Ipossici lievi perché grazie alla PEEP è possibile ottenere una minima pressione invasiva in continuo.
- Bronchitici cronici, che hanno bisogno di ridurre lo spazio morto anatomico (volume di aria
intrappolata nelle vie aeree di conduzione, in cui non avviene la diffusione dell'O2 e della CO2 fra aria
e sangue e che è quindi ipercapnico); le HFNC, portando via i 150-200 mL di aria contenuta nel cavo
orale, riducono lo spazio morto anatomico perché accorciano la via aerea attraverso una sorta di
"tracheostomia virtuale" (spostano l'apertura della via aerea dalla bocca/naso alla faringe).
- Tubi endotracheali
Questi device permettono di somministrare solo ossigeno (a FiO2 diverse a seconda del sistema), ma non
pressione (ad eccezione, come visto, della HFNC).
È importante individuare in quali pazienti è necessario intraprendere l'ossigenoterapia, perché questa, se non
necessaria, può essere dannosa. La review in basso illustra che non si deve mai somministrare O2 quando ilEmergenze medico-chirurgiche - Prof. Monti G. - Dispnea, O2 terapia, ventilazione
Pag. 3 a 13
malato ha una SpO2 ≥ 96%. Il limite inferiore, al di sotto del quale è necessario iniziare la terapia, può variare
tra il 93% e il 90% in relazione alla patologia di base del malato.
La review mostra come l'ossigenoterapia in pazienti con ictus acuto o infarto miocardico causa un aumento
del danno neurologico e della mortalità oltre che della ricorrenza di infarto.
Raccomandazioni sull'Ossigenoterapia
Overview of recommendations
Recommendation 1 STRONG
Stop oxygen therapy no higher
than 96% saturation
Recommendation 2 WEAK
We suggest not starting oxygen
therapy between 90-92% saturation
Peripheral capillary
oxygen saturation (SpO2)
100
99
98
96
95
94
92
91
90
89
88
87
or myocardial
infarction
Applies to:
Acutely ill adult
medical patients
(with exceptions)
Recommendation 3
Do not start oxygen therapy
at or above 93% saturation
Recommendation 3 - lower limit (>92%)
Comparison of benefits and harms - patients with stroke
Favours oxygen therapy
No Important difference
Favours na oxygen therapy
In hospital
Events per 1000 people
Evidence quality
* * * * Moderabe
3-6 months
Functionally depend
Ne Important differentt
#### MOOHAR
Severe disability
Ne Important different#
. . . . Moderate
Comparison of benefits and harms - patients with myocardial infarction
Favours ory
No Important different
Favours na oxygen therapy
In hospital
Events per 1000 people
Evidence quality
Mortality
Ne Important difference
* * * * Moderate
Chest pain requiring antanginal
No Important difference
* * * * Moderate
6 months
Oxygen therapy
No oxygen therapy
Coronary revascularisation
106
Modera
Strong
Weak
Weal
Strong
6 months to 1 year
Recument myocardial infarction
11 fewer
. . . . Huth
Trattamento Insufficienza Respiratoria di Tipo II
L'insufficienza respiratoria di tipo II è causata da un difetto di pompa ed è caratterizzata da ipercapnia
(causata dalla riduzione della ventilazione alveolare).
Terapia Eziologica per Insufficienza Respiratoria Tipo II
La terapia eziologica si differenzia in base alla componente responsabile dell'insufficienza respiratoria:
- Sistema nervoso centrale:
- In caso di intossicazione, talvolta è possibile utilizzare degli antidoti come il flumazenil per le
benzodiazepine o il naloxone per gli oppioidi; in alcuni casi è possibile contrastare l'azione dei
barbiturici tramite la dialisi; - In caso di ictus che colpisce i centri del respiro si può intervenire con la trombolisi.
- In caso di intossicazione, talvolta è possibile utilizzare degli antidoti come il flumazenil per le
- Sistema nervoso periferico (placca neuromuscolare):
- Esistono antagonisti (es. atropina o inibitori dell'acetilcolinesterasi come la neostigmina) efficaci
contro i curari non depolarizzanti, che bloccano la trasmissione a livello della placca neuromuscolare. - Gli inibitori dell'acetilcolinesterasi (es. piridostigmina) sono utilizzati anche per il trattamento della
miastenia gravis; è importante ricordare che bisogna evitare l'utilizzo di corticosteroidi in acuto perché
possono peggiorare la sintomatologia. - Nella sindrome di Guillan-Barrè vengono somministrate immunoglobuline e, eventualmente, si può
prendere in considerazione il plasma exchange (anche nella miastenia gravis).
- Esistono antagonisti (es. atropina o inibitori dell'acetilcolinesterasi come la neostigmina) efficaci
- Parete toracica: il volet costale è la patologia acuta della parete toracica che può causare insufficienza
respiratoria di tipo II perché è caratterizzato da fratture costali multiple in più punti con conseguente perdita
della partecipazione all'atto respiratorio di una parte della parete toracica; è uno dei pochi casi che pone
indicazione a fissazione costale chirurgica; tuttavia, il trattamento in acuto prevede la ventilazione a
pressione positiva (non necessariamente invasiva). - Vie aeree: in caso di patologie come asma e bronchite cronica il trattamento prevede broncodilatatori
(salbutamolo, 2-4 puff oppure, in pazienti dispnoici, 5 mg/ml di fisiologica in aerosol) e steroide
(metilprednisolone 40 mg in un persona normopeso o idrocortisone 200-250 mg).
Il problema è che tutti questi interventi terapeutici richiedono una finestra temporale più o meno lunga per
avere effetto e il paziente che non respira necessità di un intervento di supporto immediato che permetta di
sostituire la funzione di pompa.
Terapia di Supporto per Insufficienza Respiratoria Tipo II
La terapia di supporto nell'insufficienza respiratoria di tipo II si basa
sull'aumentare la ventilazione alveolare (VA), ovvero la quantità di aria che
raggiunge gli alveoli: in questo modo, al netto della produzione di CO2, si ha una
riduzione della PACO2, che è uguale alla PaCO2.
L'aumento della ventilazione alveolare si può ottenere andando ad aumentare:
- Frequenza respiratoria (FR): all'aumentare della frequenza respiratoria
aumenta la ventilazione alveolare; c'è stato un breve periodo in cui erano in uso
farmaci stimolanti del respiro, cioè delle sostanze che erano in grado di aumentare
la FR, ma non erano efficaci e quindi sono stati abbandonati; ad oggi l'unica
strategia per modificare la frequenza respiratoria è la ventilazione. - Volume tidal (VT, volume corrente), ovvero la quantità di aria inspirata ed
espirata durante un ciclo respiratorio normale.
PaCO2 EQUATION
PaCO2 (mmHg)
@rishirtcod
863
PaCO2
VA
alveolar ventilation (VA, L/min)
Mortality
18 fewer
93
or
+
Acute stroke
Acute myocardial
infarction
xygen saturation of greater
than 92% on ambient air
Oxygen
therapy
Provision of
supplemental
Drypen
or
No oxygen
therapy
No provision of
supplemental
caygen
97
93
Applies to:
Patients with
acute stroke
STRONG
We recommend not providing oxygen therapy
Applies to people with: